Clear Sky Science · zh
膳食铜驱动的结肠菌群失衡通过氧化应激和丁酸缺乏促进猪体内抗性基因库扩散
猪饲料为何关乎人类健康
农民常在猪饲料中额外添加铜,以帮助幼猪生长并抵抗感染。但这种有益的金属可能有隐含的负面影响:它会助长对抗生素不再敏感的细菌的出现和传播。本研究跟踪了以不同形式膳食铜饲养的仔猪,展示了日常养殖做法如何悄然重塑肠道、居住其间的微生物以及最终可能进入更广泛环境并影响人类的抗性基因库。
两种铜来源,两种截然不同的肠道
研究人员比较了三组断奶仔猪:一组不添加铜,一组摄入常用的无机铜盐(硫酸铜),另一组补充有机铜-肽制剂。猪只连续四周食用这些“高铜”饲料;随后所有组转为两周无铜饲料。通过测序动物粪便中的全部DNA,研究团队不仅能追踪哪些细菌存在,还能识别哪些细菌携带使其对抗生素或铜、锌等金属产生耐受的基因。
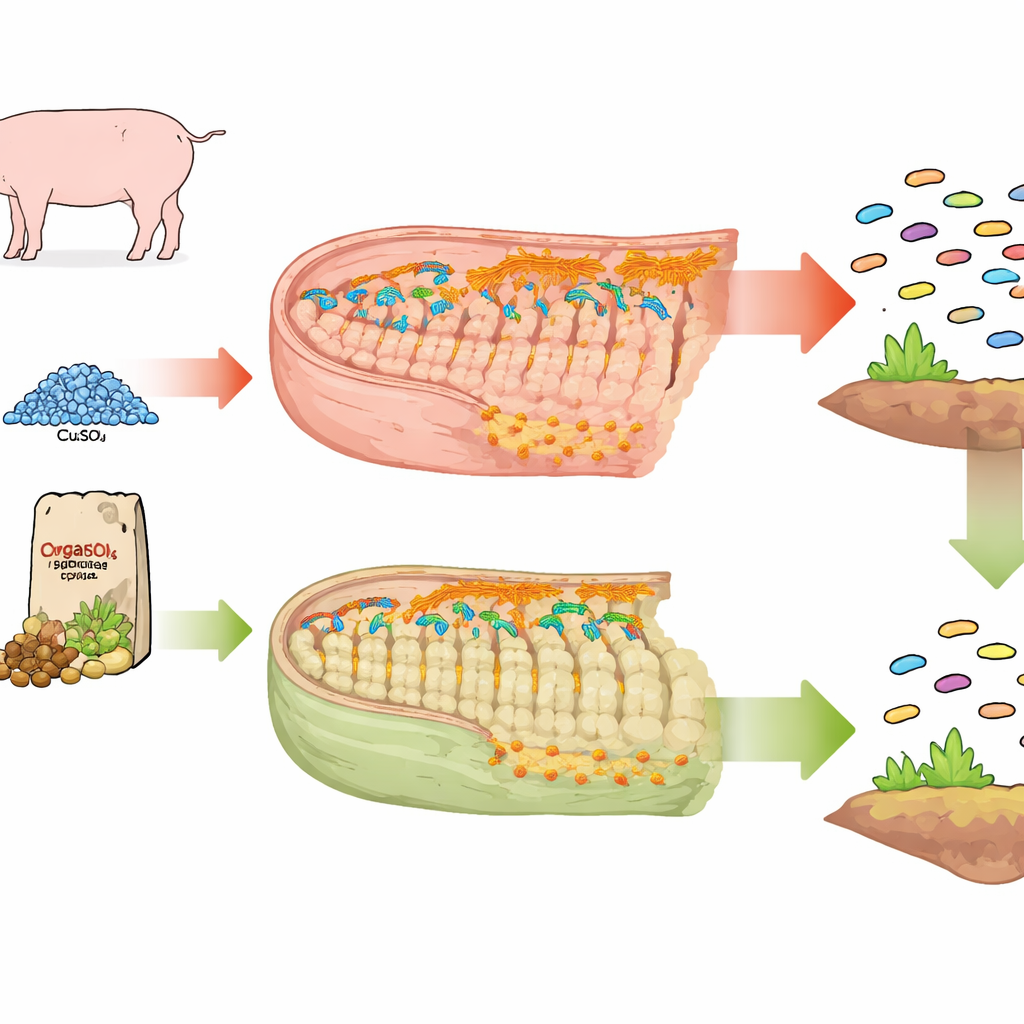
无机铜如何扰乱微生物群落
与无铜饮食的猪相比,喂食硫酸铜的仔猪在肠道中形成了更多、更密集的抗生素耐药基因和金属耐受基因。许多这些基因能同时保护细菌免受多类抗生素的作用。它们也常与可移动遗传元件相关联——例如质粒和转座子等可在微生物间跳跃并转运耐药性状的微小DNA片段。在硫酸铜饲喂下,致病性细菌如大肠埃希菌、猪链球菌和肠球菌等成为这些基因的更常见宿主,使肠道群落变成更大且更危险的耐药储库。
从健康屏障到渗漏、受压的结肠
硫酸铜的饮食不仅改变了微生物的构成,还损害了肠道的物理防御。在显微镜下,这些猪的结肠黏膜出现肿胀、组织排列紊乱和炎症信号。负责将相邻细胞紧密连接的保护性蛋白水平下降,表明屏障更易渗漏。与此同时,结肠和血液中氧化应激标志物增多——即那些可损伤DNA的活性氧化产物。产生丁酸的有益细菌减少,而丁酸(一种为结肠细胞提供能量并帮助维持低氧、稳定环境的短链脂肪酸)在肠道中的含量也下降。
为何有机铜看起来更安全
有机铜-肽补充剂则呈现不同情形。尽管它会像任何铜源一样提升铜耐受基因,但并未引发同样范围的抗生素耐药或可移动遗传元件的激增。致病菌并未显著被偏向,肠道屏障受损和丁酸水平下降也要温和得多。由于这种铜更易在消化道上部被吸收,较少到达结肠去扰动定植微生物。将所有猪转为无铜饲料后,来自硫酸铜组的大多数金属耐受基因下降,但抗生素耐药基因仍然居高不下,表明肠道生态系统发生了持久改变。相比之下,有机铜组的变化要小得多。
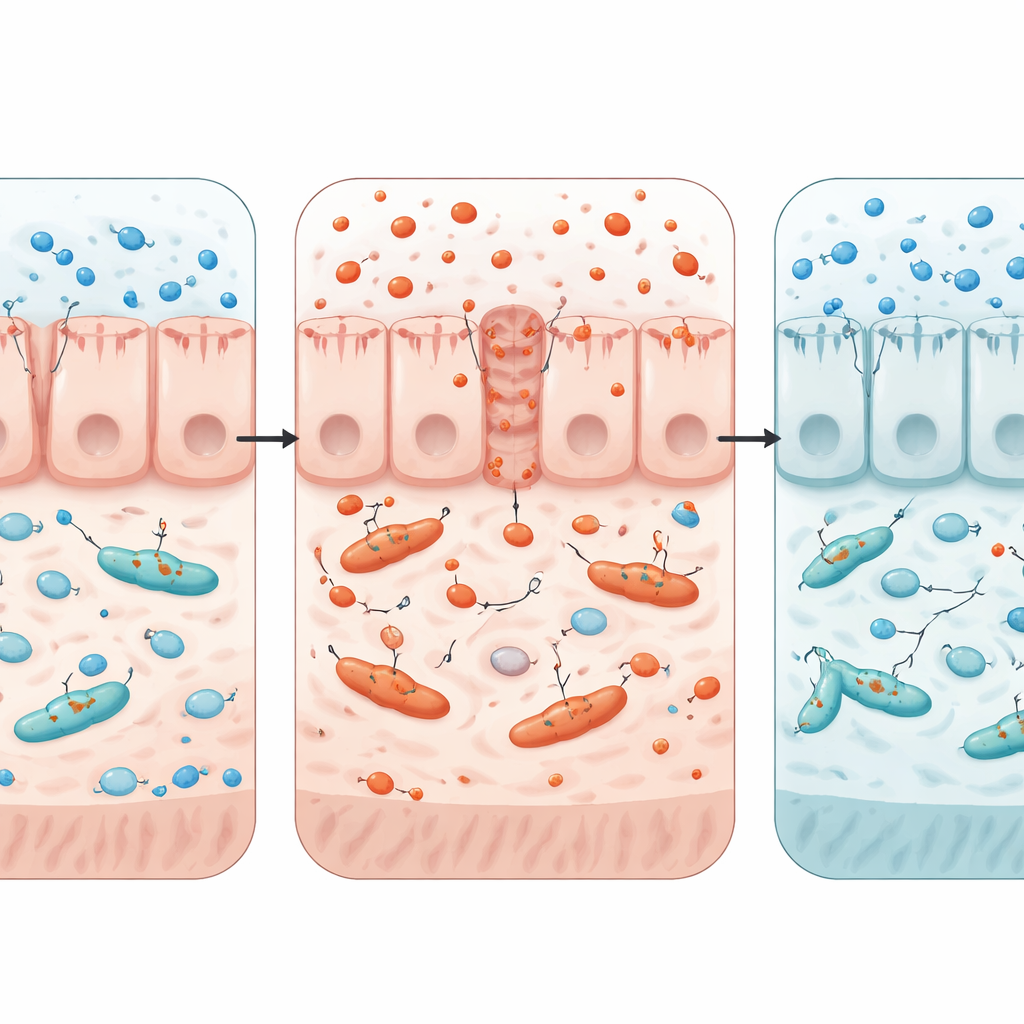
放大机制观察
为检验肠道条件如何影响耐药传播,团队建立了一个实验室模型,将类人肠上皮细胞层与两株可交换携带耐药质粒的大肠埃希菌结合。加入铜离子会增加细胞的氧化应激,削弱屏障,并提高耐药质粒在细菌间转移的速率。当研究者补充丁酸或模拟健康结肠的低氧环境时,氧化应激下降,屏障加强,基因转移减慢。这些测试支持这样的观点:促使耐药基因扩散的不是铜本身,而是铜触发的氧化应激和失去稳定、低氧的肠道环境。
对养殖场之外的意义
这项工作表明,常规在猪饲料中使用无机铜可通过损伤结肠、耗竭产生丁酸的有益菌并促使处于应激且富含可移动DNA的病原体增多,从而悄然扩大并动员动物肠道内的耐药基因集合。有机铜来源虽非完全无风险,但似乎能在较少干扰肠道平衡和耐药传播的情况下,仍提供生长收益。对农场主、兽医和公共卫生规划者而言,信息很明确:选择常用矿物补充剂的形式,有助于在任何抗生素使用之前抑制难治感染的上升。
引用: Wen, Y., Gao, M., Wang, Z. et al. Dietary copper-driven colonic dysbiosis mediates oxidative stress and butyrate deficiency to facilitate the spread of resistome in pigs. npj Biofilms Microbiomes 12, 80 (2026). https://doi.org/10.1038/s41522-026-00949-1
关键词: 抗微生物耐药性, 猪肠道微生物组, 膳食铜, 丁酸与肠道健康, 可移动耐药基因