Clear Sky Science · fr
La dysbiose colique induite par le cuivre alimentaire favorise le stress oxydatif et la carence en butyrate, facilitant la dissémination du réservoir de résistances chez le porc
Pourquoi l’alimentation des porcs compte pour la santé humaine
Les éleveurs ajoutent souvent du cuivre dans l’alimentation des porcelets pour favoriser la croissance des jeunes animaux et les aider à lutter contre les infections. Mais ce métal bénéfique peut avoir un revers caché : il peut favoriser l’émergence et la propagation de bactéries devenues résistantes aux antibiotiques. Cette étude suit des porcelets élevés avec différentes formes de cuivre alimentaire et montre comment une pratique agricole courante peut modifier subtilement l’intestin, les microbes qui y vivent et le pool de gènes de résistance susceptible d’atteindre l’environnement plus large et, potentiellement, l’homme.
Deux types de cuivre, deux microbiotes très différents
Les chercheurs ont comparé trois groupes de porcelets sevrés : un groupe sans cuivre ajouté, un recevant un sel inorganique de cuivre classique (sulfate de cuivre) et un troisième recevant un supplément organique de cuivre‑peptide. Pendant quatre semaines, les porcs ont consommé ces régimes « riches en cuivre » ; ensuite, tous les groupes ont été passés à une alimentation sans cuivre pendant deux semaines supplémentaires. En séquençant tout l’ADN présent dans les selles des animaux, l’équipe a pu suivre non seulement quelles bactéries étaient présentes, mais aussi lesquelles portaient des gènes conférant une résistance aux antibiotiques ou aux métaux comme le cuivre et le zinc.
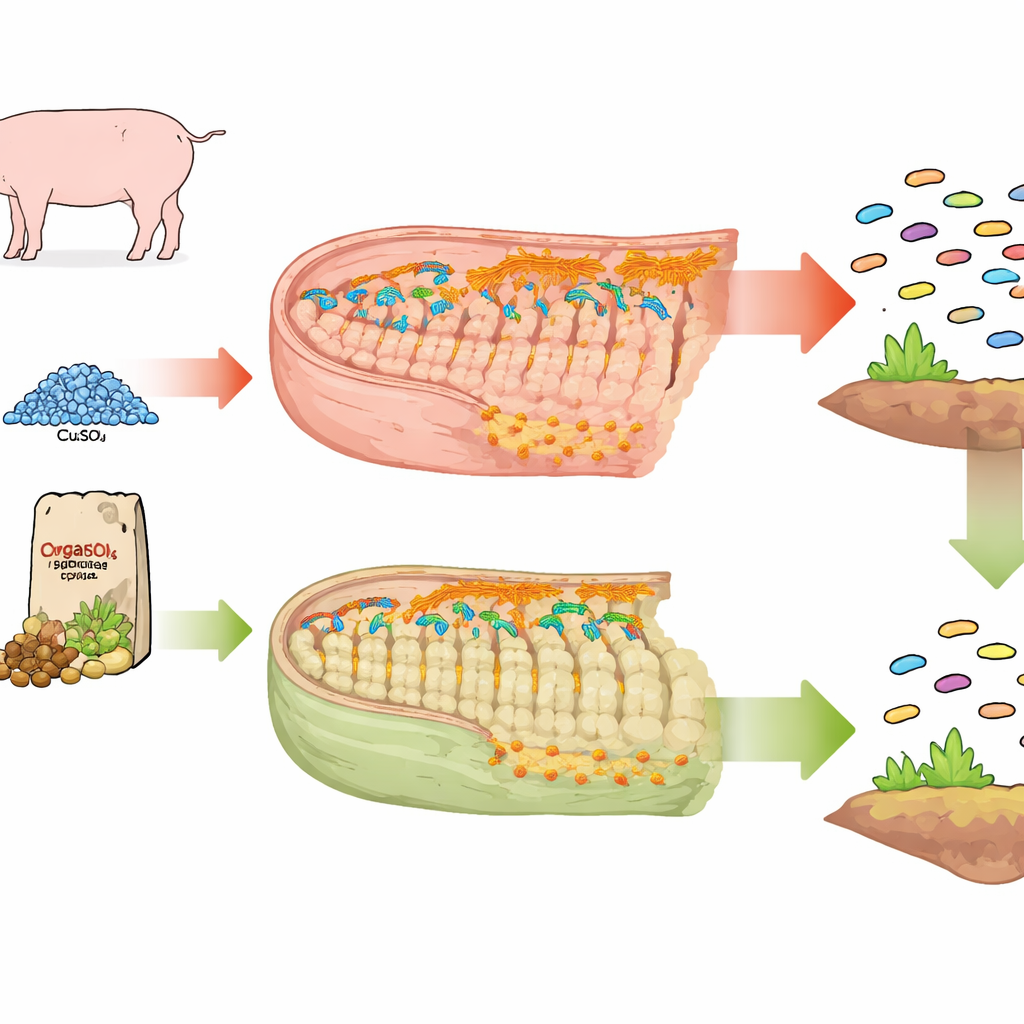
Comment le cuivre inorganique perturbe le voisinage microbien
Les porcelets nourris au sulfate de cuivre ont développé une collection beaucoup plus riche et dense de gènes de résistance aux antibiotiques et aux métaux dans leur intestin comparativement aux porcs d’un régime sans cuivre. Nombre de ces gènes protègent les bactéries contre plusieurs familles d’antibiotiques à la fois. Ils étaient aussi souvent associés à des éléments génétiques mobiles — de petits fragments d’ADN, comme des plasmides et des transposons, qui sautent d’un microbe à l’autre et transportent des traits de résistance. Des bactéries pathogènes comme Escherichia coli, Streptococcus suis et des espèces d’Enterococcus sont devenues des réservoirs plus fréquents de ces gènes sous l’alimentation au sulfate de cuivre, transformant la communauté intestinale en un réservoir de résistance plus large et plus dangereux.
D’une barrière saine à un côlon perméable et stressé
Le régime au sulfate de cuivre n’a pas seulement modifié la composition microbienne ; il a aussi endommagé les défenses physiques de l’intestin. Au microscope, la muqueuse colique de ces porcs présentait un gonflement, un désordre tissulaire et des signes d’inflammation. Les niveaux de protéines protectrices qui scellent les cellules voisines étaient plus faibles, indiquant une barrière plus perméable. Parallèlement, le côlon et le sang contenaient davantage de marqueurs de stress oxydatif — des sous‑produits chimiques appelés espèces réactives de l’oxygène susceptibles d’endommager l’ADN. Les bactéries bénéfiques productrices de butyrate, un acide gras à courte chaîne qui alimente les cellules coliques et contribue à maintenir un environnement stable et peu oxygéné, ont été réduites, et les taux de butyrate dans l’intestin ont chuté.
Pourquoi le cuivre organique paraît plus sûr
Le supplément organique cuivre‑peptide raconte une histoire différente. Bien qu’il augmente aussi les gènes de résistance au cuivre — comme toute source de cuivre — il n’a pas provoqué la même expansion générale des résistances aux antibiotiques ni des éléments génétiques mobiles. Les bactéries pathogènes n’ont pas été fortement favorisées et les lésions de la barrière intestinale ainsi que la baisse du butyrate ont été bien plus modérées. Comme cette forme de cuivre est mieux absorbée plus haut dans le tube digestif, il semble que moins atteigne le côlon pour perturber les microbes résidents. Lorsque tous les porcs ont été passés à une alimentation sans cuivre, la plupart des gènes de résistance aux métaux du groupe sulfate de cuivre ont diminué, mais les gènes de résistance aux antibiotiques sont restés élevés, témoignant de changements durables dans l’écosystème intestinal. En revanche, le groupe cuivre organique a peu changé.
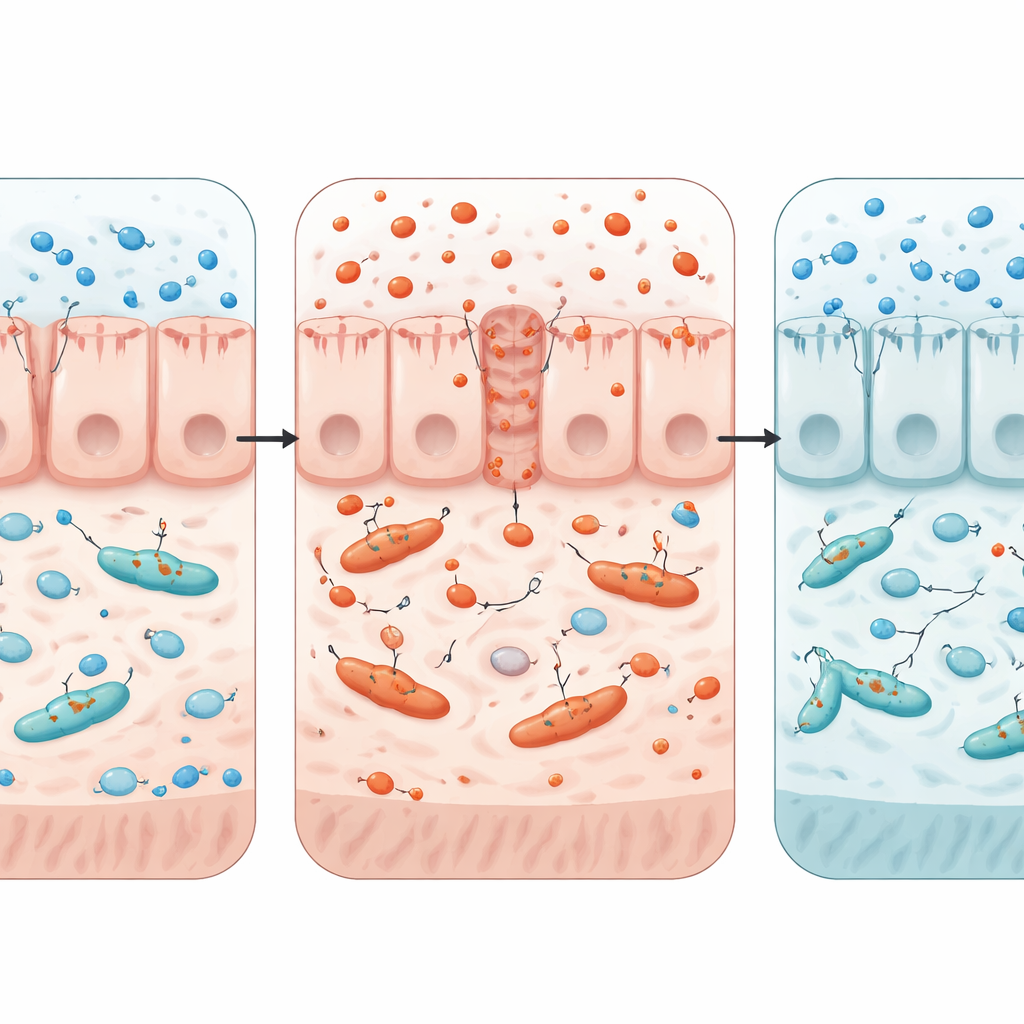
Approfondir le mécanisme
Pour tester comment les conditions intestinales influencent la propagation des résistances, l’équipe a construit un modèle de laboratoire combinant une couche de cellules intestinales de type humain et deux souches d’E. coli capables d’échanger un plasmide porte‑résistance. L’ajout d’ions cuivre a augmenté le stress oxydatif dans les cellules, affaibli la barrière et accéléré la vitesse à laquelle le plasmide de résistance circulait entre les bactéries. Lorsque les chercheurs ont ajouté du butyrate ou reproduit les conditions de faible oxygène d’un côlon sain, le stress oxydatif a diminué, la barrière s’est renforcée et le transfert de gènes a ralenti. Ces tests soutiennent l’idée que ce n’est pas le cuivre seul, mais le stress oxydatif déclenché par le cuivre et la perte d’un milieu intestinal stable et pauvre en oxygène, qui ouvrent la porte à la propagation des gènes de résistance.
Ce que cela signifie au‑delà de la ferme
Ce travail suggère que l’utilisation routinière de cuivre inorganique dans l’alimentation porcine peut élargir et mobiliser discrètement le réservoir de gènes de résistance dans l’intestin de l’animal en blessant le côlon, en appauvrissant les microbes producteurs de butyrate bénéfiques et en favorisant des agents pathogènes stressés et riches en ADN mobile. Les sources de cuivre organique, bien qu’elles ne soient pas totalement dénuées de risque, semblent offrir les avantages de croissance avec beaucoup moins de perturbation de l’équilibre intestinal et de la dissémination des résistances. Pour les agriculteurs, les vétérinaires et les responsables de la santé publique, le message est clair : choisir la forme d’un supplément minéral courant peut contribuer à freiner l’essor d’infections difficiles à traiter, avant même l’utilisation d’un antibiotique.
Citation: Wen, Y., Gao, M., Wang, Z. et al. Dietary copper-driven colonic dysbiosis mediates oxidative stress and butyrate deficiency to facilitate the spread of resistome in pigs. npj Biofilms Microbiomes 12, 80 (2026). https://doi.org/10.1038/s41522-026-00949-1
Mots-clés: résistance aux antimicrobiens, microbiote intestinal porcin, cuivre alimentaire, butyrate et santé intestinale, gènes de résistance mobiles