Clear Sky Science · zh
Dravet 综合征小鼠模型中体温-睡眠耦合机制被破坏
体温与睡眠为何在这种疾病中至关重要
患有 Dravet 综合征儿童的父母常常面临两大挥之不去的担忧:危险的癫痫发作和难眠之夜。除了癫痫外,许多患儿还难以维持稳定的体温并获得高质量的睡眠。本研究利用一种 Dravet 综合征小鼠模型揭示了体温与睡眠之间的隐性联系,并指向了一个小而功能强大的脑区,或可解释这些日常困难的根源。
一种罕见癫痫如何影响全身
Dravet 综合征由一项基因缺陷引起,该基因帮助神经元产生电活动。虽然该病以严重且难治的癫痫发作最为人所知,但患者常同时出现心率、呼吸、体温调节和睡眠方面的问题。研究者使用携带相同致病突变的小鼠,建立了反映患者许多特征的模型。他们的目标并非研究癫痫发作本身,而是弄清这些小鼠为何像患儿一样,在保暖和高质量睡眠两方面都存在困难。
体温偏低与睡眠准备不足
当团队测量幼鼠的体温时,发现 Dravet 小鼠比其健康同窝鼠体温更低。两组小鼠都先置于轻微加温的环境,随后再返回常温。尽管两组在加温后升温到相似水平,但 Dravet 小鼠在恢复常温后更易散热,最终体温更低。研究者还在过夜期间提供了筑巢材料,这是一个简单的自然行为检测,用以评估动物为睡眠做准备并保持温暖的能力。健康小鼠筑起紧密而复杂的巢;大多数 Dravet 小鼠则筑巢差或不筑巢,提示其进行这一基本睡眠准备行为的能力或驱动下降。 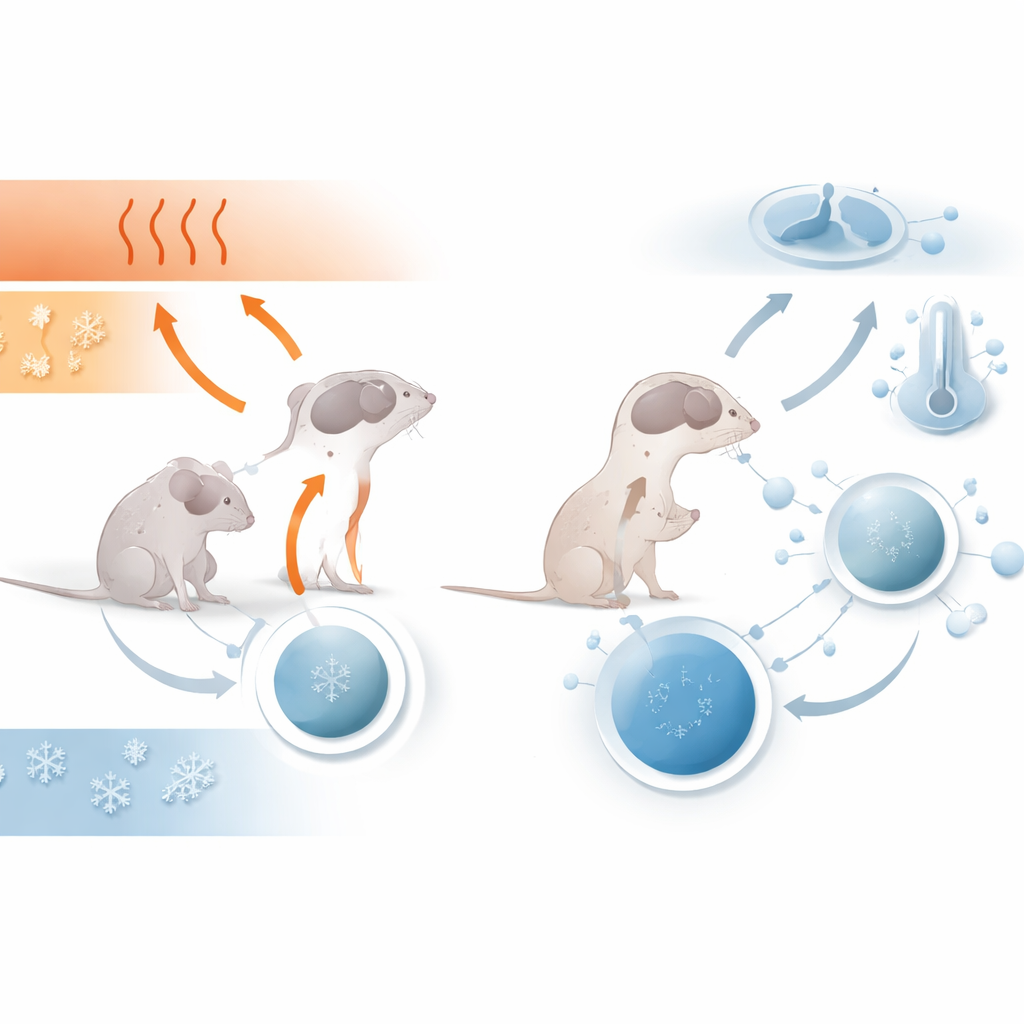
睡眠失去使身体降温的作用
在健康动物中,从清醒过渡到非快速眼动(NREM)睡眠通常伴随核心体温的小幅但重要下降,以及慢节律脑电活动(称为 delta 活动)的上升。研究者利用脑电记录和微型温度探针密切观察这一转变。在典型小鼠中,NREM 起始时会出现明显的 delta 波激增和显著的体温下降。然而在 Dravet 小鼠中,NREM 期间的 delta 活动几乎没有高于清醒水平,体温在相同转变期间则保持基本不变。直接记录前下丘脑(一个已知协调睡眠与体温控制的深部脑区)时也得到相同模式:健康小鼠在入睡时表现出强烈的 delta 变化和降温,而 Dravet 小鼠则没有。
温暖环境能帮助部分小鼠入睡,但对另一部分无效
通常,略微温暖的环境会让动物(包括人类)更容易入睡。为检验这一点,研究团队在记录脑活动的同时轻微升高年长小鼠的周围温度。健康小鼠如预期般反应:在更温暖的环境中,它们在 NREM 睡眠中的时间增加,慢波也变得更强。相比之下,Dravet 小鼠并未表现出温暖带来的助眠效果,尽管更高的温度并未引发额外的癫痫活动。研究者接着探问,增强下丘脑信号是否能修复这一缺陷。他们使用病毒载体,专门在 Dravet 小鼠的前下丘脑中增加有缺陷的钠通道蛋白的产量。经过这一针对性基因递送后,温暖环境再次增加了 NREM 睡眠并增强了 delta 活动,类似于健康动物的反应。
重新开启下丘脑神经元的功能
为了进一步探究该脑区的作用,科学家们采用了一种化学遗传学工具,允许他们用一种设计的药物暂时提高神经元的活动性。他们用携带人工受体的病毒构建感染下丘脑神经元,随后通过注射一种能将这些细胞切换到更活跃状态的化合物来激活它们。在健康小鼠中,无论是否注射该药物,温暖环境均能促进 NREM 睡眠。在 Dravet 小鼠中,然而,仅有温暖仍无法促进睡眠。只有在下丘脑神经元被人工激活时,温暖环境才会增加 NREM 睡眠并强化慢波活动。这表明仅仅提高这些神经元的兴奋性就足以恢复缺失的体温诱导睡眠反应。
对家庭与未来治疗的意义
综上所述,本研究揭示在 Dravet 综合征中,正常的体温下降与入睡之间的联动被破坏,而这种破坏与特定下丘脑枢纽活动的改变密切相关。Dravet 小鼠在基线时体温偏低,入睡时不出现通常的体温下降,在温暖环境中也不会变得更困——除非下丘脑神经元得到帮助以恢复正常放电。尽管这些实验是在小鼠中完成的,但结果表明,未来若能针对该脑区及其体温—睡眠回路进行干预,或能在癫痫发作之外帮助缓解患者和照护者所承受的睡眠与热调问题,从而提供额外的改善方向。 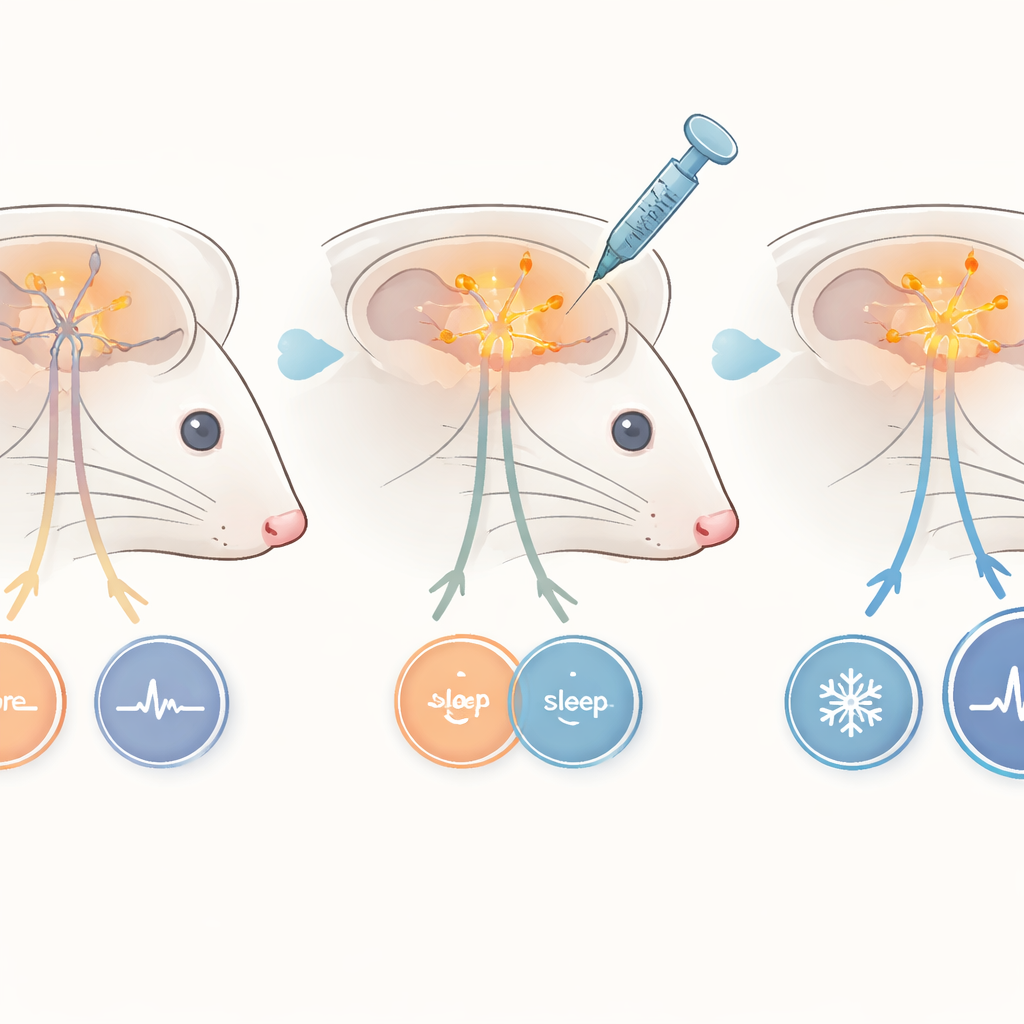
引用: Fadila, S., Krivoshein, G., Majadly, H. et al. Disrupted temperature-sleep coupling mechanism in a Dravet syndrome mouse model. Nat Commun 17, 3232 (2026). https://doi.org/10.1038/s41467-026-69957-1
关键词: Dravet 综合征, 睡眠, 体温调节, 下丘脑, 小鼠模型