Clear Sky Science · zh
肠道 CX3CR1+ 巨噬细胞稳态的维持决定了 SIV 感染猕猴停药后病毒受控的状况
为什么肠道在类 HIV 感染中很重要
长期以来,HIV 治愈研究主要关注血液和淋巴结中的潜在病毒储库。但肠道是感染中最早且受损最严重的组织之一,那里发生的损伤可能使免疫系统多年维持在低度慢性炎症状态。这项在感染了类 HIV 病毒(SIV)的猴子中进行的研究显示,一类特定的肠道免疫细胞——巨噬细胞——可能决定停药后病毒是再次反弹,还是长期在无药状态下受控。
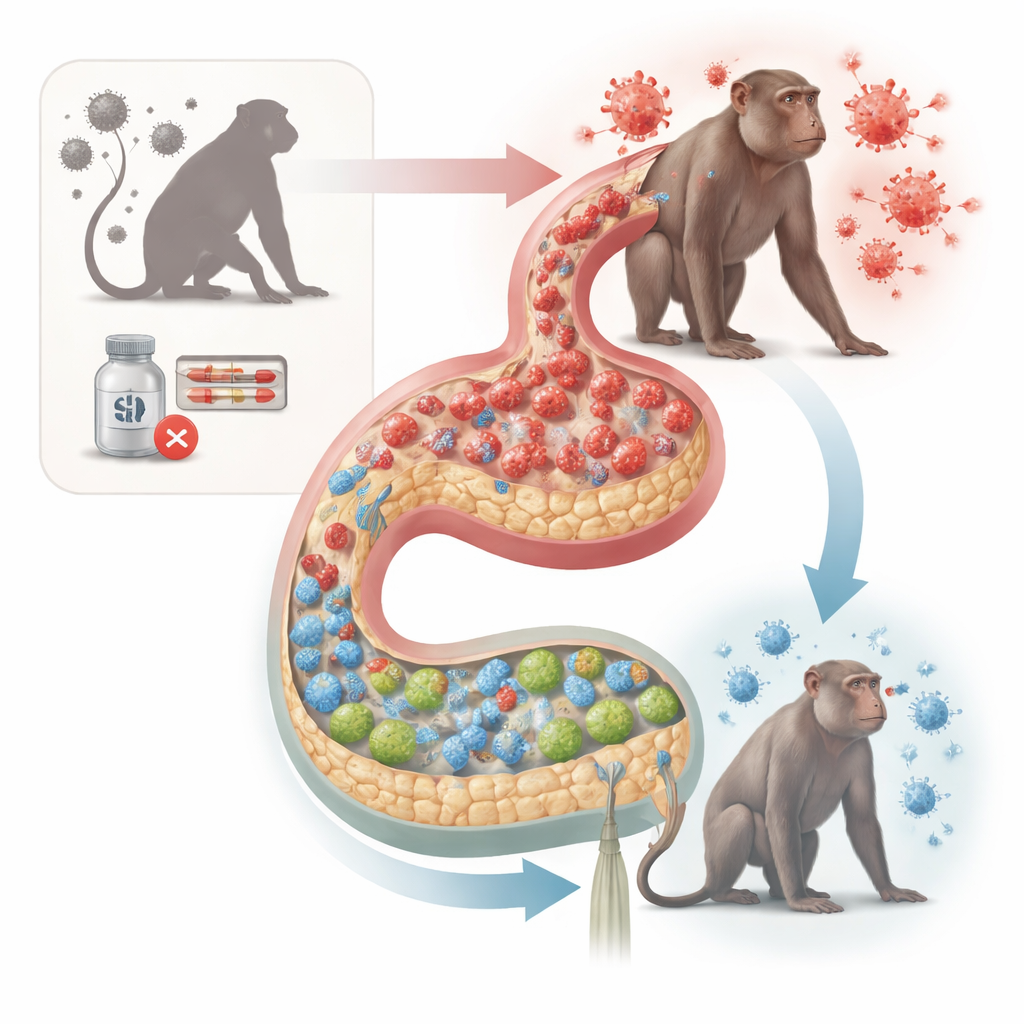
停药后的不同结局
研究人员随访了37只雄性猕猴(长尾猕猴)感染 SIV 的个体。有些动物从未接受抗逆转录病毒治疗(ART),而另一些则在感染后早期或晚期开始 ART,随后在密切监测下停止用药。停药后,一部分猴子将病毒维持在极低水平——这些被称为“停药后控制者”。另一些则出现强烈的病毒反弹,被称为非控制者。尽管所有接受过治疗的动物在开始 ART 前接触到的病毒量相似,只有成为控制者的动物能完全恢复血液中的 CD4 T 细胞,并且其在血液、淋巴结和肠组织中的病毒储库明显更小。
肠壁中的守护细胞
为弄清为何部分动物能控制病毒,研究团队将视角聚焦到肠粘膜——这是 HIV 和 SIV 的主要战场之一。他们关注巨噬细胞,这类免疫细胞在组织中巡逻、清除微生物并参与损伤修复。这些细胞有不同的表型。在健康动物中,大多数肠道巨噬细胞表现出高表达的表面分子 CX3CR1,这是成熟、镇静型细胞的标志,支持组织修复与免疫平衡。然而慢性 SIV 感染改变了这一平衡:肠道被 CX3CR1 低表达的促炎巨噬细胞所主导,而具有保护作用的 CX3CR1 高表达细胞则减少。这种倾斜的细胞谱系在感染早期就出现,并在未治疗的动物中持续存在。
平衡的巨噬细胞带来更平静的免疫状态
停药后控制者打破了这一模式。即便在停止 ART 后,他们的肠道大多维持或恢复了 CX3CR1 高表达的巨噬细胞群,并限制了 CX3CR1 低表达细胞的积累,呈现出更接近未感染猴子的细胞谱系。个体中 CX3CR1 高表达巨噬细胞越多,病毒载量越低,病毒 DNA 储库越小。这些“守护”细胞与调节性 CD4 T 细胞的存在密切相关——调节性 T 细胞能抑制过度的免疫反应——并与有助于保护肠道屏障的更健康的辅助性 T 细胞组合相联系。相比之下,CX3CR1 低表达的巨噬细胞与更高的 T 细胞活化、衰竭迹象以及更倾向促炎的辅助性 T 细胞谱系相关联。
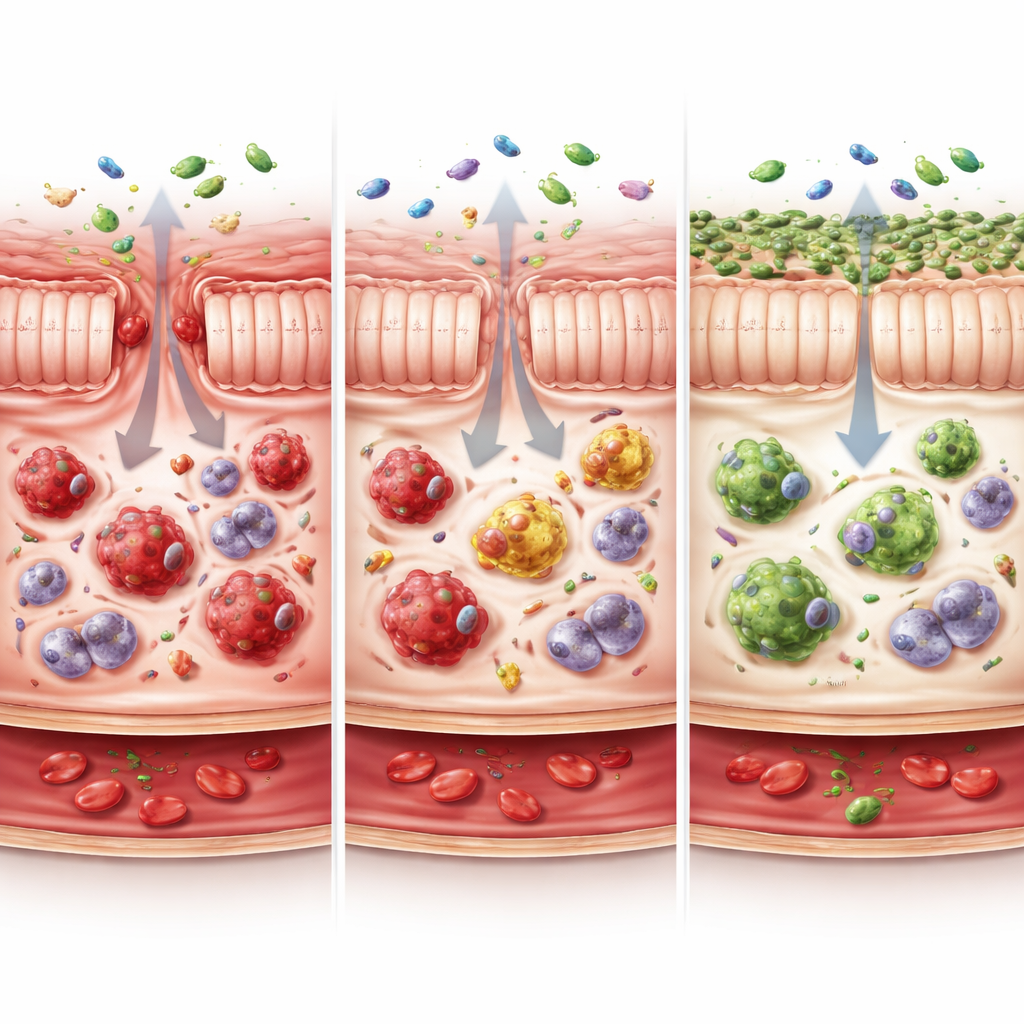
超出肠道的炎症波及
巨噬细胞失衡的连锁效应超出了肠道范围。那些拥有大量 CX3CR1 低表达巨噬细胞的动物表现出高度活化的中性粒细胞——另一类在过度激活时会损伤组织的白细胞——并且血液中炎性分子水平升高。它们的引流淋巴结也显示出活化的巨噬细胞池扩大,而 CD4 T 细胞则被消耗并处于过度工作状态。相比之下,控制者的中性粒细胞活化程度较低,淋巴结中的巨噬细胞更为静止,血液中若干炎性细胞因子的水平明显更低,这些都表明全身范围内的免疫压力降低。
这对未来 HIV 治愈意味着什么
总体而言,研究提示在肠道中维持稳定的 CX3CR1 高表达巨噬细胞群是那些在停药后能控制 SIV 的动物的一个显著特征。这些细胞并非仅仅反映低病毒水平,它们似乎有助于维持肠道屏障、支持调节性 T 细胞,并防止会促进病毒持久性的失控炎症。对普通读者而言,关键结论是:实现 HIV 的“功能性治愈”或许不仅需要直接攻击病毒,还需要培育肠道中恰当类型的守护细胞。这些细胞可作为识别有望实现停药后控制的个体的生物标志物,并可作为旨在恢复平静、有序免疫环境的疗法目标。
引用: Hua, S., Benmeziane, K., Desjardins, D. et al. Maintenance of intestinal CX3CR1+ macrophage homeostasis defines post-treatment control in SIV-infected macaques. Nat Commun 17, 3111 (2026). https://doi.org/10.1038/s41467-026-69848-5
关键词: HIV 治愈, 肠道免疫, 巨噬细胞, SIV 猕猴模型, 免疫炎症