Clear Sky Science · es
Mantenimiento de la homeostasis de macrófagos CX3CR1+ intestinales define el control postratamiento en macacos infectados por SIV
Por qué el intestino importa en infecciones similares al VIH
La búsqueda de una cura para el VIH se ha centrado durante mucho tiempo en los reservorios virales ocultos en sangre y ganglios linfáticos. Pero el intestino es uno de los tejidos más afectados desde el inicio de la infección, y el daño allí puede mantener al sistema inmune en un estado de inflamación simmerante durante años. Este estudio, realizado en monos infectados con un virus similar al VIH (SIV), muestra que un grupo concreto de células inmunitarias intestinales llamadas macrófagos puede marcar la diferencia entre la reaparición del virus tras la interrupción del tratamiento y el control duradero del virus sin fármacos.
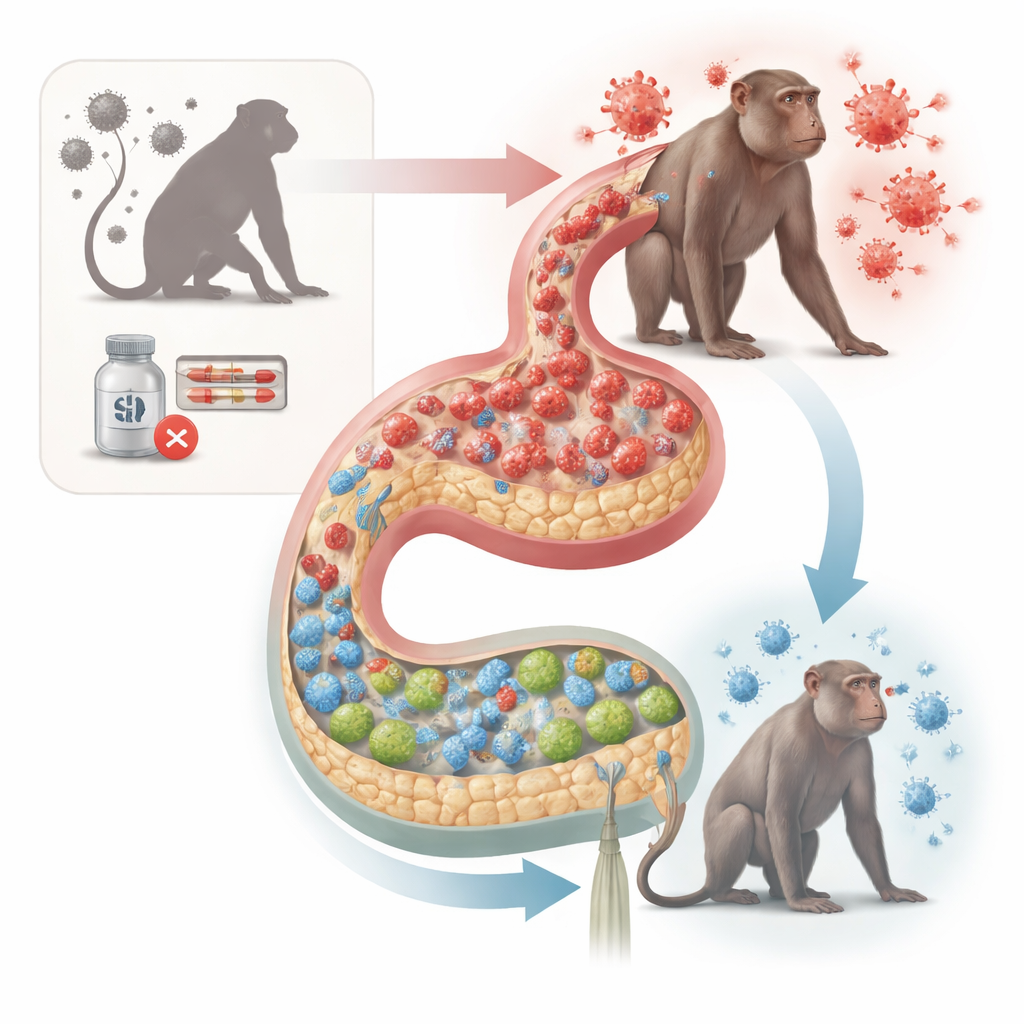
Caminos distintos tras interrumpir el tratamiento
Los investigadores siguieron a 37 macacos cínomolos machos infectados con SIV. Algunos animales nunca recibieron terapia antirretroviral (TAR), mientras que otros iniciaron TAR de forma temprana o tardía tras la infección y luego la interrumpieron bajo seguimiento estricto. Tras la interrupción del tratamiento, un subconjunto de monos mantuvo el virus a niveles muy bajos: estos fueron los “controladores postratamiento”. Otros, denominados no controladores, experimentaron una fuerte reactivación viral. Aunque todos los animales tratados habían recibido cantidades similares de exposición viral antes de la TAR, solo aquellos que se convirtieron en controladores recuperaron plenamente las células CD4 sanguíneas y tuvieron reservorios virales mucho más pequeños en sangre, ganglios linfáticos y tejido intestinal.
Células guardianas en la pared intestinal
Para entender por qué algunos animales controlaban el virus, el equipo se centró en el revestimiento intestinal, un importante campo de batalla en el VIH y el SIV. Pusieron el foco en los macrófagos, células inmunitarias que patrullan tejidos, eliminan microbios y ayudan a reparar daños. Estas células existen en distintas variantes. En animales sanos, la mayoría de los macrófagos intestinales mostraban niveles altos de una molécula de superficie llamada CX3CR1, firma de células maduras y calmantes que favorecen la reparación tisular y el equilibrio inmune. La infección crónica por SIV, sin embargo, desplazó ese equilibrio: el intestino llegó a estar dominado por macrófagos con baja expresión de CX3CR1 asociados a inflamación, mientras que las células protectoras CX3CR1-altas disminuyeron. Este perfil sesgado apareció poco después de la infección y persistió en animales no tratados.
Macrófagos equilibrados, inmunidad más serena
Los controladores postratamiento rompieron ese patrón. Incluso tras interrumpir la TAR, sus intestinos conservaron o restauraron en gran medida la población de macrófagos CX3CR1-altos y limitaron la acumulación de células CX3CR1-bajas, generando un perfil mucho más cercano al de monos no infectados. Cuantos más macrófagos CX3CR1-altos tenía un animal, menor era su carga viral y más pequeño su reservorio de ADN viral. Estas células “guardianas” se relacionaron estrechamente con la presencia de células T CD4 reguladoras—células inmunes que atenúan respuestas excesivas—y con una mezcla más saludable de células T helper que protegen la barrera intestinal. En contraste, los macrófagos CX3CR1-bajos se asociaron con una mayor activación de células T, signos de agotamiento y un cambio hacia subtipos de células T helper más inflamatorios.
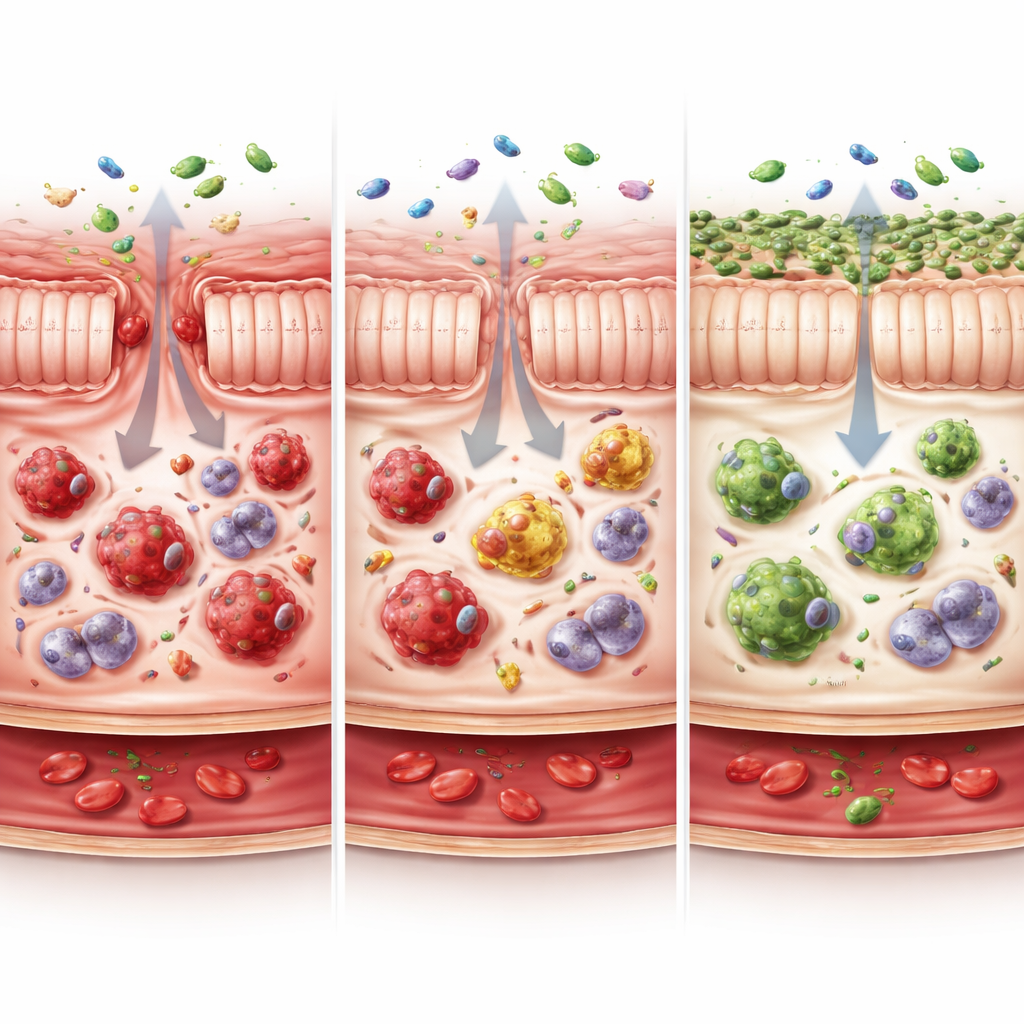
Inflamación que se extiende más allá del intestino
Los efectos en cascada del desequilibrio de macrófagos se observaron más allá del intestino. Los animales con abundantes macrófagos CX3CR1-bajos presentaban neutrófilos altamente activados—otro tipo de glóbulo blanco que puede dañar tejidos cuando se sobreestimula—y niveles elevados de moléculas inflamatorias en sangre. Sus ganglios linfáticos de drenaje también mostraron pools ampliados de macrófagos activados y células CD4 agotadas y sobrecargadas. En los controladores, por el contrario, los neutrófilos estaban menos activados, los macrófagos de los ganglios parecían más quiescentes y los niveles sanguíneos de varias citocinas inflamatorias eran mucho más bajos, todo lo cual apunta a un estado corporal de menor estrés inmune.
Qué significa esto para futuras curas del VIH
En conjunto, el estudio sugiere que mantener una población estable de macrófagos CX3CR1-altos en el intestino es una característica distintiva de los animales que pueden mantener el SIV controlado tras la interrupción de la TAR. Más que simplemente reflejar bajos niveles virales, estas células parecen ayudar a preservar la barrera intestinal, apoyar a las células T reguladoras y evitar una inflamación descontrolada que, de otro modo, alimentaría la persistencia viral. Para el lector no especializado, el mensaje clave es que una “cura funcional” eficaz para el VIH puede depender no solo de atacar el virus directamente, sino también de fomentar los tipos adecuados de células guardianas en el intestino. Estas células podrían servir como biomarcadores para identificar a individuos con buena probabilidad de control postratamiento y como dianas para terapias destinadas a restaurar un entorno inmune calmado y bien regulado.
Cita: Hua, S., Benmeziane, K., Desjardins, D. et al. Maintenance of intestinal CX3CR1+ macrophage homeostasis defines post-treatment control in SIV-infected macaques. Nat Commun 17, 3111 (2026). https://doi.org/10.1038/s41467-026-69848-5
Palabras clave: Curación del VIH, inmunidad intestinal, macrófagos, modelo de macaco con SIV, inflamación inmune