Clear Sky Science · zh
用于深层组织超分辨成像的多光子结构化照明显像中的双重去卷积
在活组织中看得更深
现代生物学常常依赖于在厚组织切片(例如脑片或发育中的胚胎)中观察极微小的细节。不幸的是,当光在这些拥挤的环境中传播时,会被折射和扰乱,使图像在科学家最希望获得清晰视野时变得模糊。本文介绍了一种数字“去抹除”这些图像的方法,使一种标准的先进显微镜能够在不增加昂贵复杂硬件的情况下,揭示组织深处的极细结构。
为什么深层成像如此困难
荧光显微镜让研究者标记特定分子并观察细胞和组织的结构与动态。过去几十年里,若干“超分辨”方法突破了传统分辨率极限,揭示了远小于200纳米的细节。然而,这些方法大多只在样品表面附近效果良好。在厚组织(如小鼠大脑)中,用于激发荧光的入射光以及返回探测器的发射光都会被组织结构的微小不均匀性扭曲。这些称为像差的扭曲会使显微镜的焦点模糊并抹去高细节信息,尤其是在几十微米以外的深度处。
从硬件修正到软件方案
对抗像差的常用方法是基于硬件的自适应光学,它使用可动镜面或其他器件来重塑光波前以恢复清晰焦点。尽管强大,这些系统价格昂贵、技术要求高,且往往一次只校正一种波长或一种传播方向的畸变。作者提出了一种计算方法,适用于许多实验室已经常见的一类显微镜:激光扫描多光子显微镜。通过用相机替换通常的单一光电探测器,他们记录到一组丰富的扫描图像,这些图像编码了入射激发光和出射荧光在组织中如何被扰动的信息。
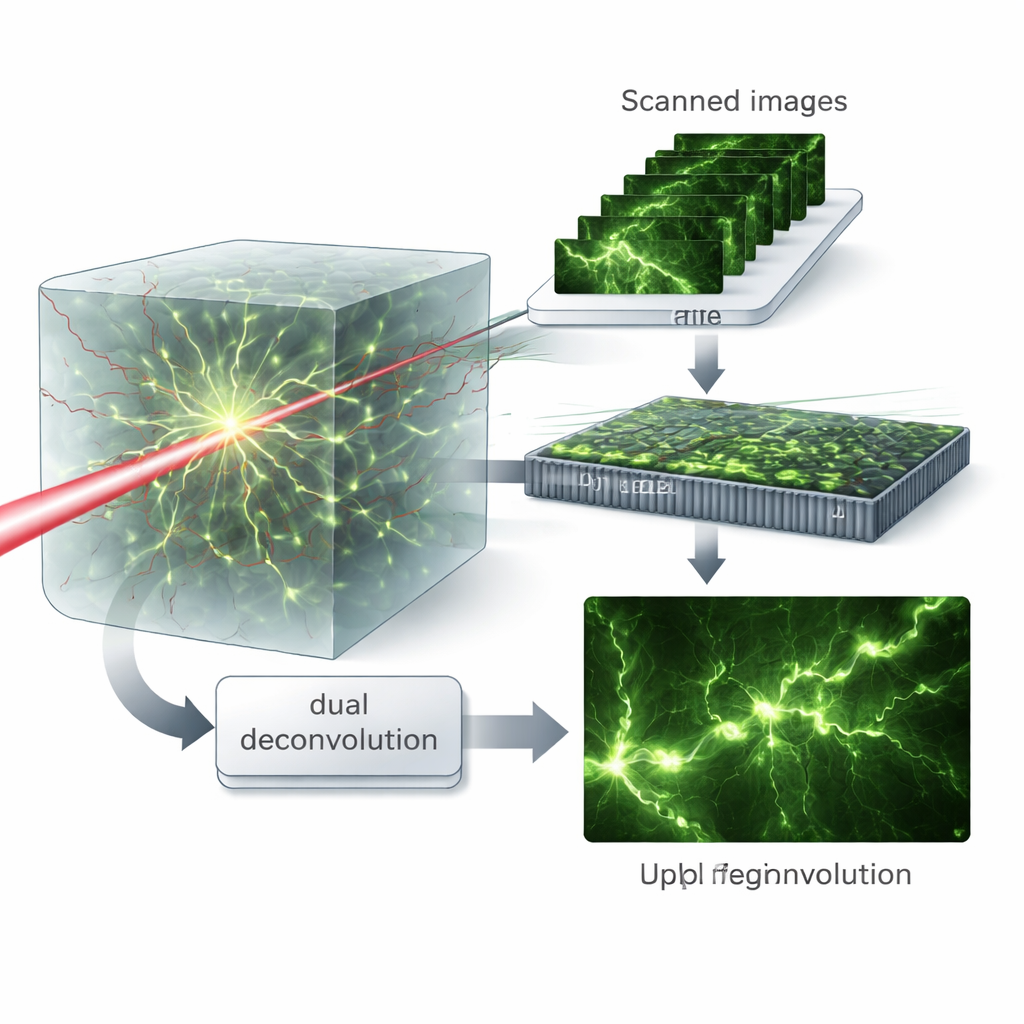
虚拟图样与双重去卷积
关键思想是将这些扫描图像视为如果样品被许多不同的细光斑图样照明时所得到的数据,作者称之为虚拟结构化照明。在频域上对这些数据进行数学重组可以将激发与发射过程的作用分离开来。随后他们引入了一种“双重去卷积”算法,交替估计并校正来自入射光和出射光各自的模糊,而不是将它们合并为单一的有效模糊。这种基于矩阵的处理保留了更多的高频细节,使算法即便在像差强烈时也能恢复出细小结构。
在仿真与真实样品中得到更清晰的视图
为了验证他们的方法,团队首先使用双光子显微镜的计算机模拟——这是一种使用两颗低能光子在焦点处才激发荧光的深层成像技术。在严重模拟畸变下,传统双光子和标准结构化照明重建出的图像明显模糊。相比之下,双重去卷积恢复出清晰的图样,其分辨率接近荧光波长的四分之一——约130纳米,符合理论预期。随后作者搭建了带科学相机的定制双光子系统,并将其算法应用于真实样品,包括荧光微球、藏在散射层后的测试图样、培养细胞、小鼠脑组织以及完整固定的斑马鱼。一次又一次,那些在传统图像中看似被抹平或重影的结构在处理后显现为清晰分离的特征,诸如树突棘等精细神经结构在小鼠大脑中在深度高达180微米处仍可分辨。
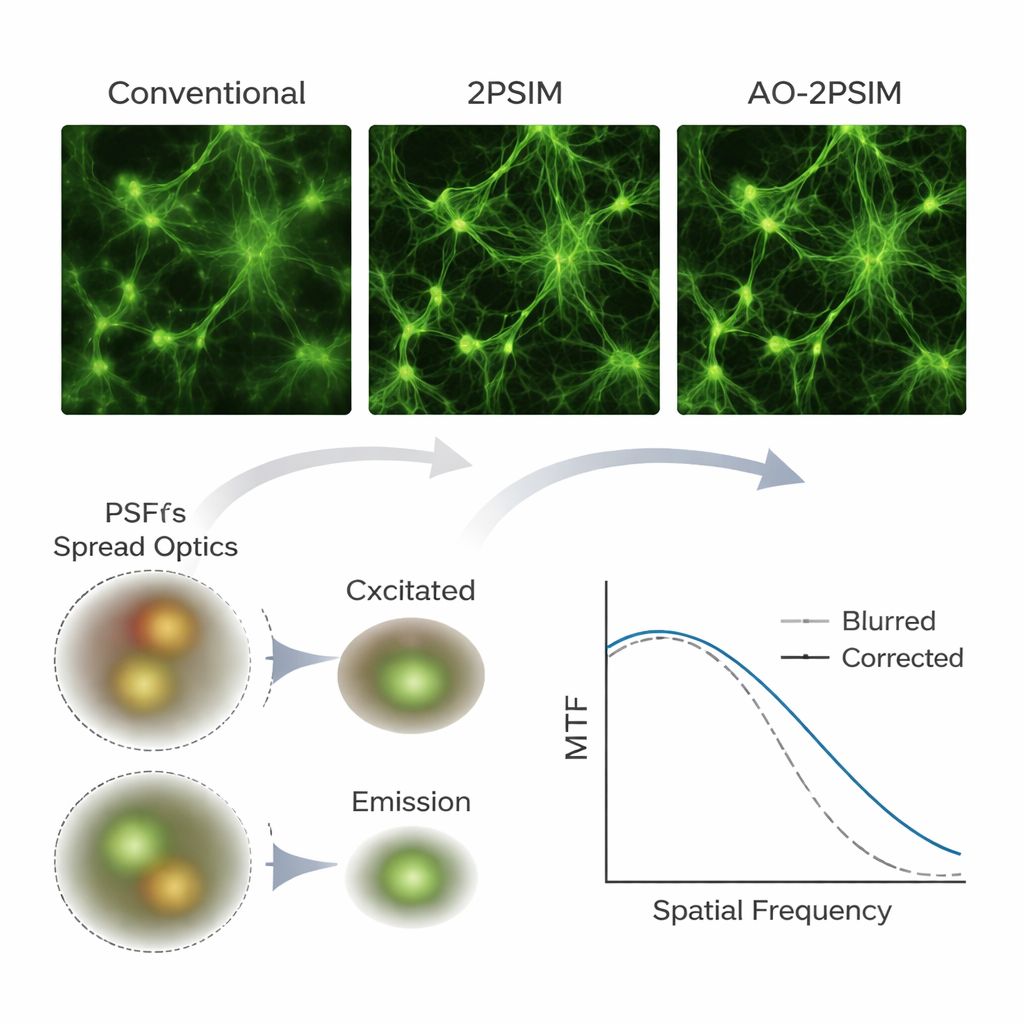
这对生物成像意味着什么
对非专业读者而言,主要信息是作者展示了如何仅通过软件以及一次相机升级,把现有的多光子显微镜转变为更强大的深层组织成像工具。通过精确建模并校正组织在入射和出射两侧对光的弯曲,他们的双重去卷积方法在挑战性厚样品中将通常的分辨界限提高了一倍,而无需依赖复杂的自适应镜面。尽管该方法仍依赖于收集足够信号并且当前需要相对较慢的扫描,但它为常规化、超清晰的三维脑组织及其他器官成像提供了一条实用且具有成本效益的路径,开启了更细致研究生物结构如何组织和随时间变化的可能性。
引用: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
关键词: 超分辨显微镜, 双光子成像, 自适应光学, 深层组织成像, 计算成像