Clear Sky Science · zh
一把铁:铁蛋白作为脑癌的脆弱点
为什么大脑中的铁很重要
铁对大脑健康功能至关重要,帮助神经细胞产生能量并进行信息交流。但过多的游离铁就像干草堆中的火星,会助长有害的化学反应。本文解释了包括胶质母细胞瘤和髓母细胞瘤在内的脑癌如何变得依赖铁,并利用一种名为铁蛋白的蛋白质作为某种安全金库。通过理解这种对铁的“成瘾”及铁蛋白的作用,研究者希望发现削弱那些对现有治疗耐受的顽固肿瘤细胞的新方法。
脑肿瘤的铁饥渴
脑肿瘤细胞,尤其是一小群但极具威力的癌症干细胞,所需的铁远多于正常脑细胞。它们从血液中获取铁、紧紧攫取并把大量铁储存起来。这些铁帮助它们生长、分裂并在低氧或暴露于药物和放疗等压力条件下存活。然而,铁是一把双刃剑。当它与某些氧代谢副产物反应时,会产生高度活泼的分子,撕裂细胞膜并触发一种由脂质氧化驱动的特殊细胞死亡,称为铁死亡。肿瘤细胞极力避免这一命运,通过严格控制游离铁的数量和被封存的铁量来自我保护。
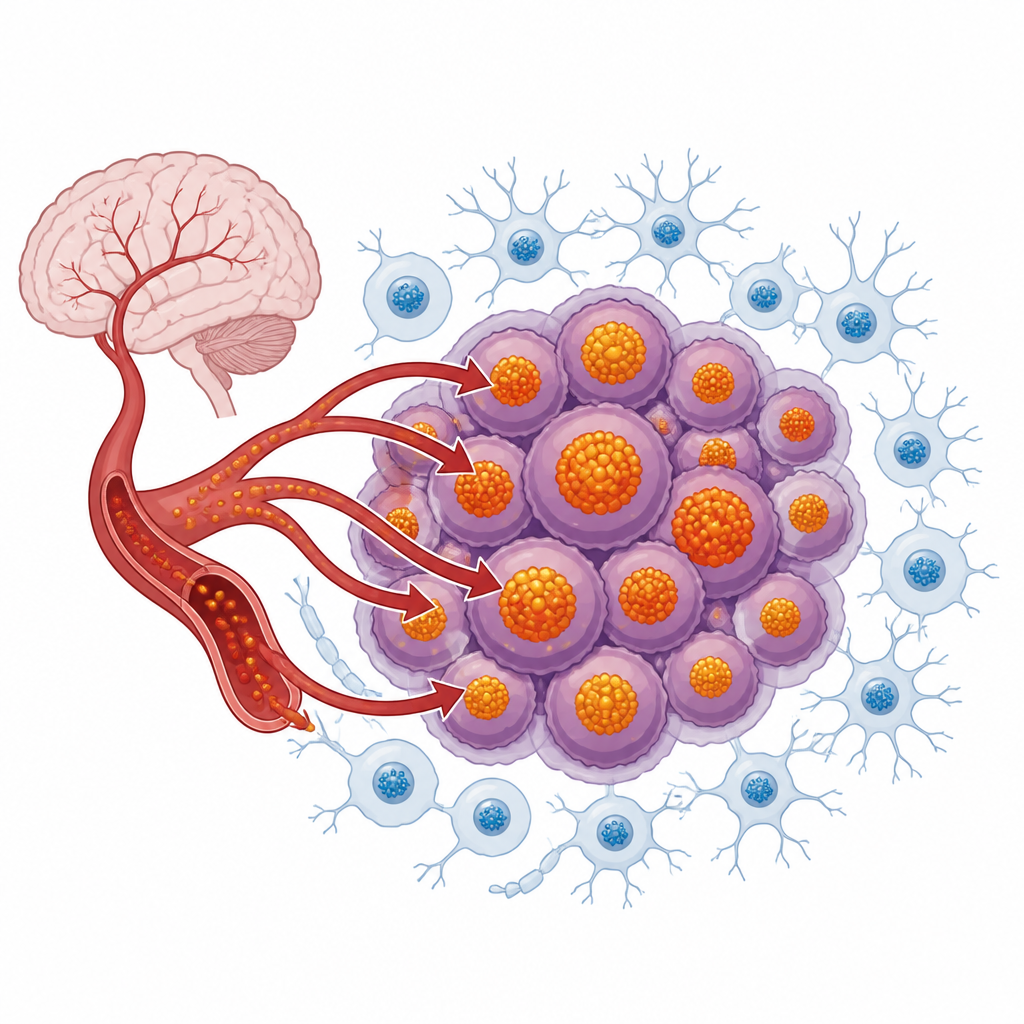
铁蛋白:铁的金库
铁蛋白是一种空心球状蛋白,作为细胞内铁的主要储存金库。每个铁蛋白颗粒可以以非反应性形式安全地容纳数千个铁原子,防止有害化学反应。在大脑中,铁蛋白对正常发育、记忆以及抵御退行性改变很重要。脑肿瘤利用了这一正常的保护系统并将其推向极端。许多胶质母细胞瘤和髓母细胞瘤表现出高水平的铁蛋白,而且这些水平常随肿瘤分级升高并与更差的预后相关。肿瘤中的癌症干细胞似乎尤其依赖铁蛋白来缓冲其大量的铁储备,并保护自己免受铁驱动的损伤。
铁、干细胞与治疗耐受
人们认为癌症干细胞驱动复发,因为它们能够自我更新、适应并在杀死大多数其他肿瘤细胞的疗法中存活。综述表明,这些细胞在多个环节重塑铁的处理:它们增加铁的摄入、减少外排,并通过铁蛋白增强储存。这些额外的铁不仅仅滋养生长,还支持染色质包装和基因活动的改变,从而强化干样性状和对治疗的耐受。在某些肿瘤类型中,扰动铁蛋白可能会推动细胞走向更具侵袭性的行为,这凸显了情境的重要性。然而在脑癌中,证据表明,移除铁蛋白的缓冲能力会使饥渴于铁的干细胞暴露于它们无法再抑制的毒性反应之下。
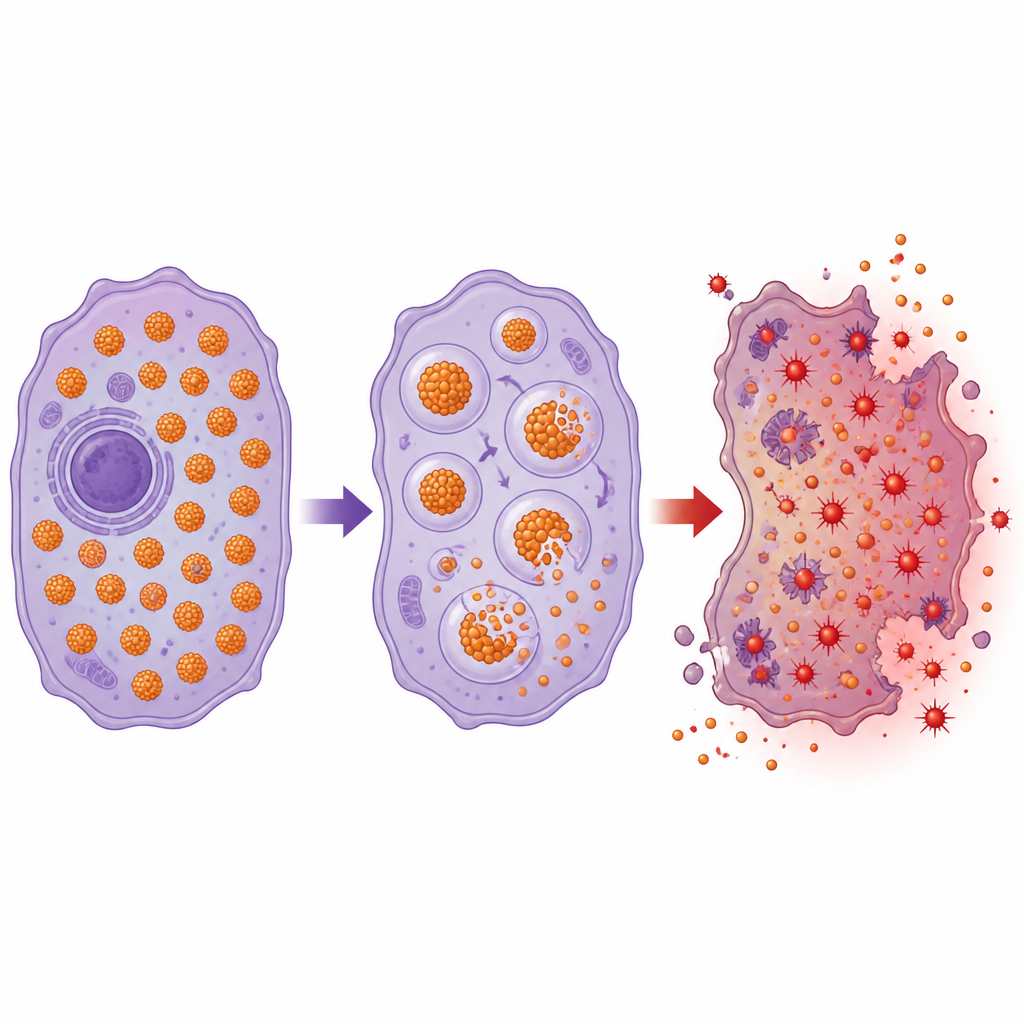
将铁从帮手变为危险因子
由于脑癌高度依赖铁,研究人员正在探索通过针对铁蛋白把铁从帮手变为危险因子的办法。一种新兴策略是铁蛋白自噬(ferritinophagy),即有意分解铁蛋白,突然释放其储存的铁。这股可及铁的激增可以驱动破坏细胞膜的反应并促使细胞走向依赖铁的死亡。实验化合物以及高剂量维生素C在细胞和动物模型中都能触发铁蛋白的分解,并可能使肿瘤对放疗和化疗更敏感——这些疗法会增加有害的氧副产物。挑战在于如何穿越血脑屏障到达脑肿瘤,以及如何在伤害癌细胞的同时不损害健康的神经元和支持细胞。
这对患者意味着什么
文章总结道,铁蛋白位于脑癌的一个关键十字路口:它将铁保持得足够安全以使肿瘤细胞繁荣,但同样的保护体系也可能被转而用于对付肿瘤。通过谨慎破坏铁蛋白在铁成瘾的脑肿瘤中的缓冲作用,医生或许有朝一日能够削弱癌症干细胞、增强现有治疗的效果并降低复发风险。要实现这一点,科学家必须更好地理解铁蛋白在不同脑肿瘤类型中的行为、如何将针对铁蛋白的药物输送入脑内,以及如何避免损伤正常组织。如果能克服这些障碍,针对铁蛋白的疗法可能为治疗侵袭性脑癌提供一件强有力的新工具。
引用: Segui, F., Parks, S.K., Vucetic, M. et al. A fistful of iron: ferritin as a vulnerability point of the brain cancers. Cell Death Dis 17, 451 (2026). https://doi.org/10.1038/s41419-026-08564-w
关键词: 脑癌, 铁蛋白, 铁代谢, 癌症干细胞, 铁死亡