Clear Sky Science · ru
Горсть железа: ферритин как уязвимая точка опухолей мозга
Почему железо в мозге имеет значение
Железо необходимо для нормальной работы мозга: оно помогает нейронам вырабатывать энергию и обмениваться сигналами. Но избыток свободного железа может вести себя как искра в сухой траве, питая вредные химические реакции. В этой статье объясняется, как опухоли мозга, включая глиобластому и медуллобластому, становятся зависимыми от железа и используют белок ферритин как нечто вроде сейфа. Поняв эту «железную зависимость» и роль ферритина, исследователи надеются найти новые способы ослабить упорные опухолевые клетки, устойчивые к нынешним методам лечения.
Голод по железу в опухолях мозга
Клетки опухоли мозга, особенно небольшая, но мощная популяция, известная как раковые стволовые клетки, нуждаются в гораздо большем количестве железа, чем нормальные клетки мозга. Они забирают железо из крови, удерживают его и запасают в больших количествах внутри себя. Это железо помогает им расти, делиться и выживать в стрессовых условиях, таких как низкий уровень кислорода или воздействие лекарств и радиации. Однако железо — это палка о двух концах. Когда оно реагирует с определёнными продуктами окисления кислорода, образуются высокоактивные молекулы, которые могут разрывать клеточные мембраны и инициировать особый тип клеточной гибели, связанный с окислением липидов, называемый ферроптозом. Опухолевые клетки прилагают усилия, чтобы избежать такого исхода, строго контролируя, сколько железа свободно, а сколько заперто.
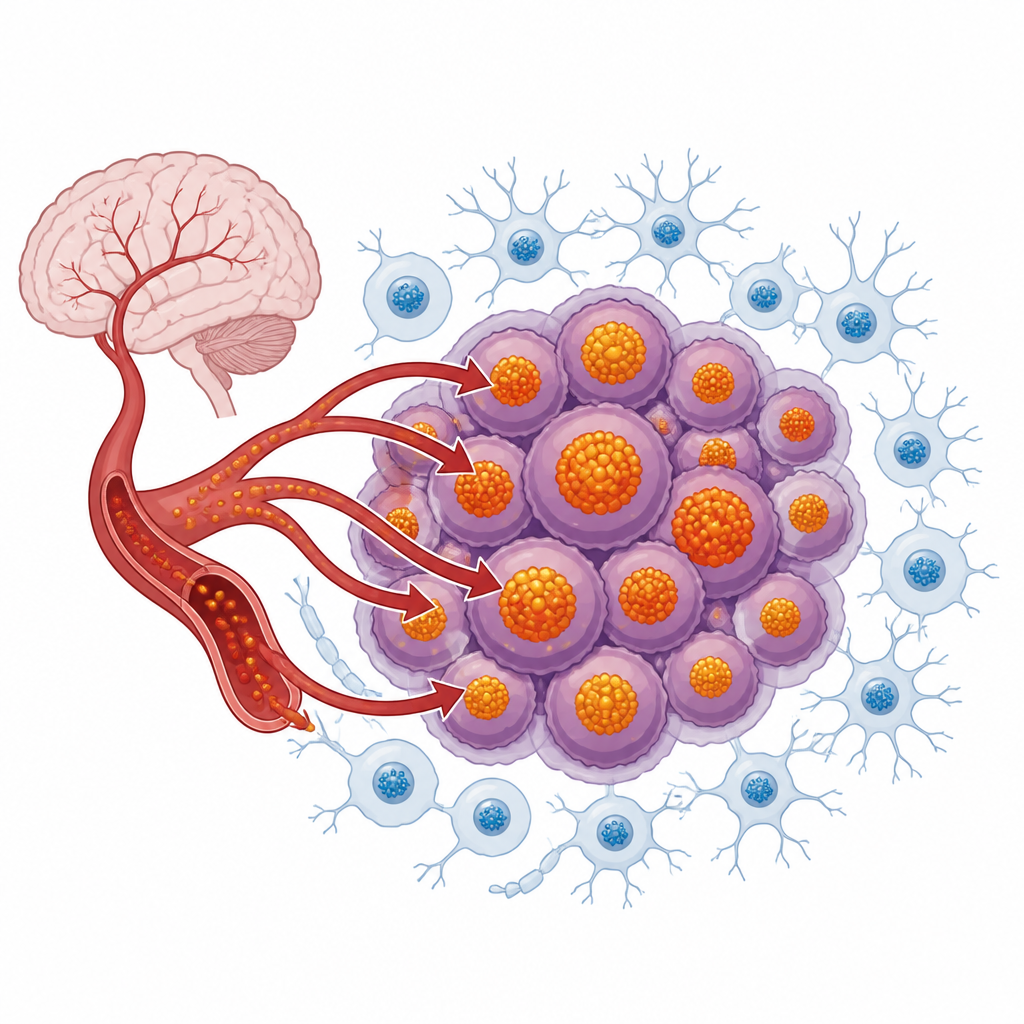
Ферритин как хранилище железа
Ферритин — полый сферический белок, который выступает основным «хранилищем» железа внутри клеток. Каждая частица ферритина может безопасно содержать тысячи атомов железа в неактивной форме, предотвращая вредные химические реакции. В мозге ферритин важен для нормального развития, памяти и защиты от дегенерации. Опухоли мозга используют эту нормальную защитную систему и доводят её до крайности. Во многих глиобластомах и медуллобластомах наблюдаются повышенные уровни ферритина, и эти уровни часто растут с увеличением степени опухоли и ухудшением прогноза. Похоже, что раковые стволовые клетки в этих опухолях особенно сильно зависят от ферритина, чтобы буферизовать свои огромные запасы железа и защищаться от железосодержащего повреждения.
Железо, стволовые клетки и устойчивость к лечению
Считается, что раковые стволовые клетки приводят к рецидиву, потому что они способны к самоподдержанию, адаптации и выживанию при терапиях, убивающих большинство других опухолевых клеток. Обзор показывает, что эти клетки перестраивают обращение с железом на многих уровнях: они усиливают импорт, уменьшают экспорт и увеличивают хранение через ферритин. Это дополнительное железо делает больше, чем просто питает рост. Оно также поддерживает изменения в упаковке ДНК и активности генов, которые укрепляют стволоподобные свойства и устойчивость к терапии. В некоторых типах опухолей нарушение функции ферритина может толкать клетки к более агрессивному поведению, что подчёркивает важность контекста. Однако в опухолях мозга имеющиеся данные свидетельствуют о том, что отмена буферной функции ферритина может оголить железозависимые стволовые клетки перед токсическими реакциями, которые они больше не в состоянии сдерживать.
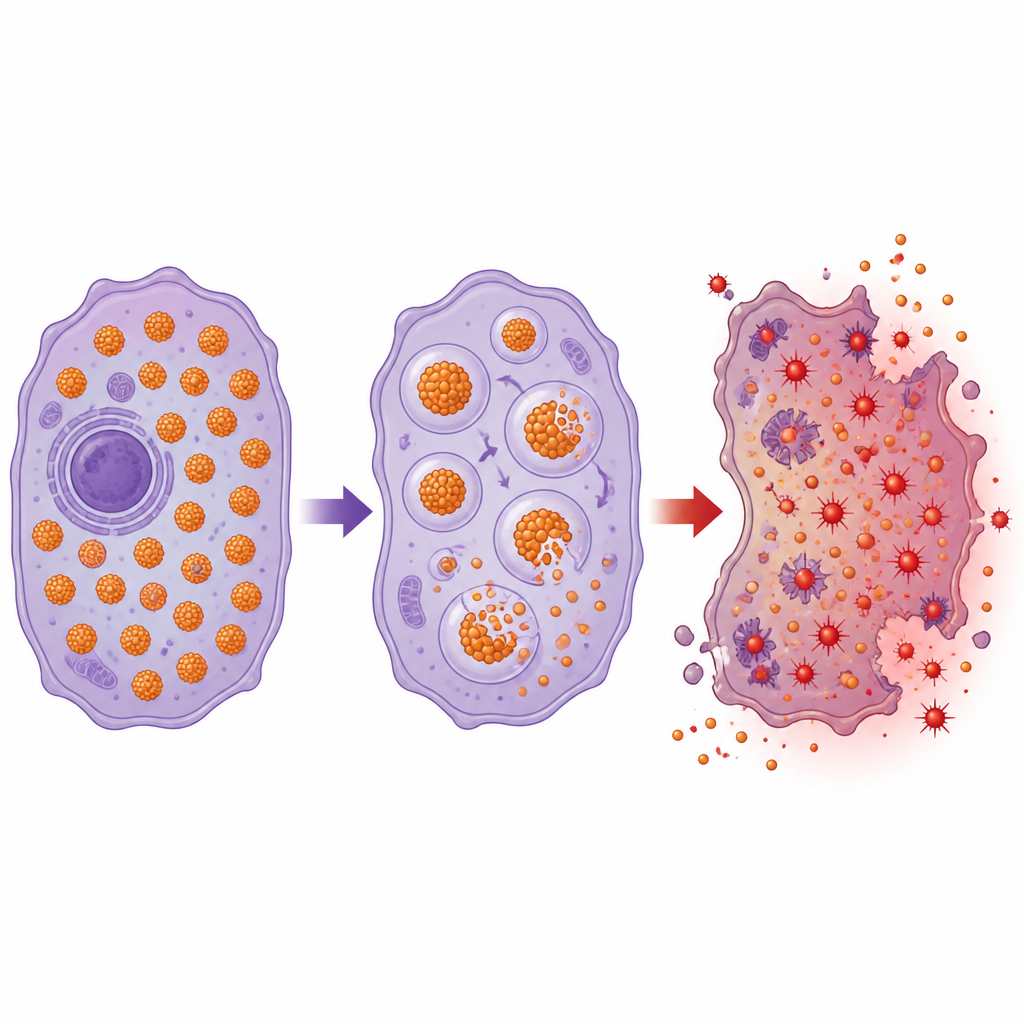
Превращение железа из помощника в угрозу
Поскольку опухоли мозга так зависят от железа, исследователи изучают способы превратить железо из помощника в угрозу, нацеливаясь на ферритин. Одна из новых стратегий — ферритинфагия (ferritinophagy), процесс, при котором ферритин целенаправленно разрушается и внезапно освобождает запасённое железо. Этот всплеск доступного железа может запустить реакции, разрушающие клеточные мембраны, и подтолкнуть клетки к железозависимой смерти. Экспериментальные соединения, а также высокие дозы витамина C могут вызывать распад ферритина в лабораторных моделях и потенциально делают опухоли более чувствительными к радиации и химиотерапии, которые повышают количество вредных продуктов окисления. Основная проблема — доставить средства до опухолей через гематоэнцефалический барьер и повредить раковые клетки, не навредив при этом здоровым нейронам и вспомогательным клеткам.
Что это может значить для пациентов
В статье делается вывод, что ферритин находится в критическом узле в опухолях мозга: он делает железо достаточно безопасным, чтобы опухолевые клетки могли процветать, но та же система безопасности может быть обращена против них. Тщательно нарушив функцию ферритина в «железозависимых» опухолях мозга, врачи когда‑нибудь смогут ослабить раковые стволовые клетки, усилить эффект существующих лечений и снизить риск рецидива. Для этого учёным предстоит лучше понять поведение ферритина в различных типах опухолей мозга, как доставлять препараты, нацеленные на ферритин, в мозг и как избежать повреждения нормальной ткани. Если эти препятствия удастся преодолеть, терапии, нацеленные на ферритин, могут стать мощным новым инструментом в лечении агрессивных опухолей мозга.
Цитирование: Segui, F., Parks, S.K., Vucetic, M. et al. A fistful of iron: ferritin as a vulnerability point of the brain cancers. Cell Death Dis 17, 451 (2026). https://doi.org/10.1038/s41419-026-08564-w
Ключевые слова: рак мозга, ферритин, метаболизм железа, раковые стволовые клетки, ферроптоз