Clear Sky Science · zh
UHRF1 调控 AR 泛素化以促进前列腺癌进展中 AR 信号丧失与恩扎卢胺耐药
这项研究为何重要
前列腺癌常通过阻断男性激素信号的药物来控制,但许多肿瘤最终会绕过这些治疗并以更具威胁性的形式复发。本研究揭示了一个关键的细胞内“开关”,帮助前列腺癌细胞逃避阻断激素的药物,并提示了一种可能延长并增强此类药物疗效的新方法。
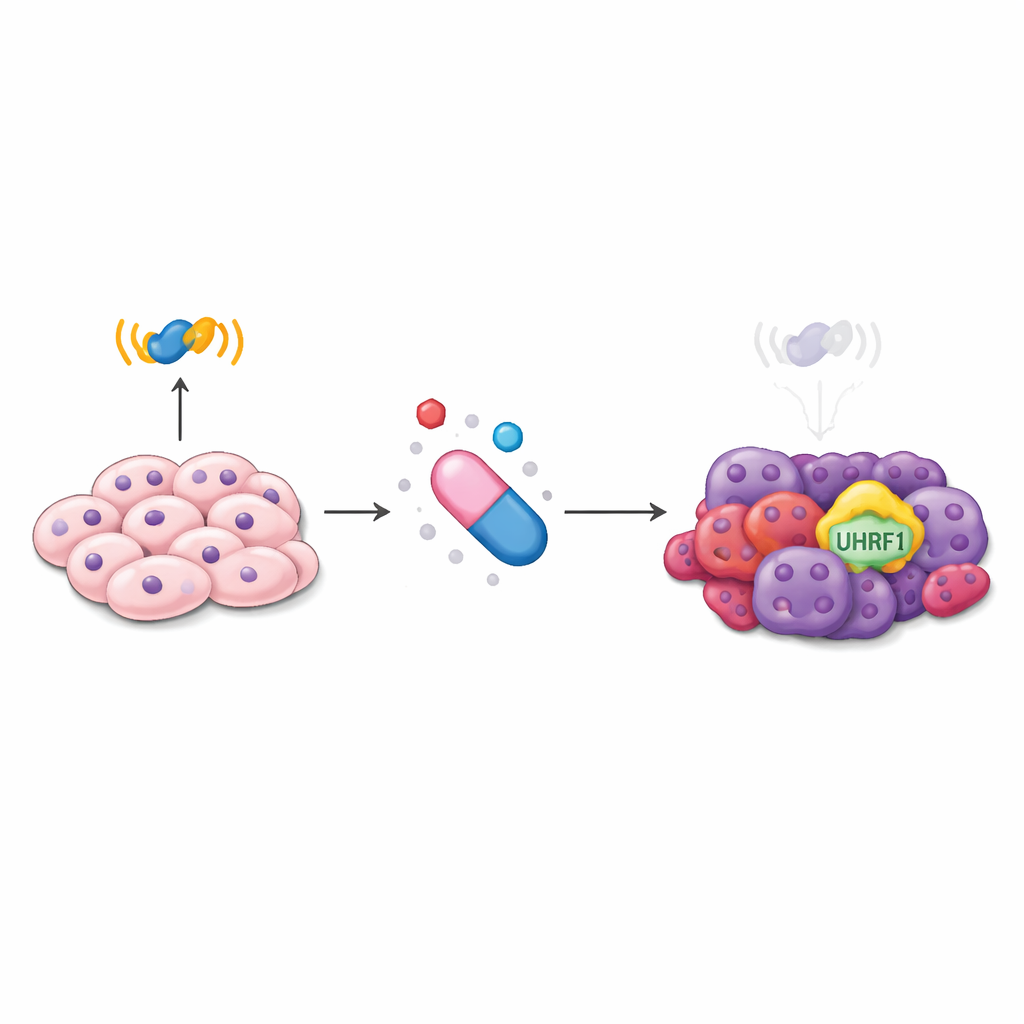
一种失效的药物
现代前列腺癌治疗高度依赖阻断雄激素受体,这是一种细胞内感知男性激素并驱动肿瘤生长的蛋白。像恩扎卢胺这样的药物旨在沉默该信号。然而,随着时间推移,一些肿瘤会逐渐不再依赖这一通路。它们表现出更具可塑性的身份,包括类干细胞和类神经样特征,对阻断激素的疗法变得基本无动于衷。在这一晚期阶段,可用选择有限。研究人员将注意力集中在一个名为 UHRF1 的分子上——它以调控 DNA 包装和读取著称——以探查它是否参与了这种危险的表型转换过程。
耐药的隐蔽帮手
通过分析患者数据和癌细胞系,研究团队发现随着前列腺癌进展和转移,UHRF1 水平上升。UHRF1 更高的肿瘤往往预后更差。在富含侵袭性、类神经的前列腺癌的数据集中,UHRF1 尤其丰富,并与标志神经内分泌和类干状态的基因聚集。在实验室中,被迫获得恩扎卢胺耐药性的细胞显示出明显模式:雄激素受体蛋白明显减少,而 UHRF1 和神经内分泌标志物增加。这表明 UHRF1 可能是允许细胞放弃其依赖激素身份并耐受治疗的机械装置的一部分。
UHRF1 如何破坏激素信号
研究者随后探究了 UHRF1 如何影响雄激素受体本身。他们发现,在耐药细胞中降低 UHRF1 可恢复雄激素受体蛋白并重新激活其下游信号,尽管该基因的 RNA 水平几乎没有变化。这指向了蛋白稳定性而非基因转录的问题。进一步实验显示,UHRF1 能物理结合雄激素受体并在其上附加一连串小蛋白(细胞用作清除信号的泛素)。这一标记将受体送入细胞的蛋白降解机制。当团队禁用 UHRF1 中负责这一标记活性的部分时,雄激素受体不再被有效降解。本质上,UHRF1 充当了一个细胞内的“杀手”,标记荷尔蒙受体以便移除,从而削弱了药物的靶点。
将耐药重新变为易感
因为 UHRF1 有助于抹除激素信号,研究人员测试了阻断 UHRF1 是否能使耐药肿瘤重新对恩扎卢胺敏感。在细胞培养中,下调 UHRF1 减缓了恩扎卢胺耐药细胞的生长,并且重要的是,使它们再次对药物产生响应。UHRF1 缺失与恩扎卢胺治疗的联合抑制细胞增殖的效果远超过任一方法单独使用,主要通过抑制生长而非诱导大量细胞死亡。在携带耐药前列腺癌移植瘤的小鼠中,降低 UHRF1 的肿瘤在恩扎卢胺治疗下显著缩小,而对照肿瘤几乎没有反应。分子分析显示侵袭性、类神经内分泌特征部分逆转,符合向更依赖激素状态回转的变化。
这对患者意味着什么
这项工作描绘了一个清晰图景:在激素阻断治疗的压力下,UHRF1 水平上升通过加速雄激素受体的破坏帮助肿瘤摆脱对该受体的依赖。这推动肿瘤朝更具可塑性、耐药的身份转变。在这一过渡期干预 UHRF1 可以在足够长的时间内维持或恢复激素信号,使恩扎卢胺等药物继续发挥作用。虽然单独抑制 UHRF1 不太可能治愈晚期、完全转分化的疾病,但将该分子作为标准治疗的补充靶点,可能延缓或阻止向不可治疗状态的转变,为患者争取更多时间并更有效地控制疾病。
引用: Zhang, Y., Yu, Z., Li, Y. et al. UHRF1 regulates AR ubiquitination to promote the loss of AR signaling and enzalutamide resistance in progression of prostate cancer. Cell Death Dis 17, 286 (2026). https://doi.org/10.1038/s41419-026-08511-9
关键词: 前列腺癌, 雄激素受体, 药物耐受性, UHRF1, 恩扎卢胺