Clear Sky Science · ar
UHRF1 ينظم يوبيكويتينة مستقبل الأندروجين لتعزيز فقدان إشارة AR ومقاومة الإنزالاتاميد في تقدم سرطان البروستاتا
لماذا يهم هذا البحث
غالباً ما يُتحكم في سرطان البروستاتا بواسطة أدوية توقف إشارات الهرمونات الذكرية، لكن العديد من الأورام في النهاية تتغلب على هذه العلاجات وتعاود الظهور بشكل أكثر خطورة. تكشف هذه الدراسة عن "مفتاح" داخلي رئيسي يساعد خلايا سرطان البروستاتا على الهروب من أدوية حجب الهرمونات، وتقترح طريقة جديدة لجعل هذه الأدوية تعمل لفترة أطول وبفعالية أكبر للمرضى.
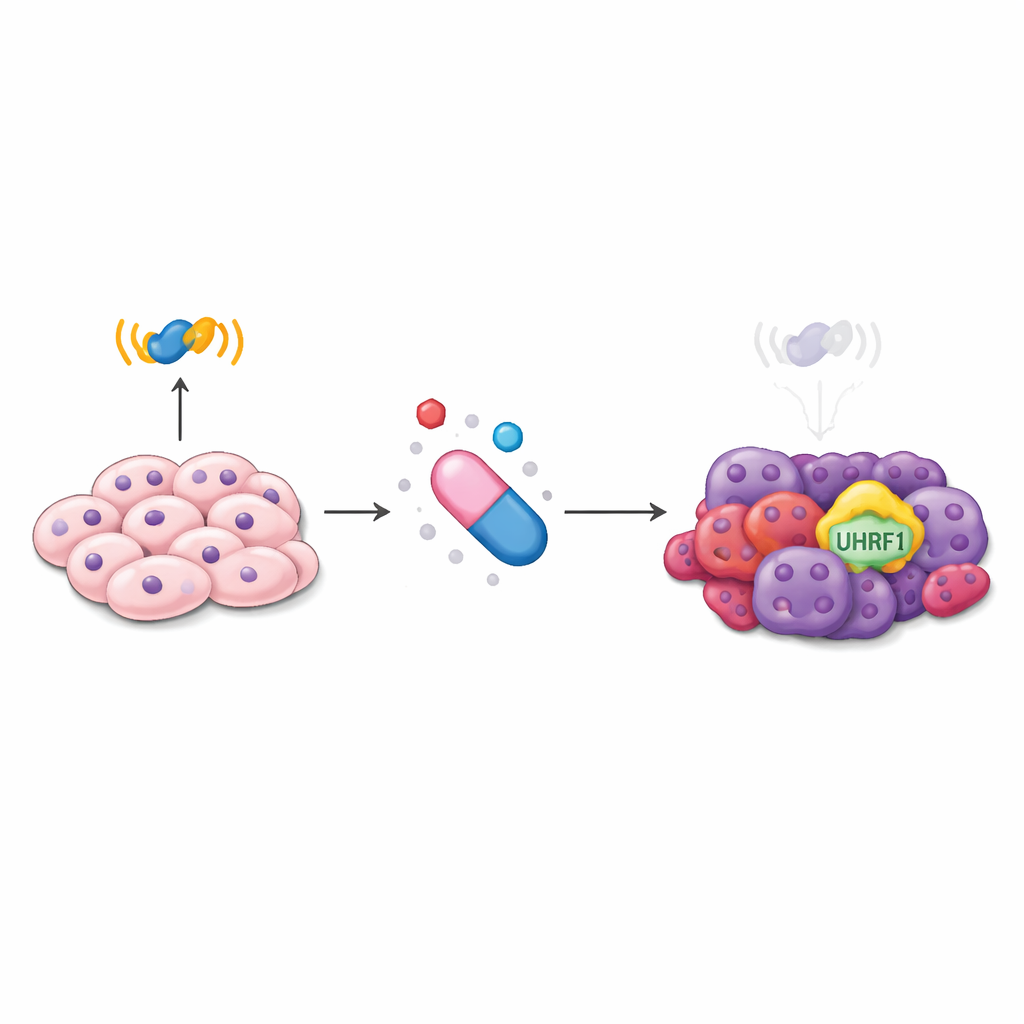
دواء يتوقف عن العمل
يعتمد علاج سرطان البروستاتا الحديث بشكل كبير على حجب مستقبل الأندروجين، وهو بروتين داخل الخلية يستشعر الهرمونات الذكرية ويحفز نمو الورم. تصمم أدوية مثل الإنزالاتاميد لإسكات هذا الإشارة. مع ذلك، مع مرور الوقت، تتحول بعض الأورام بعيداً عن الاعتماد على هذا المسار. تتبنى هويات أكثر مرونة، بما في ذلك صفات شبيهة بالخلايا الجذعية والعصبونية، وتصبح إلى حد كبير غير مبالية بالعلاج بحجب الهرمونات. في هذه المرحلة المتقدمة، تكون الخيارات محدودة. ركز الباحثون على جزيء يسمى UHRF1، المعروف بالتحكم في كيفية تغليف وقراءة الحمض النووي، لمعرفة ما إذا كان يشارك في هذه العملية الخطرة للتغيير الشكلية.
مساعد خفي للمقاومة
من خلال فحص بيانات المرضى وسلاسل خلايا السرطان، وجد الفريق أن مستويات UHRF1 ترتفع مع تقدم وانتشار سرطان البروستاتا. وكانت الأورام التي تحتوي على UHRF1 أعلى ميلاً لأن ترتبط بنتائج أسوأ. في مجموعات بيانات غنية بالأورام العدوانية الشبيهة بالعصب، كان UHRF1 متواجداً بكثرة ومجتمِعاً مع جينات تميّز الحالات العصبية الصماوية وشبيهة الجذعية. في المختبر، أظهرت الخلايا التي أُجبرت على اكتساب مقاومة للإنزالاتاميد نمطاً واضحاً: فقدان كبير في بروتين مستقبل الأندروجين، بينما ازدادت مستويات UHRF1 وعلامات الخلايا العصبية الصماوية. وهذا يوحي بأن UHRF1 قد يكون جزءاً من الآلية التي تمكّن الخلايا من التخلي عن هويتها المعتمدة على الهرمونات وتحمل العلاج.
كيف يكسر UHRF1 إشارة الهرمونات
ثم سأل الباحثون كيف يؤثر UHRF1 على مستقبل الأندروجين نفسه. اكتشفوا أن تقليل UHRF1 في الخلايا المقاومة أعاد بروتين مستقبل الأندروجين وأعاد تنشيط إشاراته اللاحقة، رغم أن مستويات الحمض النووي الريبي الخاصة بالجين لم تتغير تقريباً. أشار ذلك إلى مشكلة في استقرار البروتين بدلاً من نشاط الجين. وكشفت تجارب لاحقة أن UHRF1 يرتبط جسدياً بمستقبل الأندروجين ويعلّمه سلاسل من بروتين صغير تستخدمه الخلايا كإشارة للتخلص. تؤشر هذه الوسمة إلى تدمير المستقبل في آلية تكسير البروتينات بالخلية. عندما عطّل الفريق الجزء من UHRF1 المسؤول عن هذه الفعالية التوسيمية، لم يعد مستقبل الأندروجين يتعرض للتحلل بكفاءة. جوهرياً، يعمل UHRF1 كـ"قاتل داخلي"، وسمّ مستقبل الهرمون لإزالته وبالتالي إضعاف هدف الدواء.
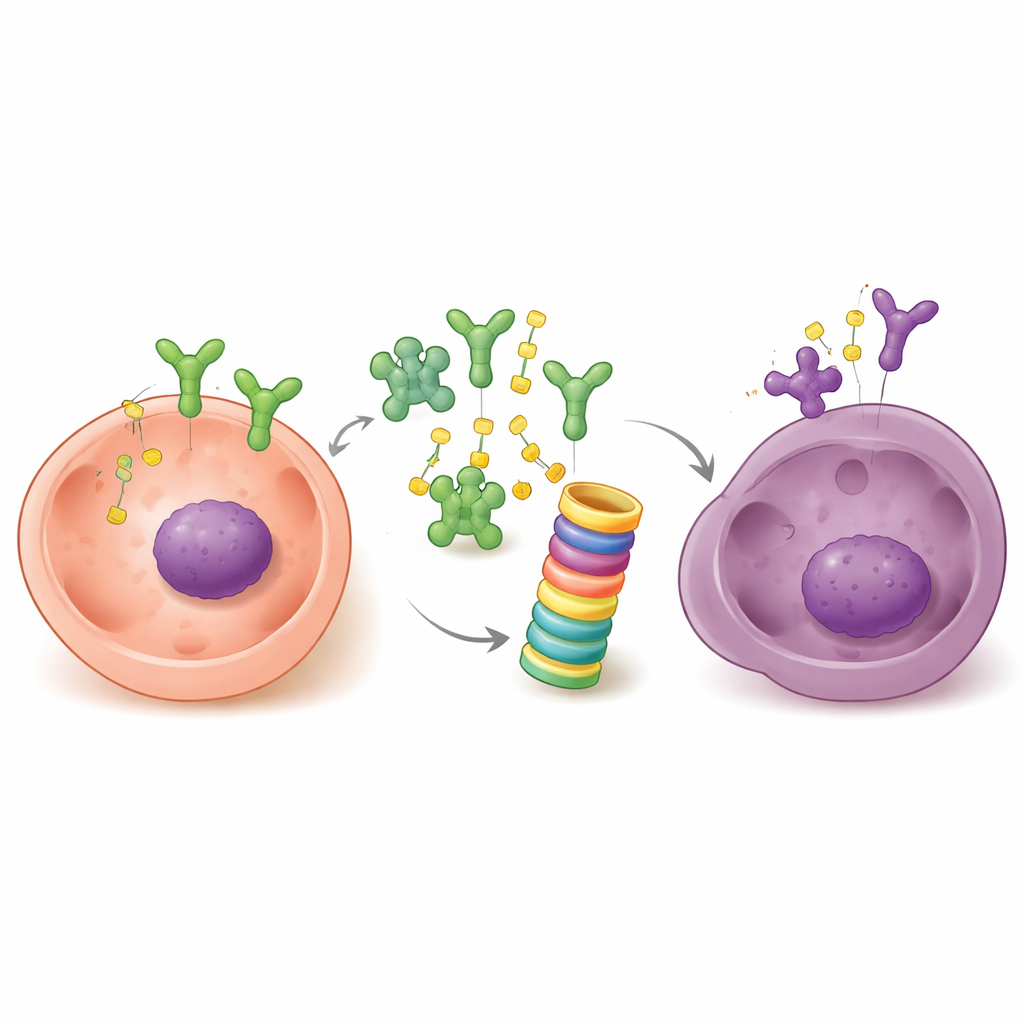
إعادة تحويل المقاومة إلى قابلية للهجوم
وبما أن UHRF1 يساعد على محو إشارة الهرمونات، اختبر الباحثون ما إذا كان حجب UHRF1 يمكن أن يجعل الأورام المقاومة حساسة للإنزالاتاميد مرة أخرى. في زراعة الخلايا، أدى تثبيط UHRF1 إلى إبطاء نمو الخلايا المقاومة للإنزالاتاميد، والأهم من ذلك، جعلها تستجيب للدواء من جديد. أدى الجمع بين فقدان UHRF1 وعلاج الإنزالاتاميد إلى قمع تكاثر الخلايا بدرجة أكبر بكثير من أي من النهجين منفردين، ويرجع ذلك إلى حد كبير إلى تقليل النمو بدلاً من إحداث موت خلوي جماعي. في فئران تحمل ترقيعات لأورام بروستاتا مقاومة، انكمشت الأورام ذات مستويات UHRF1 المنخفضة بشكل كبير تحت تأثير الإنزالاتاميد، بينما بالكاد استجابت الأورام الضابطة. أظهرت التحليلات الجزيئية انقلاباً جزئياً للصفات العدوانية الشبيهة بالعصبونية الصماوية، بما يتوافق مع تحول عكسي نحو حالة أكثر استجابة للهرمونات.
ماذا يعني هذا للمرضى
تُرسم هذه النتائج صورة واضحة: تحت ضغط علاجات حجب الهرمونات، تساهم مستويات UHRF1 المتصاعدة في تمكين السرطانات من التخلي عن اعتمادها على مستقبل الأندروجين عن طريق تسريع تدميره. هذا يدفع الأورام نحو هوية أكثر قابلية للتغيير ومقاومة للأدوية. إن مقاطعة UHRF1 خلال هذه النافذة الانتقالية يمكن أن تحافظ على الإشارة الهرمونية أو تعيدها لفترة تكفي لأن تستمر أدوية مثل الإنزالاتاميد في العمل. بينما من غير المرجح أن يخلص تثبيط UHRF1 بمفرده إلى شفاء للمرض المتقدم والمتحول بالكامل، فإن استهداف هذا الجزيء إلى جانب العلاج القياسي قد يؤخر أو يمنع التحول إلى حالة غير قابلة للعلاج، مما يوفّر للمرضى وقتاً أطول وتحكماً أكثر فعالية في سرطانهم.
الاستشهاد: Zhang, Y., Yu, Z., Li, Y. et al. UHRF1 regulates AR ubiquitination to promote the loss of AR signaling and enzalutamide resistance in progression of prostate cancer. Cell Death Dis 17, 286 (2026). https://doi.org/10.1038/s41419-026-08511-9
الكلمات المفتاحية: سرطان البروستاتا, مستقبل الأندروجين, مقاومة الأدوية, UHRF1, إنزالاتاميد