Clear Sky Science · zh
具有时序同步降解以增强骨整合的骨粘合剂
帮助断骨更好愈合的“胶水”
当骨头断成零散片段时,外科医生常依赖金属钢板和螺钉将碎片固定在一起。这些装置有效但体积大,可能需要二次手术取出,而且并不总是符合骨组织自然愈合的方式。本研究介绍了一种新型骨用“强力胶”,它不仅能牢固固定碎片,还被设计为随身体自身修复进程同步消失,从而有望使骨折治疗更温和、更有效。
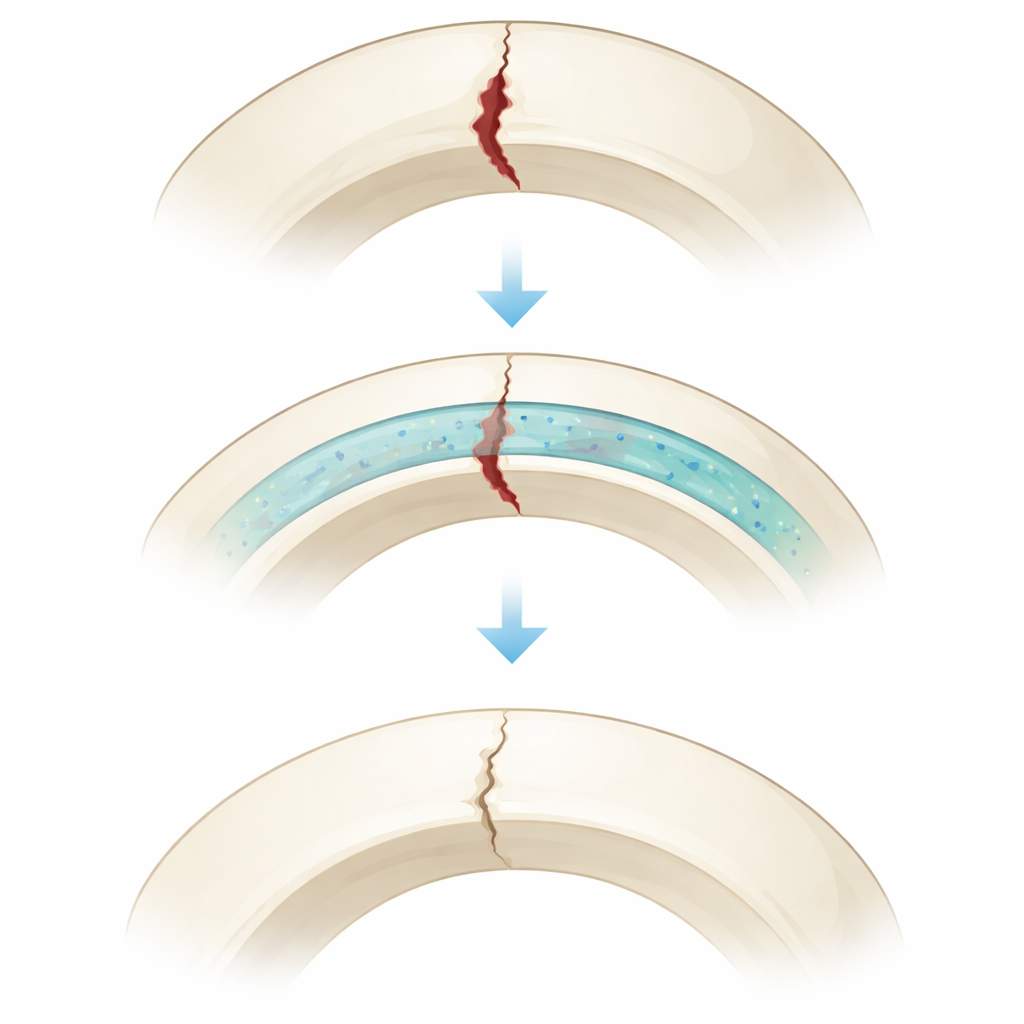
为什么骨头需要更智能的粘合剂
传统被称为骨水泥或组织粘合剂的材料存在重要缺点。有些难以牢固附着于致密骨表面,另一些虽强但固化时间过长或在体内滞留时间过久。如果粘合剂降解太快,骨折可能松动;如果停留太久,会阻碍新骨和血管的生长。天然骨愈合经过明确阶段,从早期血凝和软组织形成到硬骨痂,最后缓慢重塑。该研究的核心思想是:真正先进的骨粘合剂应与这些阶段相匹配——在早期非常稳定,然后在骨组织足够坚固时加速降解。
构建对骨友好的“超级胶”
研究者制备了一种基于聚氨酯的材料,称为TNC,由三种构件组成:一种反应性连接分子(tri-HDI)、微小的类骨矿物颗粒(纳米羟基磷灰石)以及天然骨中主要蛋白质I型胶原。混合后,这些成分形成一种起初为粘稠液体并在类体温条件下约十分钟内固化的胶,避免了可能损伤组织的高温峰值。通过调节胶原的添加量,团队调控了材料的内部孔隙结构。较高的胶原含量产生更开放、海绵状的结构,便于细胞和体液进入;较低的胶原则提供更高的机械强度。在各个配方中,该粘合剂对致密骨和松质骨均表现出强的粘结力,即使在潮湿或被血液污染的表面也能保持粘附,性能可与现有实验性骨粘合剂媲美或更优。
对细胞安全且对机体温和
任何植入物都必须对活组织友好。在体外实验中,与TNC胶提取物共培养的成骨细胞仍保持高存活率,且该材料对红细胞几乎没有破坏作用。在显微镜下,细胞深度迁移进入多孔结构,尤其是在更开放、高胶原配方中,这表明该胶可作为新组织的支架。在大鼠体内,将小块TNC置于皮下并未对主要器官造成损害,也未扰乱常规血液指标。相反,宿主细胞和结缔组织长入材料孔隙,显示机体良好耐受该粘合剂并开始整合而非将其隔离包裹。
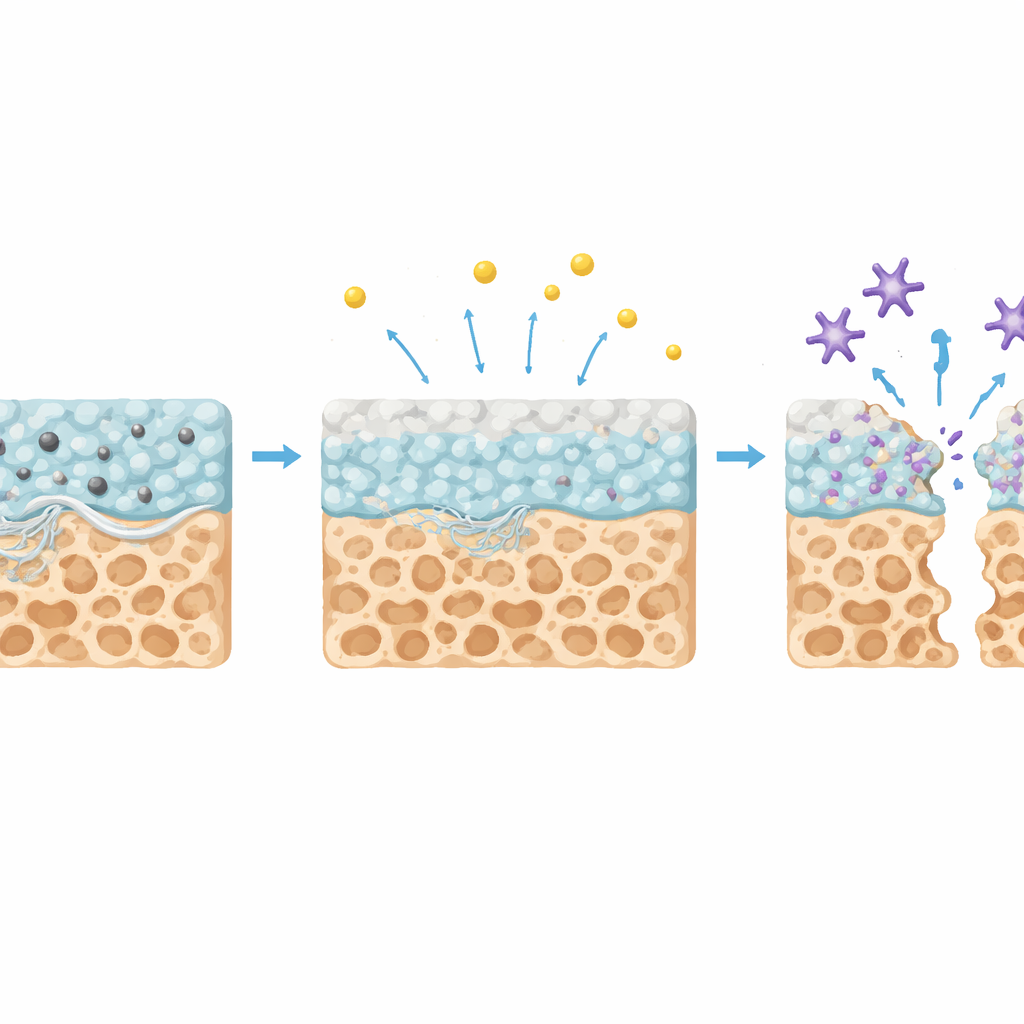
一种会加速自身消失的胶
TNC最具创新性的特征是其随时间的降解行为。在正常骨重塑过程中,专门细胞会释放一种名为猫hepsin K的酶来溶解旧骨基质。研究团队表明,在该酶存在时,TNC起初缓慢降解,然后在数周后通过在表面形成富含钙磷的薄矿物层来自我加速降解。该矿层释放钙离子,进而改变猫hepsin K的构象与柔性,使该酶活性增强。因此,胶在后期的降解速率几乎翻倍,恰好与天然骨重塑最活跃的阶段重合。与此同时,材料的矿物含量及亲水多孔结构也鼓励成骨细胞沉积新矿物,进一步支持修复过程。
帮助动物颅骨断裂愈合
为验证这一概念在活体骨中的效果,研究者在大鼠头骨上制造圆形骨折,并分别采取不治疗、使用仅含胶原的胶或使用含矿物颗粒的完整TNC配方三种处理。未使用任何粘合剂时,骨片保持错位并未能正常愈合。仅胶原的配方提供了一定的稳定性,但降解太慢,留下大量材料,限制了新骨和血管的形成。相比之下,TNC既牢固固定碎片,又在表面形成矿物层,并随后及时降解,为血管和新骨腾出空间。影像与组织染色显示,TNC组的骨折愈合桥接更完整,骨体积和密度更高,并有明显的新骨与血管生成,而粘合剂残留很少。
这对未来骨折护理意味着什么
通俗地说,该研究描述了一种行为类似于定时临时支架的骨胶。它在碎片脆弱时抓牢并固定,随后感知机体的重塑信号,在新骨接管时退出。通过结合早期牢固固定、良好生物相容性与内置的晚期降解加速触发器,TNC指向了修复复杂骨折的下一代“智能”材料。尽管还需在不同骨骼和更大型动物中做更多测试,这一方法表明未来外科医生有可能通过可注射的粘合剂固定困难骨折,而这些粘合剂会在患者自身骨骼恢复时安全消失。
引用: Gu, Jt., Li, Zt., Wang, Yz. et al. Bone adhesive with temporally-synchronized degradation for enhanced osteointegration. Bone Res 14, 39 (2026). https://doi.org/10.1038/s41413-026-00522-8
关键词: 骨粘合剂, 骨折愈合, 可生物降解植入物, 骨再生, 智能生物材料