Clear Sky Science · de
Knochenkleber mit zeitlich synchronem Abbau zur verbesserten Osteointegration
Klebstoff, der gebrochenen Knochen beim besseren Heilen hilft
Wenn ein Knochen in ungünstige Stücke zerbricht, verlassen sich Chirurgen oft auf Metallplatten und -schrauben, um alles zusammenzuhalten. Diese Vorrichtungen funktionieren gut, können aber sperrig sein, Zweitoperationen zur Entfernung erfordern und stimmen nicht immer mit der natürlichen Art des Knochenheilens überein. Diese Studie stellt eine neue Art von Knochen‑„Superkleber“ vor, der nicht nur Fragmente fest an ihrem Platz hält, sondern so gestaltet ist, dass er im Takt mit dem körpereigenen Reparaturprozess verschwindet — was die Behandlung von Frakturen schonender und wirkungsvoller machen könnte.
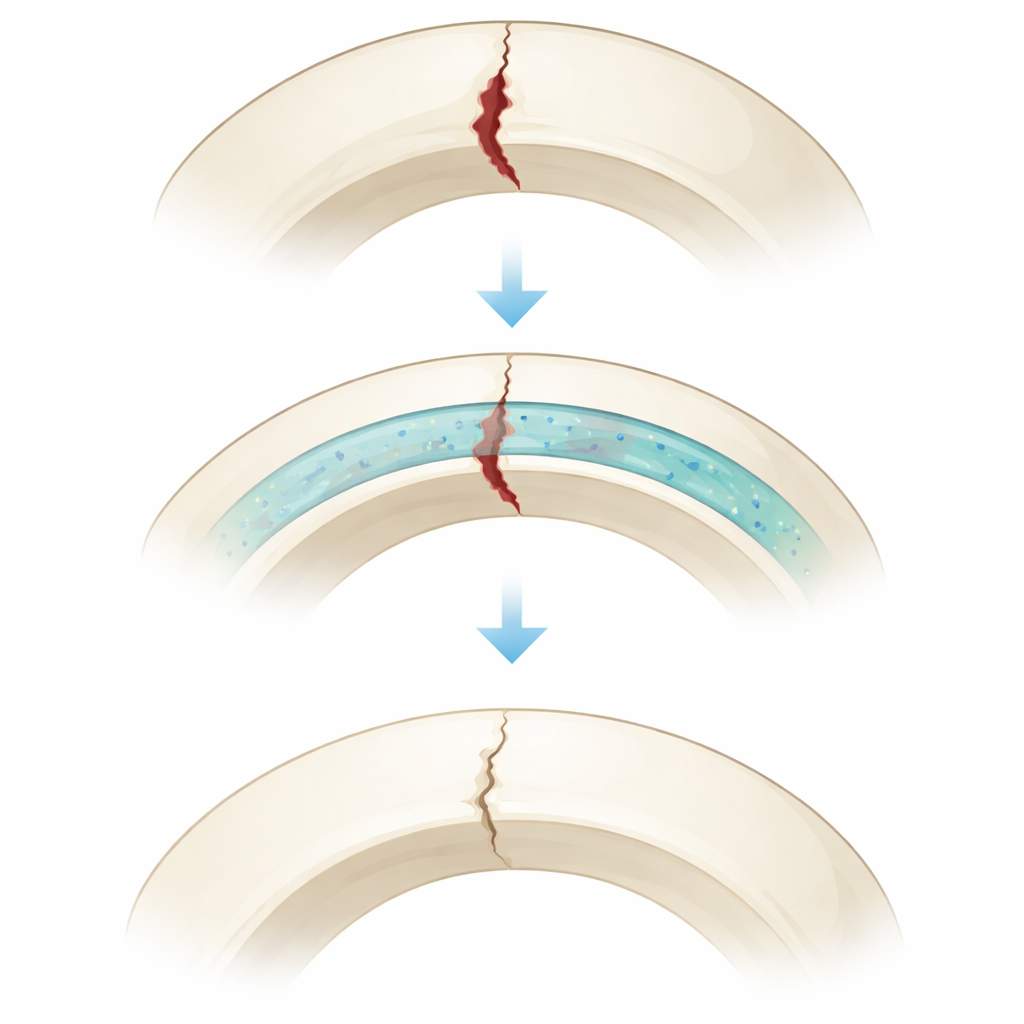
Warum Knochen einen intelligenteren Kleber brauchen
Traditionelle Materialien, die als Knochenzemente oder Gewebekleber bezeichnet werden, haben bedeutende Nachteile. Manche haften schlecht an hartem Knochen, andere sind zwar stark, härten aber zu langsam aus oder verbleiben lange im Körper, nachdem sie nicht mehr benötigt werden. Wenn ein Klebstoff zu schnell verschwindet, kann die Fraktur sich lösen; bleibt er zu lange, kann er das Wachstum neuen Knochens und neuer Blutgefäße blockieren. Die natürliche Knochenheilung durchläuft klar definierte Phasen — von frühem Blutgerinnsel und weichem Gewebe über harten Kallus bis hin zur langsamen Umformung des Knochens. Die zentrale Idee dieser Arbeit ist, dass ein wirklich fortschrittlicher Knochenkleber diese Phasen widerspiegeln sollte: anfangs sehr stabil und dann erst schneller abbauend, wenn der Knochen stark genug ist, die Belastung zu übernehmen.
Entwicklung eines knochenfreundlichen Superklebers
Die Forscher entwickelten ein auf Polyurethan basierendes Material, das sie TNC nennen und das aus drei Bausteinen besteht: einem reaktiven Verbindungsmolekül (tri‑HDI), winzigen Partikeln knochenähnlichen Minerals (Nano‑Hydroxylapatit) und Typ‑I‑Kollagen, dem Hauptprotein des natürlichen Knochens. Zusammen gemischt bilden diese Zutaten einen Klebstoff, der als viskose Flüssigkeit beginnt und sich innerhalb von etwa zehn Minuten bei körperähnlichen Temperaturen verfestigt, wobei Hitze‑Spitzen vermieden werden, die Gewebe schädigen könnten. Durch Anpassung der zugesetzten Kollagenmenge justierte das Team die innere Porenstruktur des Materials. Höhere Kollagenanteile erzeugten einen offeneren, schwammartigen Kleber, der für Zellen und Flüssigkeiten leichter zugänglich war, während geringere Kollagenanteile zu höherer mechanischer Festigkeit führten. In allen Versionen zeigte der Klebstoff eine starke Haftung an sowohl dichter als auch schwammiger Knochenoberfläche, sogar bei nassen oder blutverschmutzten Flächen, und erreichte damit Leistungen, die mit bestehenden experimentellen Knochenklebern mithalten oder diese übertreffen.
Zellverträglich und schonend für den Körper
Jedes Implantat muss lebendem Gewebe gegenüber verträglich sein. In Labortests blieben knochenbildende Zellen, die mit Extrakten des TNC‑Klebers kultiviert wurden, hoch lebensfähig, und das Material verursachte nahezu keine Schädigung roter Blutkörperchen. Unter dem Mikroskop wanderten Zellen tief in die poröse Struktur ein, besonders in der offeneren, kollagenreicheren Variante, was darauf hindeutet, dass der Klebstoff als Gerüst für neues Gewebe fungieren kann. Bei Ratten führten kleine unter die Haut eingesetzte TNC‑Proben nicht zu Schäden an wichtigen Organen oder zu Störungen routinemäßiger Blutwerte. Stattdessen wuchsen Wirtszellen und Bindegewebe in die Poren des Materials ein, was zeigt, dass der Körper den Klebstoff gut tolerierte und begann, ihn zu integrieren, anstatt ihn abzukapseln.
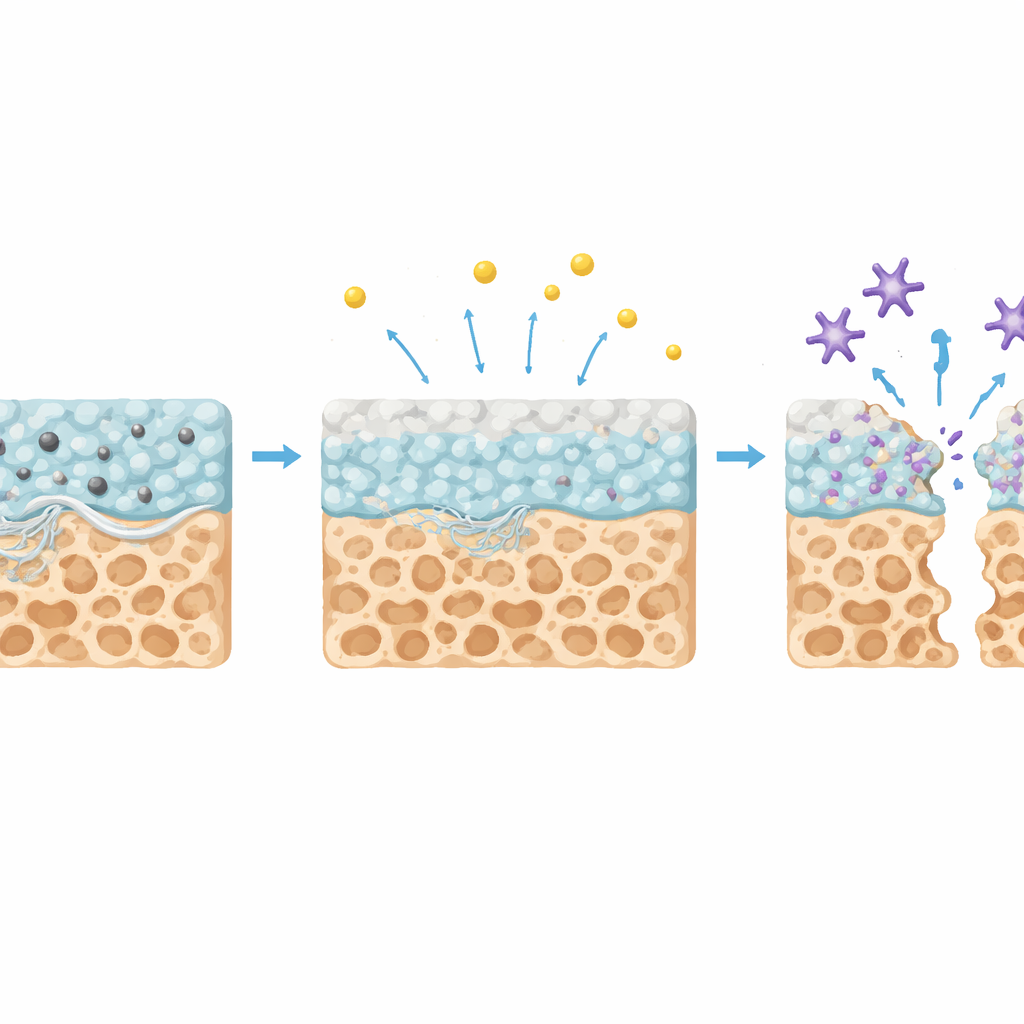
Ein Kleber, der sein eigenes Verschwinden beschleunigt
Das innovativste Merkmal von TNC ist, wie es sich im Laufe der Zeit abbaut. Während der normalen Knochenumbauprozesse setzen spezialisierte Zellen ein Enzym namens Cathepsin K frei, das hilft, alte Knochenmatrix aufzulösen. Das Team zeigte, dass TNC in Anwesenheit dieses Enzyms zunächst langsam zerfällt, dann aber nach einigen Wochen seinen eigenen Abbau beschleunigt, indem es an seiner Oberfläche eine dünne Mineralschicht reich an Calcium und Phosphat bildet. Diese Schicht setzt Calciumionen frei, die wiederum die Form und Flexibilität von Cathepsin K verändern und das Enzym aktiver machen. In der Folge verdoppelt sich die Abbaurate des Klebers in der späteren Phase nahezu — genau zu dem Zeitpunkt, an dem der natürliche Knochenumbau am aktivsten ist. Gleichzeitig fördern der Mineralgehalt und die poröse, wasserliebende Struktur des Materials das Absetzen neuen Minerals durch knochenbildende Zellen und unterstützen so die Reparatur weiter.
Unterstützung der Heilung gebrochener Schädelfragmente in Tiermodellen
Um zu prüfen, ob dieses Konzept im lebenden Knochen funktioniert, erzeugten die Forscher kreisförmige Schädelfrakturen bei Ratten und ließen diese entweder unbehandelt, stabilisierten sie mit einem ausschließlich aus Kollagen bestehenden Kleber oder verwendeten die vollständige TNC‑Formulierung mit Mineralpartikeln. Ohne Kleber blieben die Knochenfragmente fehlgestellt und heilten nicht ordentlich. Der Kollagen‑allein‑Kleber bot eine gewisse Stabilisierung, baute sich jedoch zu langsam ab, so dass ein Großteil des Materials bestehen blieb und neues Knochen‑ und Gefäßwachstum einschränkte. Im Gegensatz dazu hielt TNC die Fragmente sicher, bildete eine mineralische Oberfläche und baute sich dann zeitgerecht ab, wodurch Platz für Blutgefäße und neuen Knochen entstand. Bildgebende Verfahren und Gewebefärbungen zeigten eine vollständigere Überbrückung der Fraktur, ein höheres Knochenvolumen und eine größere Dichte sowie deutliche Anzeichen neuen Knochen‑ und Gefäßwachstums in der TNC‑Gruppe, während nur kleine Reste des Klebers zurückblieben.
Was das für die zukünftige Frakturversorgung bedeuten könnte
Alltäglich ausgedrückt beschreibt diese Studie einen Knochenkleber, der wie ein gut getimtes temporäres Gerüst funktioniert. Er greift und hält gebrochene Stücke sicher, solange sie fragil sind, erkennt dann die körpereigenen Umbau‑Signale und tritt zurück, sobald neuer Knochen die Aufgabe übernimmt. Durch die Kombination starker Anfangsstabilisierung, guter Biokompatibilität und eines eingebauten Auslösers für einen schnelleren Abbau in der Spätphase weist TNC auf eine neue Generation von „intelligenten“ Materialien zur Versorgung komplexer Frakturen hin. Obwohl weitere Tests an unterschiedlichen Knochen und in größeren Tiermodellen nötig sind, deutet der Ansatz darauf hin, dass Chirurgen künftig schwierige Brüche mit injizierbaren Klebern fixieren könnten, die sicher verschwinden, während das körpereigene Skelett wiederhergestellt wird.
Zitation: Gu, Jt., Li, Zt., Wang, Yz. et al. Bone adhesive with temporally-synchronized degradation for enhanced osteointegration. Bone Res 14, 39 (2026). https://doi.org/10.1038/s41413-026-00522-8
Schlüsselwörter: Knochenkleber, Frakturheilung, biologisch abbaubares Implantat, Knochenregeneration, intelligentes Biomaterial