Clear Sky Science · zh
通过肥胖脂肪组织移植减轻基于活动的厌食症被新生期AgRP神经元消融所消除
这项研究为何重要
神经性厌食症是致死率极高的精神疾病之一,主要原因是患者难以在治疗下恢复并维持健康体重。临床上仍缺乏能够可靠恢复体重的药物。本研究利用一种强大的小鼠厌食样行为模型,探讨对抗危险性体重下降的意想不到盟友:体脂本身。研究者通过询问来自既往肥胖动物的脂肪是否能抵御极端消瘦,揭示了脂肪组织与大脑之间一种意外的对话,可能为新疗法提供灵感。
自我饥饿的实验室模型
为了研究厌食样状态的生物学机制,科学家常用“基于活动的厌食”(ABA)模型。在该模型中,原本健康的啮齿动物可以使用跑轮,但每天只有很短的进食窗口。许多动物会跑得更多、吃得更少,体重迅速下降,当它们失去初始体重的四分之一时便会退出实验。该模型模拟了人类神经性厌食症的关键特征:限制性进食、强迫性运动和剧烈体重下降,尤其在年轻雌性中常见。因为实验条件可控,ABA让研究者可以测试哪些体内系统帮助动物抵抗或陷入这一恶性循环。
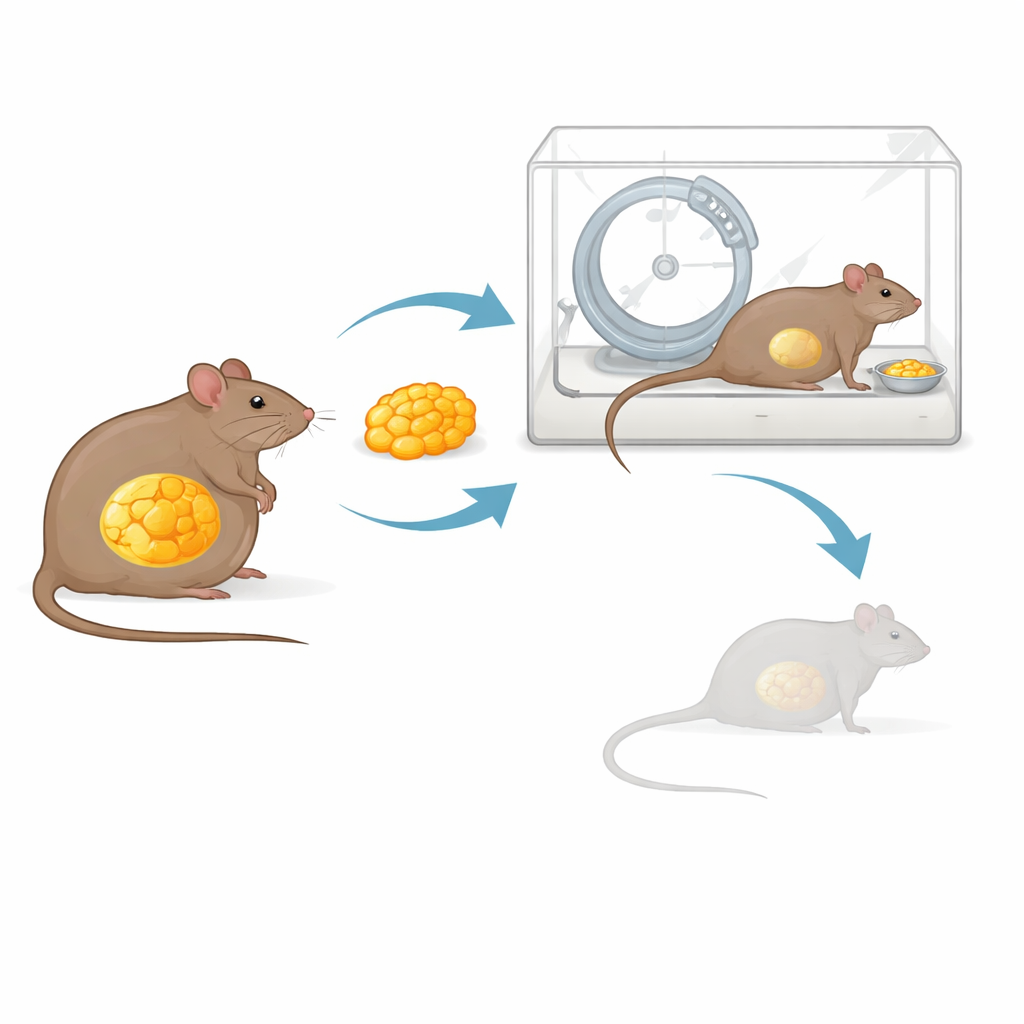
作为保护性移植的肥胖脂肪
近期的代谢研究显示,白色脂肪组织不仅是被动的储能仓库,还是一种记忆既往肥胖的内分泌器官。即便在体重下降后,来自既往肥胖动物的脂肪仍保有独特的分子“印记”,并持续发出有利于恢复体重的信号。作者提出疑问:能否将这种记忆转化为优势——来自肥胖小鼠的移植脂肪能否帮助体重正常的雌鼠抵抗由ABA驱动的消瘦?他们从在高脂饮食下变得肥胖的小鼠腹部取脂,并将其外科植入瘦受体鼠的腹腔内。对照组接受等量来自瘦供体的脂肪。恢复数周后,所有小鼠均进入带跑轮和有限食物供应的ABA程序。
脂肪到大脑的信号提升存活率
结果令人瞩目。接受肥胖脂肪移植的小鼠在达到关键的25%体重减轻阈值之前,在ABA实验中坚持的时间更长。换言之,在苛刻条件下,它们比接受瘦脂肪的小鼠“存活”得更好。在两次独立实验中,移植的肥胖脂肪帮助小鼠在限制期内维持更高的体重,并显示出可能促进更高食量的迹象,而不一致地改变它们在跑轮上的运动量。这些模式表明,移植的脂肪以某种方式鼓励动物节约能量并增加进食,从而缓冲自我饥饿的螺旋,而不是简单地降低其活动水平。
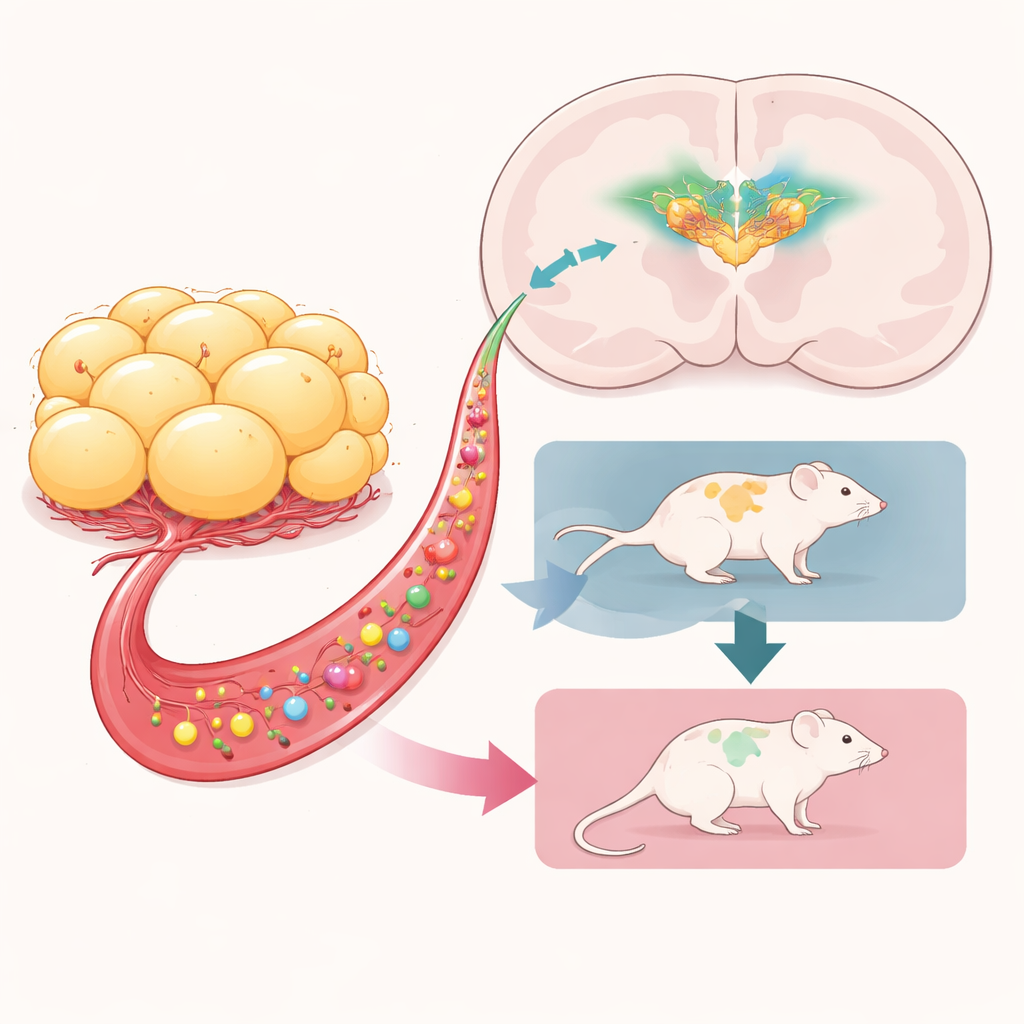
感知饥饿的大脑细胞发挥关键作用
团队随后探究了哪些大脑回路对这种保护性效应是必要的。他们聚焦于AgRP神经元——位于下丘脑深处的一小群细胞,能感知能量短缺并驱动食物寻求、燃料保存和代谢转变。研究者使用一种遗传手段,在部分小鼠出生后不久选择性地消除这些神经元,另一些则保留完整。所有动物随后接受肥胖或瘦脂肪移植,并接受相同的ABA程序。当AgRP神经元完整时,肥胖脂肪再次帮助小鼠维持体重并延长存活时间。但当这些神经元在婴儿期被消除时,这一益处消失:既接受肥胖脂肪又缺失AgRP神经元的小鼠体重迅速下降,并比可比对照更快退出实验。
这对未来治疗构想意味着什么
综合来看,研究结果指向一条从肥胖脂肪组织到大脑AgRP神经元的直接通讯通路,这二者共同作用以在压力下保护机体免受极端体重下降。移植脂肪释放的信号——很可能是由既往肥胖塑造的激素和其他循环分子混合物——似乎激活了这些与饥饿相关的神经元,推动机体增加进食并节约能量。虽然将肥胖供体的脂肪外科移植给人类并非实用疗法,但识别出具体参与的因子可能激发出新的药物,从而安全地利用机体自身保持体重的回路。对于因持续体重下降而生命受威胁的神经性厌食症患者,这类来源于脂肪的信号也许有朝一日能帮助患者朝康复方向转变。
引用: Yoon, D.J., Zhang, J., Zapata, R.C. et al. The mitigation of activity-based anorexia by obese adipose tissue transplant is abolished by neonatal AgRP neuron ablation. Transl Psychiatry 16, 199 (2026). https://doi.org/10.1038/s41398-026-03970-2
关键词: 神经性厌食症, 基于活动的厌食, 白色脂肪组织, AgRP神经元, 代谢信号