Clear Sky Science · nl
Het verminderen van activity-based anorexia door transplantatie van vetweefsel uit obese dieren wordt opgeheven door neonatale Ablatie van AgRP-neuronen
Waarom dit onderzoek ertoe doet
Anorexia nervosa is een van de dodelijkste psychiatrische aandoeningen, grotendeels omdat patiënten moeite hebben om aan te komen en gewicht vast te houden, zelfs met intensieve zorg. Artsen hebben nog geen medicijnen die betrouwbaar een gezond gewicht herstellen. Deze studie gebruikt een krachtig muismodel van anorexia-achtig gedrag om een onverwachte bondgenoot in de strijd tegen gevaarlijk gewichtsverlies te onderzoeken: lichaamsvet zelf. Door te vragen of vet van eerder obese dieren kan beschermen tegen extreem afvallen, onthullen de onderzoekers een verrassende communicatie tussen vetweefsel en de hersenen die nieuwe behandelingen zou kunnen inspireren.
Een laboratoriummodel van zelfuithongering
Om de biologie van anorexia-achtige toestanden te onderzoeken, gebruiken wetenschappers vaak het “activity-based anorexia” (ABA)-model. In deze opzet krijgen anders gezonde knaagdieren toegang tot een renrad, maar mogen ze slechts tijdens een korte dagelijkse periode eten. Velen reageren door meer te rennen en minder te eten, waardoor ze snel gewicht verliezen en uiteindelijk uit het experiment vallen wanneer ze een kwart van hun begingewicht verliezen. Dit model bootst belangrijke kenmerken van menselijke anorexia nervosa na: restrictief eten, dwangmatig bewegen en dramatisch gewichtsverlies, vooral bij jongere vrouwtjes. Omdat de omstandigheden gecontroleerd zijn, laat ABA onderzoekers testen welke lichaamssystemen dieren helpen deze neerwaartse spiraal te weerstaan of eraan ten onder te gaan.
Obese vet als beschermende transplantatie
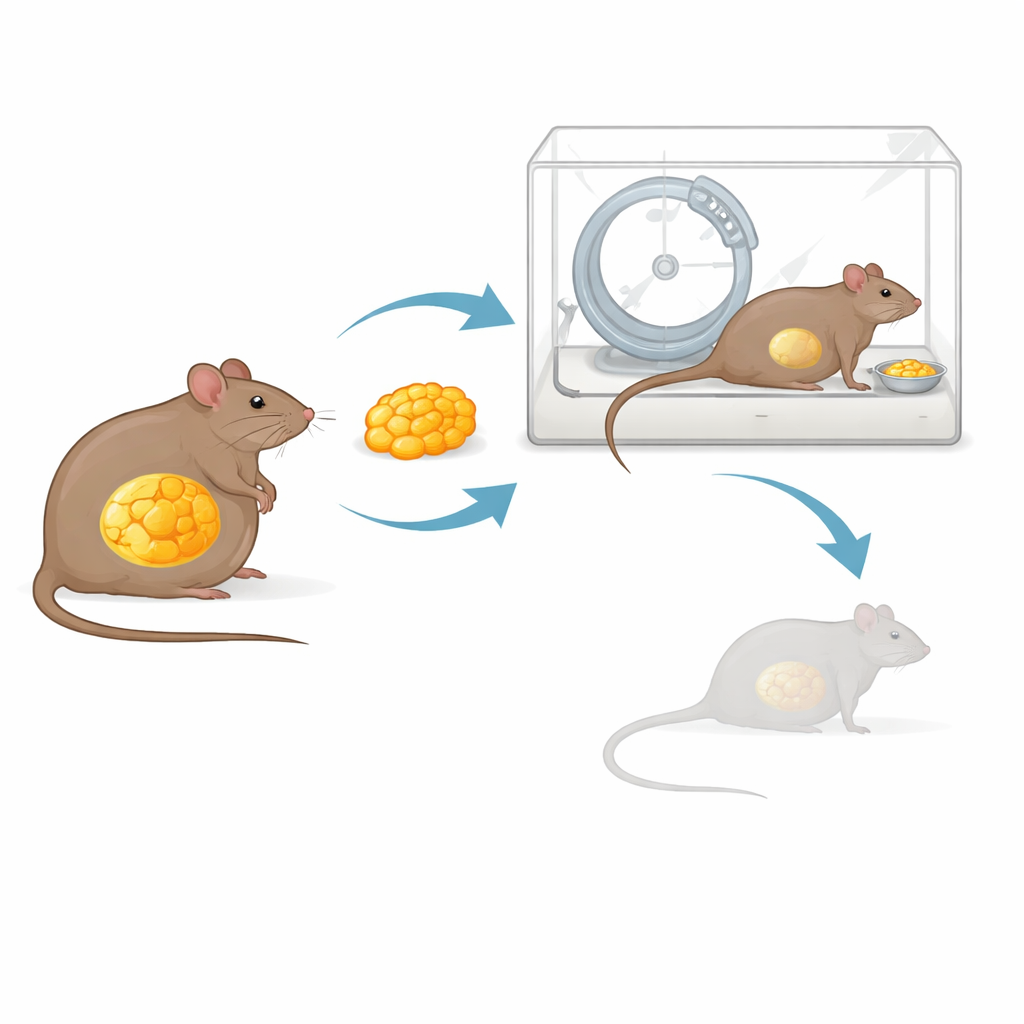
Recent metabolisch werk heeft aangetoond dat wit vetweefsel niet slechts een passieve opslagplaats is, maar een endocrien orgaan dat zich eerdere obesitas herinnert. Zelfs na gewichtsverlies behoudt vet van eerder obese dieren een onderscheidend moleculair “handtekening” en blijft het signalen afgeven die herstel van gewicht bevorderen. De auteurs vroegen zich af of diezelfde herinnering in het voordeel kon worden gebruikt—zou getransplanteerd vet van obese muizen kunnen helpen normale gewichtige vrouwtjes weerstand te bieden tegen ABA-gedreven verarming? Ze namen vet uit de buik van muizen die obees waren gemaakt met een vetrijk dieet en hechtten dit chirurgisch in de buiken van magere ontvangers. Controle dieren kregen dezelfde hoeveelheid vet van magere donoren. Na enkele weken herstel begonnen alle muizen aan het ABA-protocol met renraderen en beperkte voedseltoegang.
Vet-naar-hersenen signalering verhoogt overleving
De resultaten waren opvallend. Muizen die obese vettransplantaties kregen, bleven langer in het ABA-experiment voordat ze de kritische drempel van 25 procent gewichtsverlies bereikten. Met andere woorden, ze “overleefden” beter onder de veeleisende omstandigheden dan muizen die mager vet kregen. In twee onafhankelijke experimenten hielp getransplanteerd obese vet muizen hun lichaamsgewicht hoger te houden tijdens de restrictie en suggereerde het een toename van de voedselinname, zonder consequent te veranderen hoeveel ze aan hun raderen renden. Deze patronen suggereren dat het getransplanteerde vet de dieren op de een of andere manier aanmoedigde energie te besparen en meer te eten, waardoor ze werden gebufferd tegen de zelfuithongeringsspiraal, in plaats van ze eenvoudigweg minder actief te maken.
Een sleutelrol voor honger-sensorische hersencellen
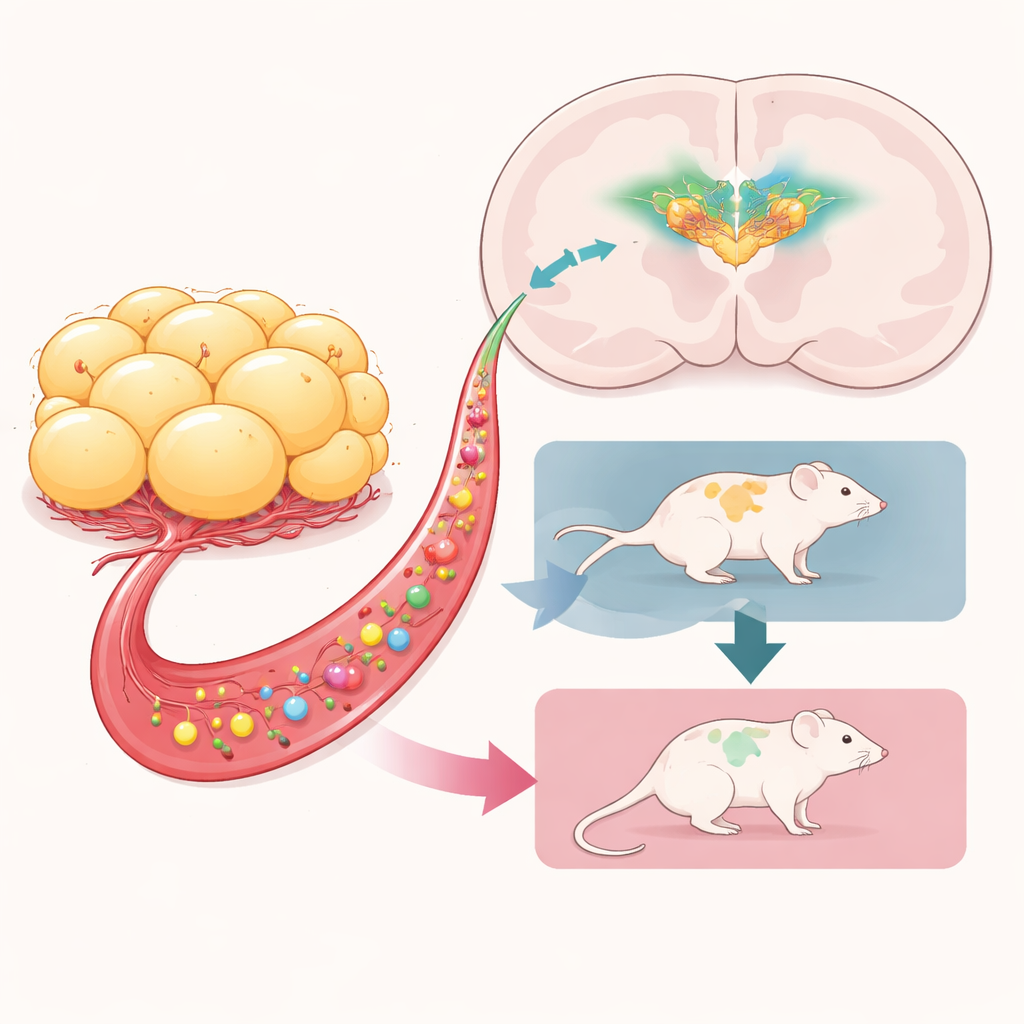
Het team vroeg vervolgens welke hersencircuits nodig waren voor dit beschermende effect. Ze richtten zich op AgRP-neuronen, een kleine groep cellen diep in de hypothalamus die energietekort detecteren en voedselzoekgedrag, brandstofbesparing en metabole verschuivingen aandrijven. Met een genetische truc wisten ze deze neuronen selectief uit te schakelen kort na de geboorte bij sommige muizen, terwijl anderen intact bleven. Al deze dieren kregen later ofwel obese of mager vettransplantaties en ondergingen hetzelfde ABA-protocol. Wanneer AgRP-neuronen intact waren, hielp obese vet opnieuw muizen gewicht te behouden en langer te overleven. Maar wanneer deze neuronen in de infancy waren verwijderd, verdween het voordeel: muizen met obese vet en ontbrekende AgRP-neuronen verloren snel gewicht en verlieten het experiment zelfs sneller dan vergelijkbare controles.
Wat dit betekent voor toekomstige behandelideeën
Samen wijzen de bevindingen op een directe communicatielijn van obese adipose weefsels naar AgRP-neuronen in de hersenen, die gezamenlijk beschermen tegen extreem gewichtsverlies onder stress. Signalen die door het getransplanteerde vet worden afgegeven—waarschijnlijk een mix van hormonen en andere circulerende moleculen gevormd door eerdere obesitas—lijken deze hongergerelateerde neuronen te activeren, waardoor het lichaam gestimuleerd wordt meer te eten en energie te sparen. Hoewel het chirurgisch transplanteren van vet van obese donoren naar mensen geen praktische therapie is, kan het identificeren van de specifieke factoren die betrokken zijn nieuwe geneesmiddelen inspireren die veilig gebruikmaken van de eigen gewichtsbeschermende circuits van het lichaam. Voor patiënten met anorexia nervosa, wier leven wordt bedreigd door onophoudelijk gewichtsverlies, zouden dergelijke vet-afgeleide signalen op termijn kunnen helpen het evenwicht weer naar herstel te verschuiven.
Bronvermelding: Yoon, D.J., Zhang, J., Zapata, R.C. et al. The mitigation of activity-based anorexia by obese adipose tissue transplant is abolished by neonatal AgRP neuron ablation. Transl Psychiatry 16, 199 (2026). https://doi.org/10.1038/s41398-026-03970-2
Trefwoorden: anorexia nervosa, activity-based anorexia, wit vetweefsel, AgRP-neuronen, metabole signalering