Clear Sky Science · zh
丧失 p300/CBP 相关因子加剧心脏重构:通过调控 CAMKK2 的乙酰化
这项心脏研究为何重要
心力衰竭是导致住院的常见原因之一,且常常在心脏收缩腔室形态变化并功能减弱时逐步形成。本研究从心肌细胞内部寻找一个分子“开关”,它能帮助心脏在陷入衰竭前应对压力。理解这一开关可能为开发在高血压、激素风暴或其他慢性应激下保持心脏功能的新疗法提供线索。
心脏在压力下如何改变
当心脏面临长期应激,如高血压或激素过载时,心肌细胞会发生增大,心腔室发生重构。起初这种增大可能是有益的,有助于维持血流。但随着时间推移,主要的泵血腔室可能被拉伸,心壁变薄,收缩力减弱,导致气短和乏力。研究者把注意力放在这一重构过程上,探究为何有些心脏能适应而有些则进展为称为扩张型心肌病的弱化、扩大状态。
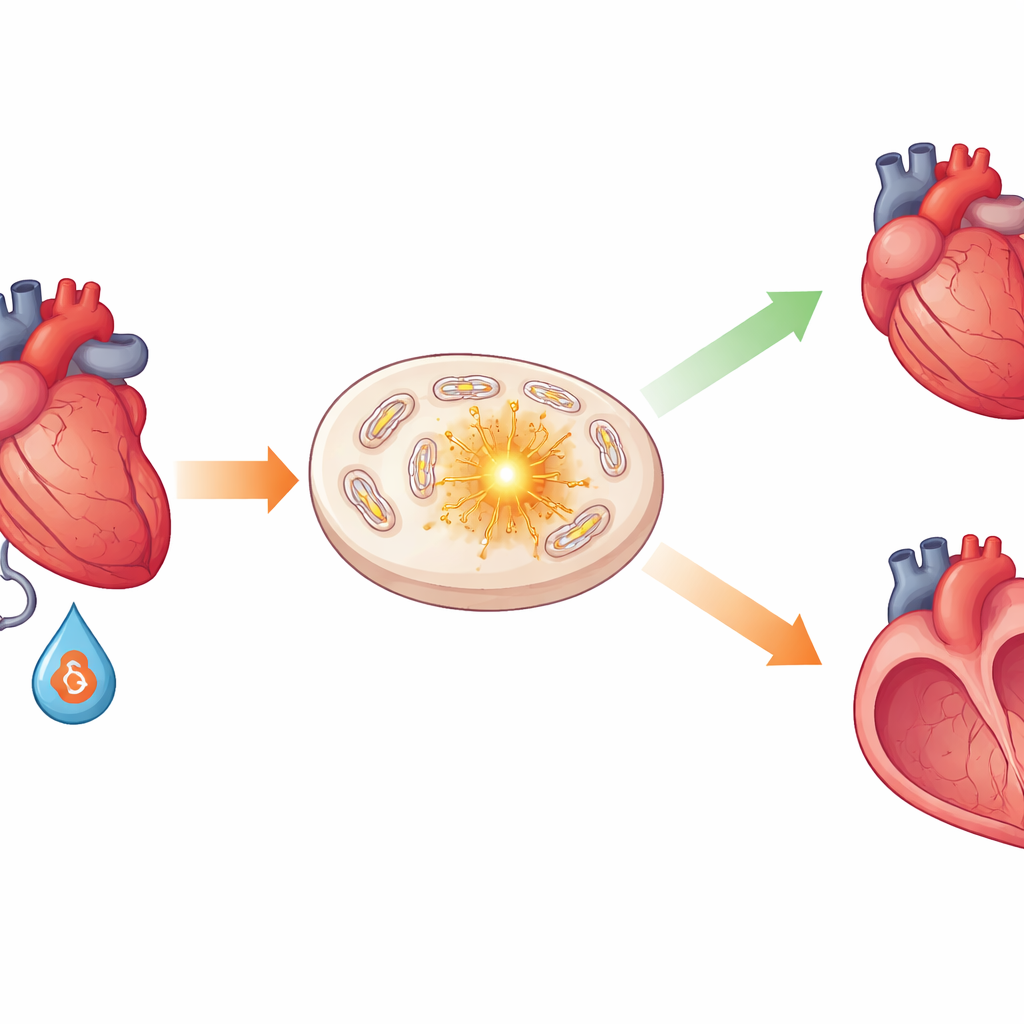
心肌细胞内的保护性帮手
研究团队研究了一种名为 PCAF 的蛋白,它以在其它蛋白上添加称为乙酰基的小化学标记而闻名。这些微小的标记可以改变蛋白的功能。研究者使用基因工程手段构建缺失 PCAF 的小鼠,对这些动物的心脏施加两类应激:一种药物模拟的应激激素激增,另一种是对离开心脏的主动脉进行手术性加压。在正常小鼠中,心肌出现肥厚但基本保持泵血功能。而在缺失 PCAF 的小鼠中,心腔室更大,心壁更薄,瘢痕增加且泵血功能下降,表现与人类扩张型心肌病相似。
将 PCAF 与细胞能量守护者联系起来
为弄清 PCAF 如何发挥保护作用,研究者考察了一条帮助细胞平衡能量供应的信号通路。该通路的中心是 AMPK,一种感知低能量并帮助细胞调整燃料使用的蛋白。另一个蛋白 CAMKK2 可激活 AMPK,但 CAMKK2 在心脏中如何被调控此前尚不清楚。本研究显示 PCAF 在心肌细胞中直接对 CAMKK2 进行乙酰化。这种乙酰化增强了 CAMKK2 激活 AMPK 的能力,进而支持健康的能量处理,并在应激期间帮助防止心肌发生有害的过度生长和功能衰弱。
当这个帮手缺失时会发生什么
在缺失 PCAF 的小鼠中,CAMKK2 所带的乙酰标记减少,AMPK 活性下降,心肌细胞的精细内部结构尤其是线粒体出现退化。面对激素或压力过载时,这些缺乏 PCAF 的心脏无法发起常见的保护性能量反应。心肌没有呈现受控的肥厚,反而腔室膨胀、心壁变薄,导致收缩力差并伴随更高的死亡率。当仅从心肌细胞中特异性去除 PCAF 时,也出现相同模式,说明这种保护作用主要来源于这些细胞内的作用,而非心脏中其他细胞类型。
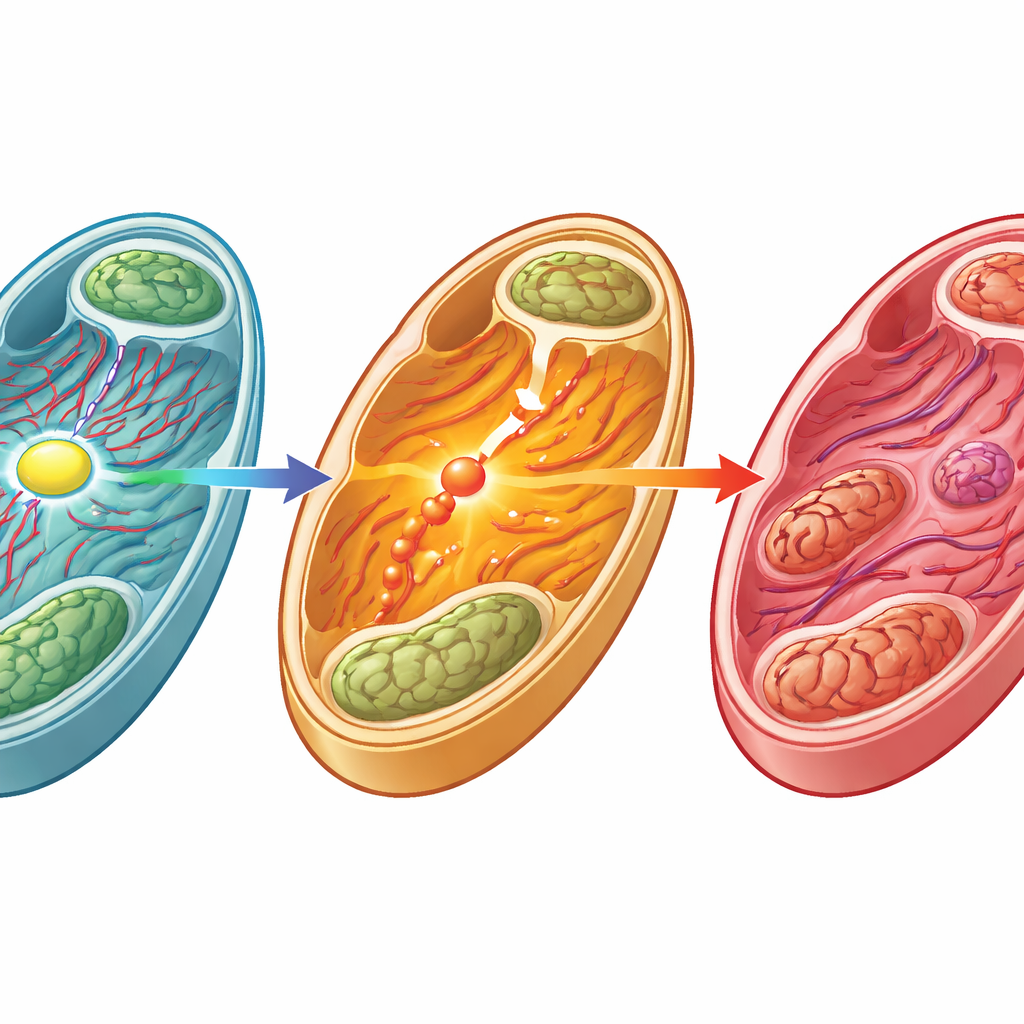
支持衰弱心脏的潜在新途径
科学家们还测试了一种名为 SPV106 的小分子药物,它能增强 PCAF 活性。在压力过载的小鼠中,SPV106 处理减少了腔室扩大与瘢痕形成并改善了泵血功能,同时提升了 CAMKK2 和 AMPK 的活性。对非专业读者而言,核心结论是 PCAF 像心肌细胞内的一个守护开关,帮助它们在应激时维持能量平衡和结构完整。当这一守护被缺失或削弱时,心脏更容易被拉伸、变薄并衰竭。温和激活这一开关或模拟其对 CAMKK2 与 AMPK 的作用的药物,未来可能有助于保护人们的心脏,防止滑向心力衰竭。
引用: Lim, Y., Jeong, A., Kwon, DH. et al. Loss of p300/CBP-associated factor aggravates cardiac remodeling via regulation of CAMKK2 acetylation. Exp Mol Med 58, 1297–1310 (2026). https://doi.org/10.1038/s12276-026-01698-z
关键词: 心力衰竭, 心脏重构, 能量代谢, AMPK 信号, 小鼠模型