Clear Sky Science · ja
p300/CBP関連因子(PCAF)の喪失はCAMKK2のアセチル化制御を介して心リモデリングを悪化させる
この心臓研究が重要な理由
心不全は入院の最も多い原因のひとつで、心臓のポンプ室が形を変え弱くなることでゆっくり進行することが多いです。本研究は心細胞内を調べ、心臓が失敗に陥る前にストレスに対処する分子レベルの「スイッチ」を明らかにしようとしています。このスイッチを理解することで、高血圧やホルモンの急増、その他の慢性ストレスにさらされた際に心臓の機能を保つ新しい治療法の手がかりが得られる可能性があります。
ストレス下での心臓の変化
高血圧やホルモン負荷のような長期的なストレスに直面すると、心筋細胞は肥大し、心室のリモデリングが起きます。初期にはこの成長は血流を維持するために有益に働くことがありますが、時間が経つと主要な駆出室が拡張し壁が薄くなり、その収縮力が低下して息切れや倦怠感を招きます。研究者らはこのリモデリング過程に注目し、なぜある心臓は適応できる一方で、他は拡張型心筋症として知られる弱く拡大した状態へ進行するのかを問いかけました。
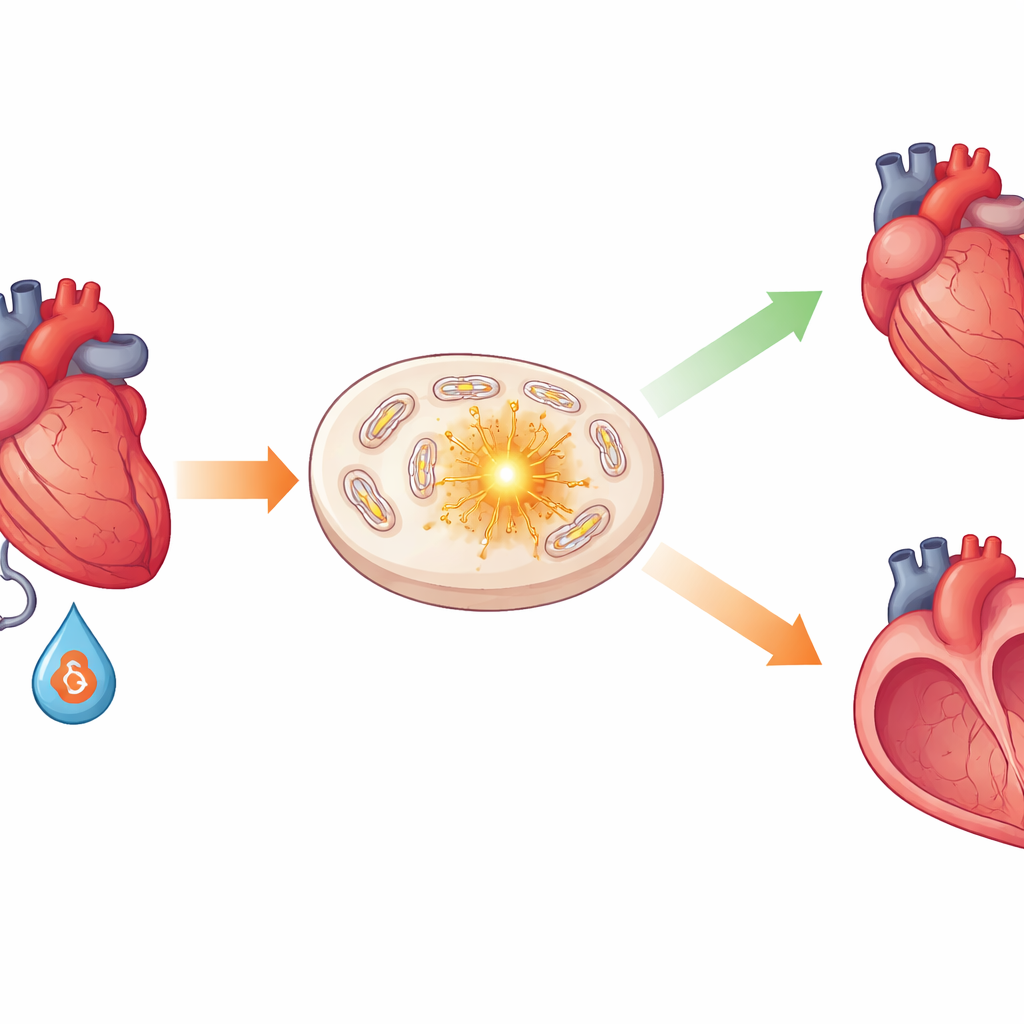
心細胞内の保護的な助け手
研究チームはPCAFと呼ばれるタンパク質を調べました。PCAFは他のタンパク質にアセチル基という小さな化学タグを付与することで知られており、これらのタグがタンパク質の振る舞いを変え得ます。PCAFを欠損するように遺伝子操作したマウスを用い、研究者らは2種類のストレスを心臓に与えました:ストレスホルモンの急増を模す薬剤と、心臓から出る大動脈を締める外科的処置です。正常なマウスでは心筋が肥厚してもポンプ機能は概ね保たれましたが、PCAF欠損マウスでは心室がより拡大し、壁が薄くなり、瘢痕化が増え、駆出機能が低下して、人の拡張型心筋症に近い状態を示しました。
PCAFとエネルギー監視役のつながり
PCAFがどのように保護作用を発揮するかを解明するため、研究者らは細胞のエネルギー供給のバランスを助けるシグナル経路を調べました。この経路の中心には、エネルギー欠乏を感知して細胞の燃料利用を調整するタンパク質AMPKがあります。別のタンパク質であるCAMKK2がAMPKを活性化しますが、心臓におけるCAMKK2自身の制御は明らかではありませんでした。本研究は、PCAFが心細胞内で直接CAMKK2をアセチル化することを示します。このアセチル化によりCAMKK2はAMPKを効率よく働かせる能力が高まり、結果として健全なエネルギー代謝が維持され、ストレス下での有害な過剰成長や筋力低下を防ぐのに寄与します。
助け手が欠けると何が起きるか
PCAF欠損マウスではCAMKK2のアセチル化が減少し、AMPK活性が低下、心細胞の精緻な内部構造、とくにミトコンドリアが悪化しました。ホルモンや圧負荷の下では、これらのPCAF欠損心臓は通常の保護的なエネルギー応答を発揮できませんでした。制御された肥厚の代わりに心室が膨らみ壁が薄くなり、収縮不良と死亡率の上昇を招きました。PCAFを心筋細胞だけで欠損させても同様のパターンが現れ、この保護作用が主に心筋細胞内部での作用によるものであり、心臓内の他の細胞型からの影響だけでは説明できないことを示しました。
心不全を支える新たな可能性
研究者らはPCAF活性を高める小分子SPV106も評価しました。圧負荷を受けたマウスにSPV106を投与すると、心室の拡大や瘢痕化が抑えられ、駆出機能が改善し、同時にCAMKK2およびAMPKの活性が上昇しました。一般向けの要点としては、PCAFは心細胞内のガードスイッチのように働き、ストレス時にエネルギーのバランスと細胞構造を維持するのを助けるということです。このガードが欠けるか弱まると、心臓は伸張し壁が薄くなり心不全に陥りやすくなります。将来的にこのスイッチを穏やかに再活性化する薬や、CAMKK2とAMPKへの効果を模倣する治療は、人々の心臓が心不全へ進行するのを防ぐ手段になり得るかもしれません。
引用: Lim, Y., Jeong, A., Kwon, DH. et al. Loss of p300/CBP-associated factor aggravates cardiac remodeling via regulation of CAMKK2 acetylation. Exp Mol Med 58, 1297–1310 (2026). https://doi.org/10.1038/s12276-026-01698-z
キーワード: 心不全, 心リモデリング, エネルギー代謝, AMPKシグナル, マウスモデル