Clear Sky Science · tr
Söz vaadinden tuzaklara: dang aşılarından immünolojik dersler ve bunların sonuçları
Günlük sağlık açısından neden önemli
Deng ateşi daha fazla ülkeye yayılıyor, ancak hâlâ herkes için tek beden uygun bir aşısı yok. Bu derleme, dang aşısı geliştirmenin neden benzersiz şekilde zor olduğunu, ilk aşıların gerçek dünyada nasıl performans gösterdiğini ve bu deneyimlerin insanları güvenli şekilde koruma konusunda bize neler öğrettiğini açıklıyor. Bu dersleri anlamak yalnızca dengue için değil, ortaya çıkan diğer sivrisinek kaynaklı hastalıklara karşı geliştirilecek gelecekteki aşılar için de önemli.
Dengenin genişleyen kapsama alanı
Deng virüsleri Aedes sivrisinekleri tarafından taşınıyor ve artık 80’den fazla ülkede yılda tahmini yüz milyarlarca enfeksiyona neden oluyor. Pek çok kişide dengue yüksek ateş, döküntü ve eklem ağrısı ile geçen bir haftadır; bazı kişilerde ise ani şekilde ölümcül hâle gelebilir, tehlikeli kanama, sıvı kaçışı ve organ yetmezliği görülebilir. Antiviral ilaç bulunmadığı için halk sağlığı çabaları sivrisinek kontrolüne ve aşılama programlarına dayanıyor. Önemli bir güçlük, dengue’nin dört yakın ilişkili versiyon—serotip—olarak var olması. Bir serotiple enfeksiyon, gelecekte aynı versiyona karşı koruma sağlayabilir, ancak kişi daha sonra farklı bir serotiple karşılaşırsa hastalığı kötüleştirebilir. Bu nedenle başarılı herhangi bir aşı, yanlışlıkla vücudu daha şiddetli hastalığa hazırlamadan aynı anda tüm dört serotipe karşı güçlü ve kalıcı koruma vermelidir.
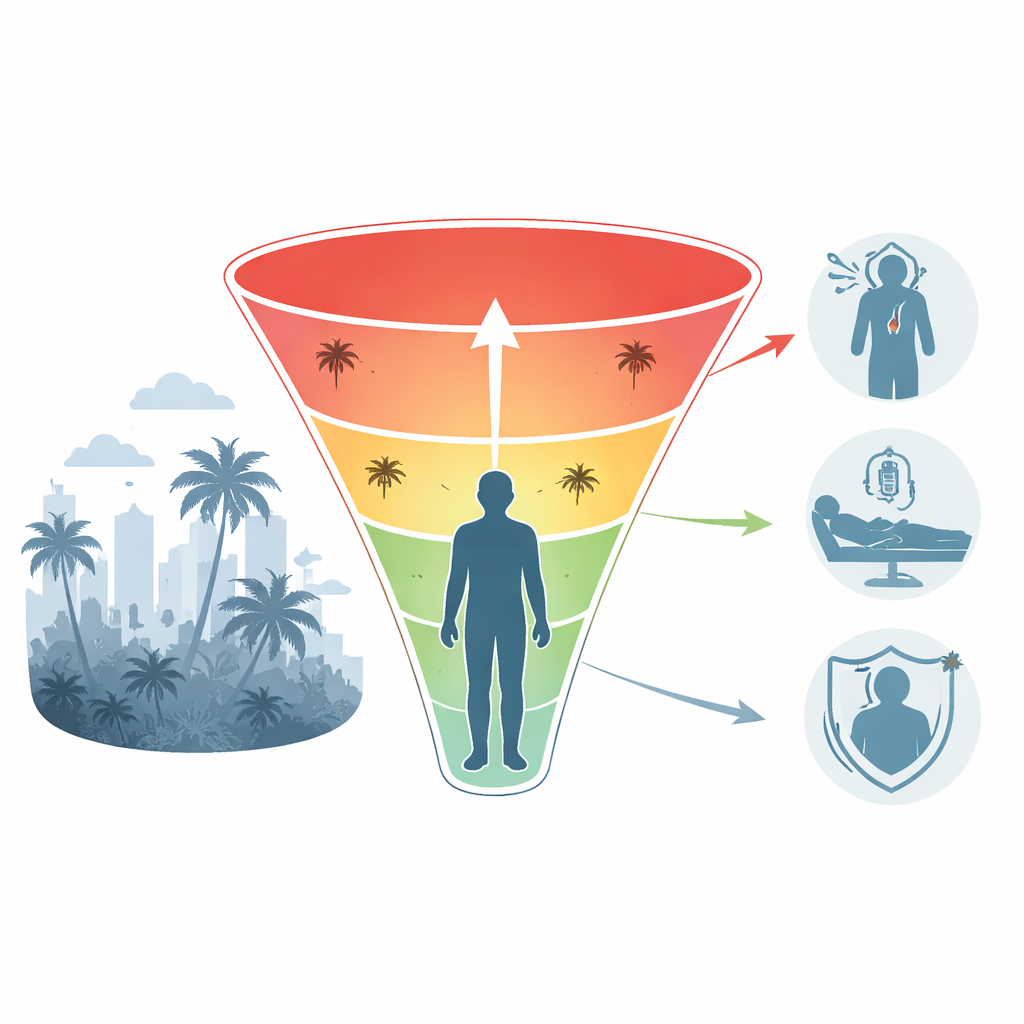
Koruma ile zarar arasındaki ince çizgi
İmmün sistemin dengue’ye yanıtı dar bir çizgide yürüyor. Doğru türde yüksek düzeyde antikorlar virüsü etkili şekilde bloke edebilir. Ancak antikor düzeyleri çok düşükse, zamanla azalıyorsa veya virüsün yanlış bölgelerine odaklanıyorsa, antikorlar dengue’nin bağışıklık hücrelerine daha kolay girmesine ve çoğalmasına yardımcı olabilir; bu olgu güçlenme (enhancement) olarak biliniyor. Önceki dengue veya Zika, sarı humma gibi ilişkili virüslerle temas da tabloyu daha da karmaşıklaştırıyor; çünkü bağışıklık hücreleri ilk enfeksiyon tarafından “izlenimlenebilir” ve ileride yanıtları yanlı hale gelebilir. Sivrisinek tükürüğü de ısırık yerindeki erken bağışıklık tepkilerini aşıların—iğneyle yapılan testlerin—tam olarak yakalayamadığı biçimde değiştiriyor. Birlikte, bu faktörler koruyucu olan bir tarafta ve potansiyel olarak zararlı olan diğer tarafta kalan dar bir immünolojik pencere yaratıyor; bu da dengue aşılarını kızamık veya çocuk felci gibi standart aşılardan çok daha karmaşık hale getiriyor.
Mevcut aşılardan neler öğrendik
Üç büyük tetravalent (dört bir arada) canlı aşı ilerlemeyi ve tuzakları gösteriyor. İlk ruhsatlı ürün olan Dengvaxia, sarı humma iskeletine yerleştirilmiş dengue yüzey proteinlerini kullandı. Genel olarak orta düzeyde koruma gösterdi ancak dört serotip arasında dengesiz çalıştı ve kritik olarak daha önce hiç enfekte olmamış çocuklarda şiddetli dengue riskini artırdı. Bu deneyim sağlık kurumlarını geçmişte dengue geçirdiği doğrulanmış kişilerle sınırlama yapmaya zorladı ve yüksek antikor düzeylerinin tek başına güvenlik veya koruma işareti olmadığını vurguladı. Zayıflatılmış bir dengue-2 virüs iskeletine dayanan daha yeni Qdenga aşısı, T hücrelerini uyaran önemli iç dengue proteinlerini ekliyor ve dengue-naif alıcılarda aynı güvenlik sorunlarını göstermedi. Kısa vadede—özellikle serotip 2’ye karşı—güçlü koruma sağlıyor ve hastaneye yatışları azaltıyor, ancak diğer serotiplere karşı etkinliği birkaç yıl içinde azalma gösteriyor. ABD Ulusal Sağlık Enstitüleri kökenli yapılarla geliştirilen ve Brezilya’da test edilen üçüncü aday Butantan-DV, dört zayıflatılmış dengue suşu kullanıyor ve tek doz sonrası serotip 1 ve 2’ye karşı umut verici koruma gösterdi; hem daha önce maruz kalmış hem de naif gönüllülerde iyi güvenlik sergiledi, ancak serotip 3 ve 4’e karşı gerçek dünya performansının daha uzun takipte ölçülmesi gerekiyor.
Antikor sayılarının ötesinde: gerçekte ne korumayı öngörür
Bu aşılar arasında açık bir mesaj ortaya çıkıyor: Kandaki parçacıkları ne kadar iyi nötralize ettiğini ölçen basit laboratuvar testleri kimin korunacağını tam olarak öngörmüyor. Antikorların kalitesi—virüsün neresine bağlandıkları, ne kadar sıkı tutundukları ve diğer bağışıklık savunmalarını nasıl devreye soktukları—miktarları kadar önem taşıyor. Virüs yüzeyindeki karmaşık yapılara yönelik yanıtlar genellikle daha geniş koruma sağlar ve enfeksiyonu güçlendirme olasılığı daha düşüktür. Aynı zamanda iç viral proteinlere karşı güçlü T hücre yanıtları, enfekte hücreleri temizlemeye yardımcı olur ve antikor düzeyleri doğal olarak azaldıkça korumayı sürdürebilir. Yazarlar, gelecekteki dengue aşıları ve çalışmalarının tek bir sayıya dayanmak yerine nötralizasyon genişliği, antikor gücü, hafıza B hücreleri ve T hücre fonksiyonu dahil bileşik bir belirteç setini takip etmesi gerektiğini savunuyor. Ayrıca doğal sivrisinek bulaşmasını daha iyi taklit eden ve insanların diğer flavivirüslere önceki maruziyetini hesaba katan deneyler ve challenge çalışmaları yapılması çağrısında bulunuyorlar.
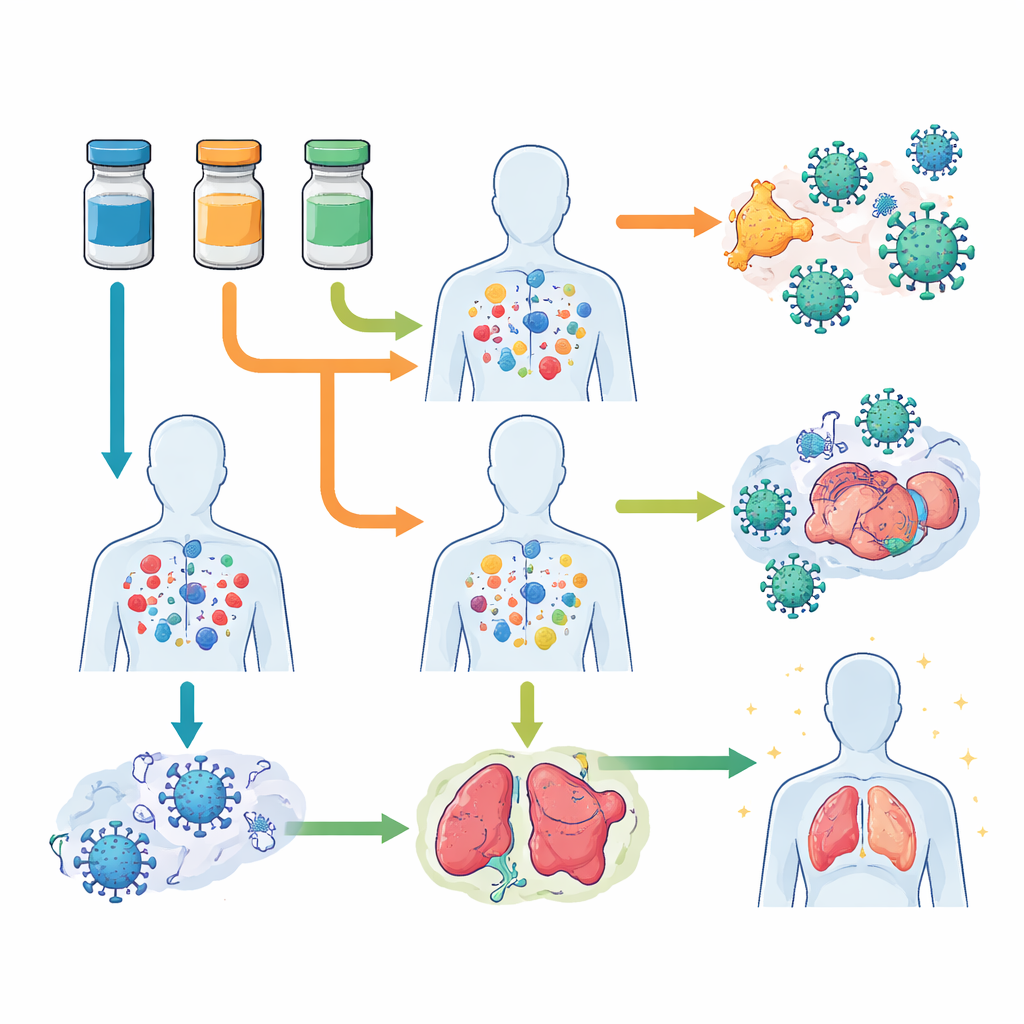
Daha güvenli ve uzun süreli korumaya bakış
Derleme, etkili dengue aşılamanın mümkün olduğunu ancak bunun çoğu mevcut aşıların gerektirdiğinden daha sofistike, öngörücü bir bağışıklık sistemi anlayışı gerektirdiğini sonucuna varıyor. Yeni nesil yaklaşımlar, canlı-attenüe virüsleri mRNA, viral vektörler ve sadece enfeksiyonu değil viral proteinlerin hastalığa yol açan etkilerini de hedefleyen subunit aşılar gibi daha yeni platformlarla harmanlayabilir. Dengvaxia, Qdenga ve Butantan-DV’nin hem başarılarından hem de aksaklıklarından öğrenerek bilim insanları, önceki enfeksiyona bakılmaksızın güvenli, dengeli ve tüm dört dengue serotipine karşı uzun süreli koruma sağlayan; en çok ihtiyaç duyulan bölgelerde geniş çapta kullanılabilecek aşılar tasarlamayı amaçlıyor.
Atıf: Estofolete, C.F., Saivish, M.V., Nogueira, M.L. et al. From promise to pitfalls: immunological lessons from dengue vaccines and their implications. npj Vaccines 11, 68 (2026). https://doi.org/10.1038/s41541-026-01400-4
Anahtar kelimeler: deng aşıları, antikor-bağımlı güçlenme, tetravalent canlı aşılar, sivrisinek kaynaklı virüsler, aşı immünolojisi