Clear Sky Science · sv
Från löften till fallgropar: immunologiska lärdomar från dengue-vacciner och deras konsekvenser
Varför detta är viktigt för vardagshälsan
Denguefeber sprider sig till fler länder, men vi har fortfarande inget enkelt, universellt vaccin. Denna översikt förklarar varför det är särskilt svårt att ta fram ett denguevaccin, hur de första vaccinerna har fungerat i verkligheten och vad dessa erfarenheter lär oss om att skydda människor på ett säkert sätt. Att förstå dessa lärdomar är viktigt inte bara för dengue utan också för framtida vacciner mot andra framväxande myggöverförda sjukdomar.
Dengues växande utbredning
Denguevirus sprids av Aedes-myggor och orsakar nu uppskattningsvis hundratals miljoner infektioner varje år i mer än 80 länder. Hos många människor innebär dengue en vecka med hög feber, utslag och värk i lederna; hos andra kan sjukdomen plötsligt bli livshotande med farliga blödningar, vätskeläckage och organsvikt. Det finns inga antivirala läkemedel, så folkhälsoinsatser förlitar sig på myggbekämpning och vaccination. En stor komplikation är att dengue förekommer i fyra nära besläktade varianter, eller serotyper. En infektion med en serotyp kan skydda mot just den varianten i framtiden, men kan faktiskt förvärra sjukdomen om en person senare utsätts för en annan serotyp. Ett framgångsrikt vaccin måste därför ge starkt och varaktigt skydd mot alla fyra samtidigt, utan att oavsiktligt förbereda kroppen för svårare sjukdom.
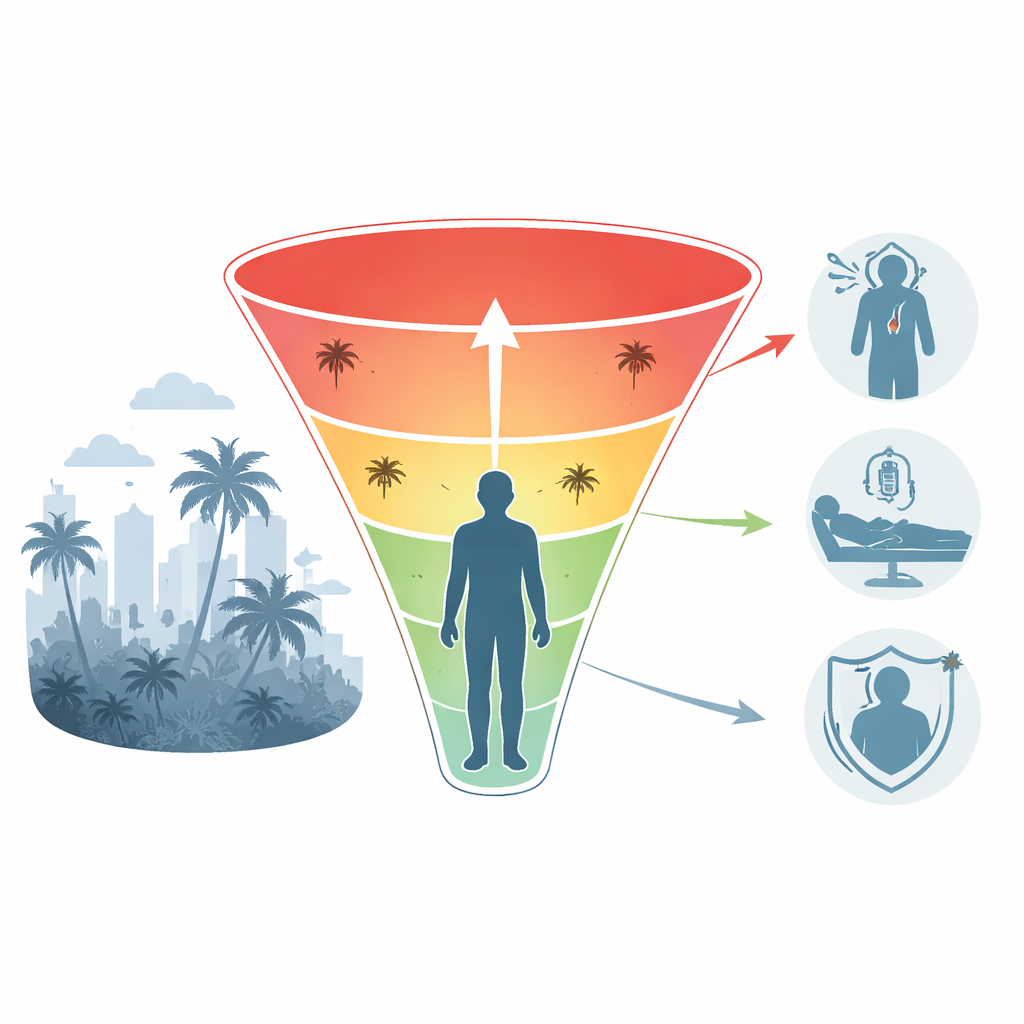
En balansakt mellan skydd och skada
Immunsystemets svar på dengue går på en smal lina. Höga nivåer av rätt slags antikroppar kan effektivt blockera viruset. Men om antikroppsnivåerna är för låga, avtar över tid eller riktas mot fel delar av viruset kan de hjälpa dengue att ta sig in i immunceller lättare och föröka sig — ett fenomen känt som förbättring (enhancement). Tidigare exponering för dengue eller närbesläktade virus som zikavirus och gula febern komplicerar bilden ytterligare, eftersom immunceller kan bli ”präglade” av den första infektionen och senare svara på ett snedvridet sätt. Myggsaliv i sig förändrar också de tidiga immunreaktionerna vid bettstället på sätt som de flesta vaccinprövningar — gjorda med nålinjektioner — inte fullt ut fångar. Tillsammans skapar dessa faktorer ett smalt immunologiskt fönster där svaren är skyddande åt ena hållet och potentiellt skadliga åt andra, vilket gör denguevacciner mycket mer komplexa än standardvacciner som mässling eller polio.
Vad vi lärt oss av nuvarande vacciner
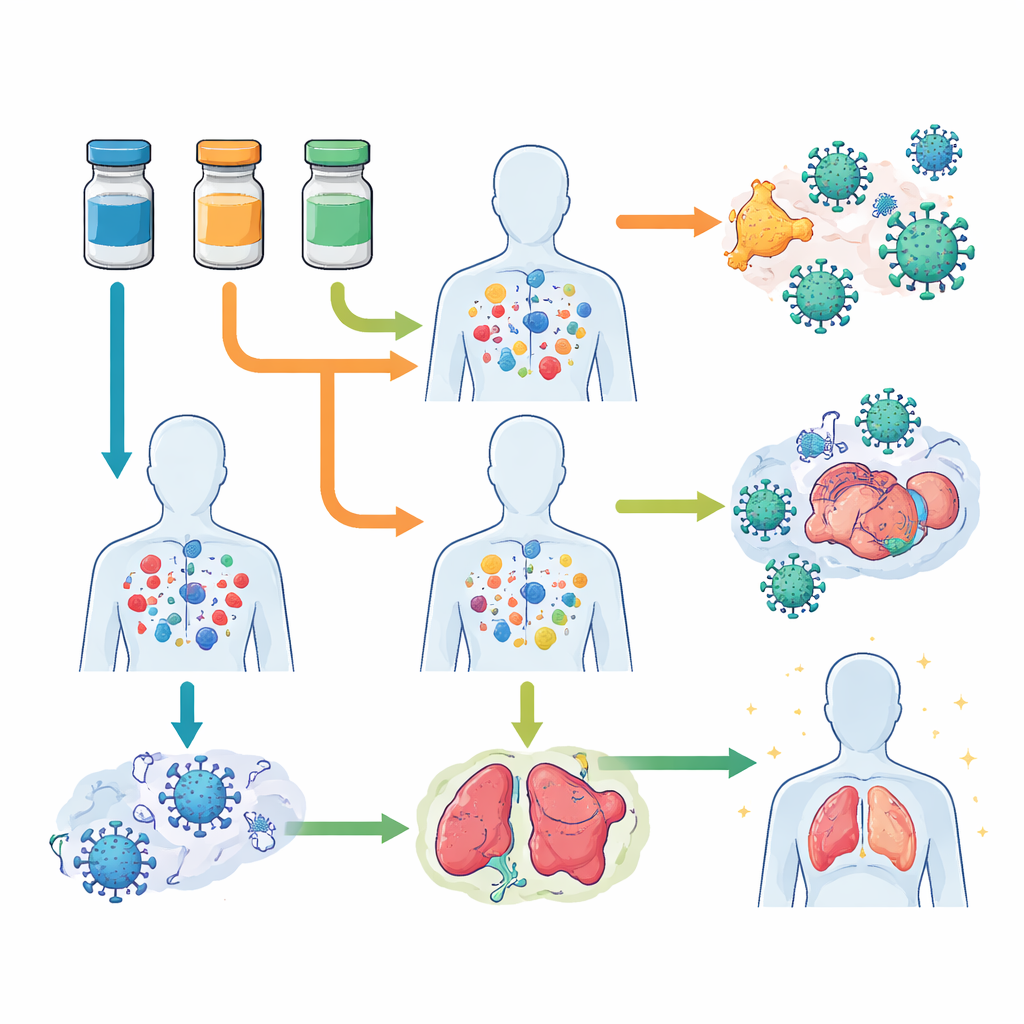
Tre stora tetravalenta (fyra-i-ett) levande vacciner illustrerar både framsteg och fallgropar. Dengvaxia, den första godkända produkten, använde en ryggrad från gula febern med dengues ytantigen. Den visade måttligt skydd totalt sett men fungerade ojämnt mot de fyra serotyperna och, avgörande nog, ökade risken för svår dengue hos barn som aldrig tidigare varit infekterade. Den erfarenheten tvingade hälsomyndigheter att begränsa dess användning till personer med bekräftad tidigare dengue och betonade att höga antikroppsnivåer inte ensamt är en tillförlitlig signal för säkerhet eller skydd. Det nyare vaccinet Qdenga, byggt på en försvagad dengue-2-ryggrad, inkluderar viktiga interna dengueproteiner som stimulerar T-celler och har inte visat samma säkerhetsproblem hos denguenativa mottagare. Det erbjuder starkt korttidsskydd — särskilt mot serotyp 2 — och minskar sjukhusinläggningar, men dess effekt mot andra serotyper avtar över flera år. En tredje kandidat, Butantan-DV, härledd från konstrukter från U.S. National Institutes of Health och testad i Brasilien, använder fyra försvagade denguestammar och har visat lovande skydd mot serotyperna 1 och 2 efter en enda dos, med god säkerhet både hos tidigare exponerade och naiva frivilliga, även om dess verkliga prestanda mot serotyperna 3 och 4 ännu kräver längre uppföljning.
Bortom antikroppsräkning: vad som verkligen förutsäger skydd
I dessa vacciner framträder ett tydligt budskap: enkla laboratorietester som mäter hur väl blod neutraliserar viruspartiklar förutsäger inte fullt ut vem som kommer att vara skyddad. Antikropparnas kvalitet — var på viruset de binder, hur starkt de fäster och hur de rekryterar andra immunförsvar — är lika viktig som deras kvantitet. Svar som riktar sig mot komplexa strukturer på virusytan tenderar att vara mer brett skyddande och mindre benägna att förbättra infektion. Samtidigt hjälper robusta T-cellssvar mot interna viralproteiner till att rensa infekterade celler och kan upprätthålla skydd när antikroppsnivåerna naturligt sjunker. Författarna menar att framtida denguevacciner och prövningar måste följa en sammansatt uppsättning markörer, inklusive neutraliseringsbredd, antikroppsstyrka, minnes B‑celler och T‑cellsfunktion, snarare än att förlita sig på ett enda tal. De kräver också experiment och utmaningsstudier som bättre efterliknar naturlig myggöverföring och tar hänsyn till människors tidigare exponering för andra flavivirus.
Framåtblick mot säkrare och mer långvarigt skydd
Översikten avslutar att medan effektiv denguevaccination är möjlig kräver den en mer sofistikerad, förutsägbar förståelse av immunsystemet än vad de flesta nuvarande vacciner kräver. Nästa generations tillvägagångssätt kan kombinera levande försvagade virus med nyare plattformar såsom mRNA, virusvektorer och subenhetsvacciner som riktar sig inte bara mot infektion utan också mot de sjukdomsframkallande effekterna av viralproteiner. Genom att lära av både framgångarna och bakslagen med Dengvaxia, Qdenga och Butantan‑DV strävar forskare efter att utforma vacciner som ger balanserat, långvarigt skydd mot alla fyra dengueserotyper, är säkra oavsett tidigare infektion och kan användas i stor skala i de regioner som behöver dem mest.
Citering: Estofolete, C.F., Saivish, M.V., Nogueira, M.L. et al. From promise to pitfalls: immunological lessons from dengue vaccines and their implications. npj Vaccines 11, 68 (2026). https://doi.org/10.1038/s41541-026-01400-4
Nyckelord: denguevacciner, antikroppsberoende förbättring, tetravalenta levande vacciner, myggöverförda virus, vaccineimmunologi