Clear Sky Science · tr
Sentezlenmiş nöron-astrosit etkileşimleriyle sinaptik bağlantıların yeniden düzenlenmesi
Beyin bağlantılarını değiştirmek neden önemli
Beynimiz, sinaps adı verilen trilyonlarca küçük bağlantıyla donatılmıştır; bu bağlantılar sinir hücrelerinin birbirine sinyal ilettiği noktalardır. Bu bağlantılar bir devre kartı gibi sabit değildir; sürekli olarak güçlenir, zayıflar, eklenir veya kaldırılır. Bu kablolamadaki ince dengesizliklerin otizmden Alzheimer hastalığına kadar birçok beyin bozukluğunun temelinde olduğu düşünülüyor. Ancak bilim insanlarının, aktiviteyi basitçe artırıp azaltmadan sinaptik bağlantıları seçici olarak yeniden şekillendirebilecek fazla hassas aracı yoktu. Bu çalışma, beynin kendi destek hücreleri aracılığıyla sinapsları nazikçe “düzenleyen” sentetik biyolojik bir yöntemi tanıtıyor; devrelerin nasıl daha seyrek ama daha esnek hale gelebileceğini ve bunun bir gün terapide nasıl kullanılabileceğini gösteriyor. 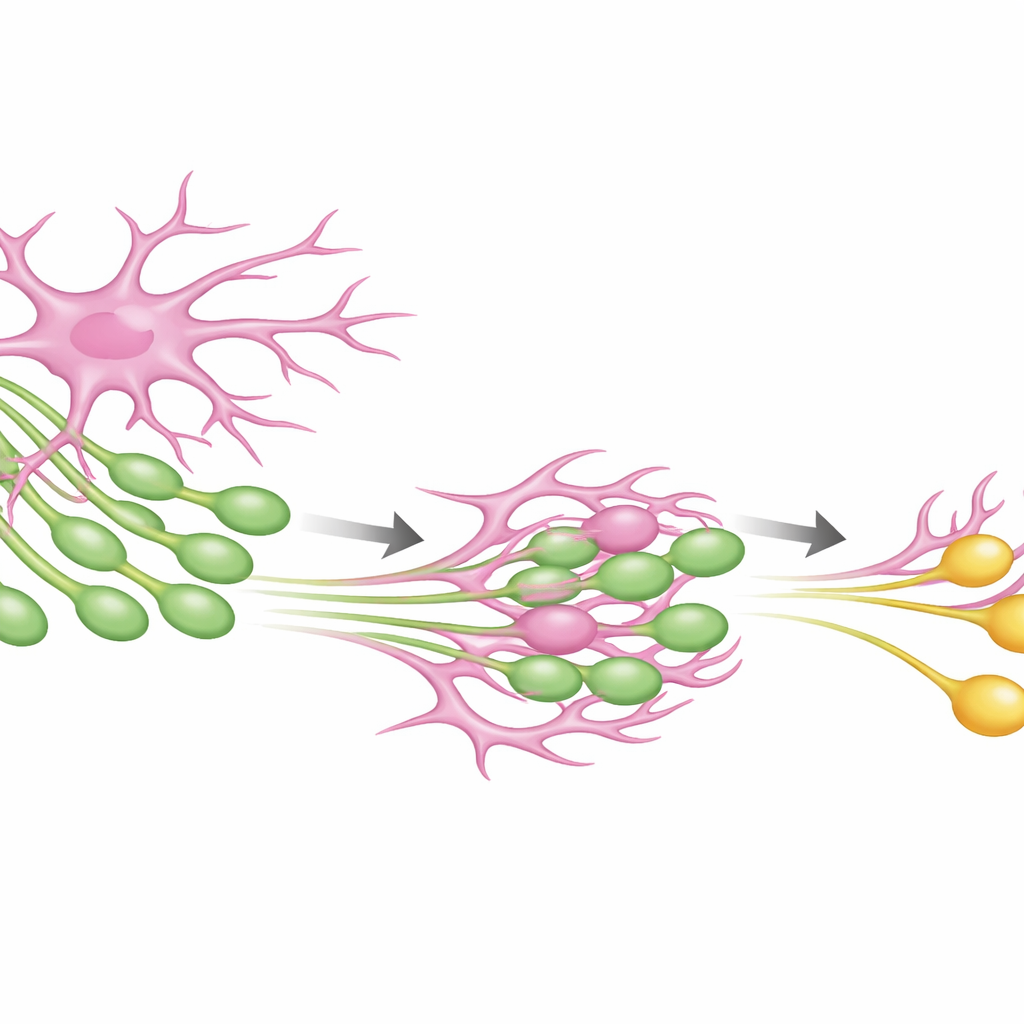
Beyin hücrelerini birbirine değdirmenin yeni bir yolu
Yazarlar, seçilmiş hücrelerin çok sıkı bir şekilde birbirine yapışmasını sağlayan yapay bir “civata” sistemi geliştirdiler. Bir hücre türünde “tutamaç” olarak bilinen, iyi bilinen parlak bir protein olan GFP’yi; diğer hücre türünde ise GFP’yi yakalayan küçük antikor benzeri bir partneri (nanobody) “kanca” olarak kullandılar. Her iki parça da hücre yüzeyine sabitlendi; böylece GFP taşıyan bir hücre, nanobody taşıyan bir komşuyla karşılaştığında membranları kilitleniyordu. Laboratuvar kaplarında bu güçlü temas, reseptör taşıyan hücrenin partnerin membranından ve yakın içeriğinden küçük yamalar koparıp içselleştirmesiyle sonuçlanan trogotitoz benzeri bir süreci tetikledi. İki mühendislik ürünü protein arasındaki moleküler kavrama ne kadar güçlü olursa, bu küçük parçaların alınması o kadar verimli gerçekleşti ve süreç birçok hücre türünde hücreleri öldürmeden çok yönlü biçimde çalıştı.
Nöronları kemiren beyin destek hücrelerini görevlendirmek
Araştırmacılar ardından doğal olarak sinapsların etrafını saran ve istenmeyen bağlantıları kaldırmaya yardımcı olan yıldız şekilli destek hücreler olan astrositlere yöneldi. Nöronlarda GFP “ligandını”, astrositlerde ise nanobody “reseptörünü” ifade ettiler. Kültürdeki nöronlarda astrositler, uzantıları aksonlara, dendritlere veya hücre gövdelerine değdiği her yerde nöronal membrandan küçük parçaları tekrar tekrar kopardı. Önemli olarak, GFP etiketinin yakınındaki sinaptik proteinler de astrositlerle birlikte çekilerek içselleştirildi; bu, mühendislik ürünü etkileşimin sinaptik materyali nöronlardan seçici olarak uzaklaştırabileceğini gösterdi. Bu, SynTrogo (Sentetik Trogotitoz) olarak adlandırılan sentetik sistemin astrositlerin nöronal bağlantılarla ne kadar yakın etkileşime girdiğini ve hangi hücresel yükleri aldığını yönlendirebileceğini doğruladı.
Bir bellek devresindeki bağlantıları inceltmek
SynTrogo’nun yaşayan beyinde ne yaptığını görmek için araştırmacılar fare hipokampusundaki klasik bir bellek yolunu hedef aldı; burada CA3 nöronları CA1 nöronlarına bağlanır. GFP tutamaç CA3 aksonlarına, nanobody reseptör ise CA1 astrositlerine kondu. Bu koşullar altında CA3 aksonlarından gelen floresan sinyalin astrositik alanlar içinde biriktiği gözlendi; bu, aktif kemirmeyi gösteriyordu. Nanometre çözünürlüğünde mikroskopi, astrosit membranlarının presinaptik butonlarla olağandışı derecede sıkı, birbirine geçtiği arayüzler oluşturduğunu gösterdi; bazen veziküller ve diğer organeller içeren akson parçalarını kısmen sarıyorlardı. Bu yol boyunca eksitatör sinapsların yoğunluğu yaklaşık dörtte bir oranında azaldı, özellikle mühendislik ürünü astrositlerin bulunduğu yerlerde; buna karşılık inhibitör bağlantılar ılımlı şekilde arttı — CA1 üzerindeki girişlerin dengesini aksiyon potansiyellerini yok etmeden değiştirdi.
Daha güçlü kalanlar ve daha uyumlu devreler
Sürpriz bir şekilde, bu budamadan sonra kalan sinapslar zayıflamamıştı. Elektriksel kayıtlarda genel olarak daha az eksitatör olay görüldü; bu, sinaps sayısındaki azalmayla uyumluydu — fakat kalan presinaptik terminaller nörotransmiteri daha kolay saldı ve daha büyük bir hazır salınabilir vezikül havuzuna sahipti. Üç boyutlu yeniden yapılandırmalar, hayatta kalan butonların daha büyük olduğunu, daha fazla sinaptik vezikül ve mitokondri içerdiğini ve genişletilmiş temas alanlarına sahip büyümüş postsinaptik dikenlerle karşılaştığını ortaya koydu. Bu dikenlerin birçoğu kalsiyum yönetimi ve reseptör trafiği ile ilişkili özel bir iç yapı olan diken aparatını edindi. İşlevsel olarak, bu yeniden şekillenmiş ağ sinaptik plastisitenin bir göstergesi olan daha güçlü uzun süreli potansiyasyon sergiledi ve fareler bağlamsal korku belleği testlerinde daha iyi performans gösterdi; anıları daha uzun süre korudular, aynı zamanda eğitimle söndürmeyi sürdürebildiler. 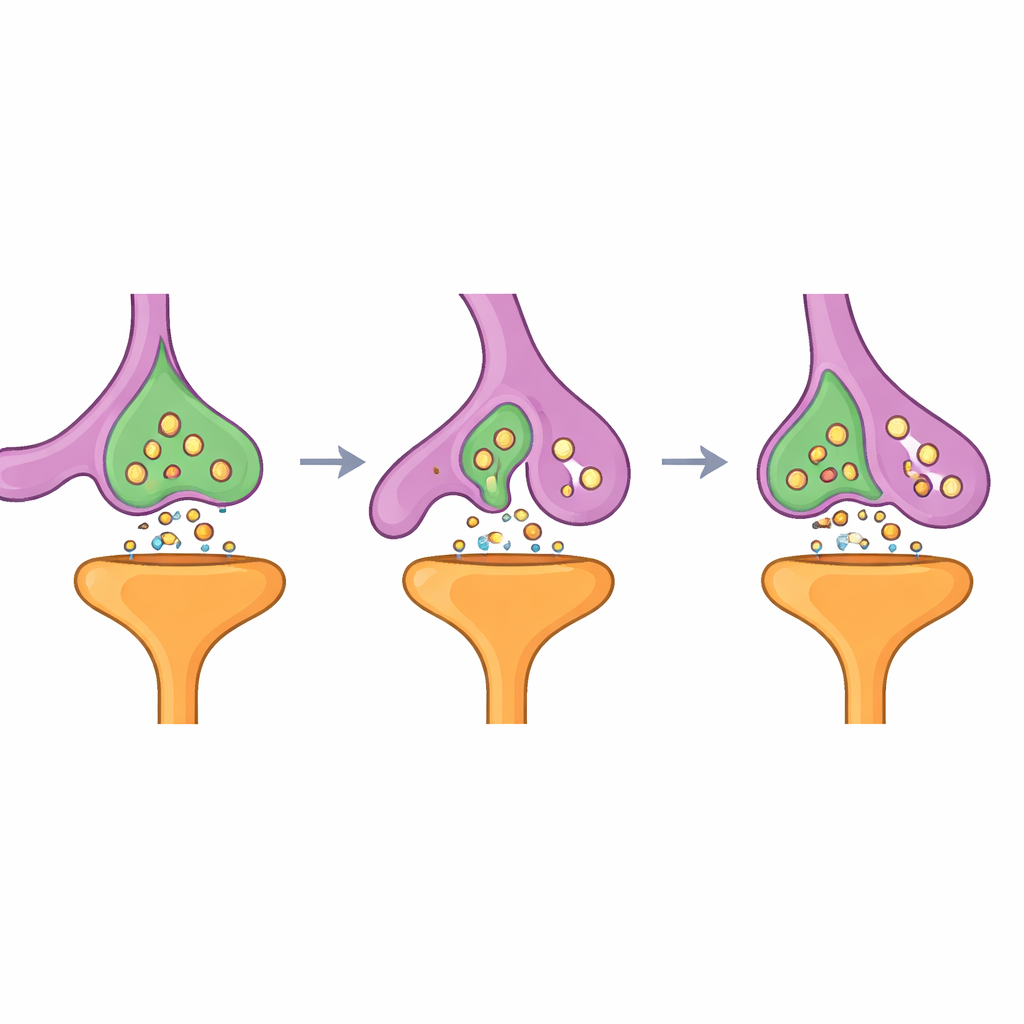
Bu, beyin sağlığı için ne anlama gelebilir
Bir uzman olmayan kişi için ana mesaj şudur: bir devredeki sinaps sayısını dikkatli bir şekilde azaltmak zorunlu olarak beyin fonksiyonunu köreltmez; aslında onu keskinleştirebilir. SynTrogo, astrositleri belirli nöronal bağlantıları seçici olarak kemirmeye yönlendirerek bağlantıları inceltmenin ve hayatta kalan sinapsların daha güçlü ve daha uyumlu hale gelmesini sağlamanın mümkün olduğunu gösteriyor. Bu sentetik yaklaşım, yapısal yeniden kablolamayı basit elektriksel aktivite değişikliklerinden ayırıyor ve devre mimarisinin öğrenme, bellek ve dayanıklılığı nasıl şekillendirdiğini incelemek için güçlü yeni bir yol sunuyor. Uzun vadede, SynTrogo’dan ilham alan stratejiler, otizm, şizofreni veya erken Alzheimer hastalığı gibi durumlarda aşırı yoğun veya düzensiz bağlantıları yeniden dengelemeye yardımcı olabilir; kontrollü sinaps kaybını daha sağlıklı devre onarımları için bir fırsata çevirebilir.
Atıf: Kim, S.H., Won, W., Kim, G.H. et al. Remodeling synaptic connections via engineered neuron-astrocyte interactions. Nat Commun 17, 3490 (2026). https://doi.org/10.1038/s41467-026-71440-w
Anahtar kelimeler: sinaptik budama, astrositler, nöral plastisite, sentetik biyoloji, hipokampus