Clear Sky Science · de
Umgestaltung synaptischer Verbindungen durch konstruierte Neuron-Astrozyten-Interaktionen
Warum das Verändern von Hirnverbindungen wichtig ist
Unser Gehirn ist durch Billionen winziger Verbindungen, so genannter Synapsen, verdrahtet, an denen Nervenzellen Signale aneinander weitergeben. Diese Verbindungen sind nicht starr wie eine Leiterplatte; sie werden ständig verstärkt, geschwächt, hinzugefügt oder entfernt. Feine Ungleichgewichte in dieser Verdrahtung gelten als Ursache vieler Gehirnerkrankungen, von Autismus bis Alzheimer. Forscher hatten jedoch nur wenige präzise Werkzeuge, um synaptische Verbindungen selektiv umzubauen, ohne einfach nur die Aktivität hoch- oder runterzufahren. Diese Studie stellt eine Methode der synthetischen Biologie vor, mit der Synapsen über die eigenen Stützzellen des Gehirns behutsam „korrigiert“ werden können. Sie zeigt, wie Schaltkreise schlanker und zugleich flexibler werden können — und wie sich dies eines Tages therapeutisch nutzen lassen könnte. 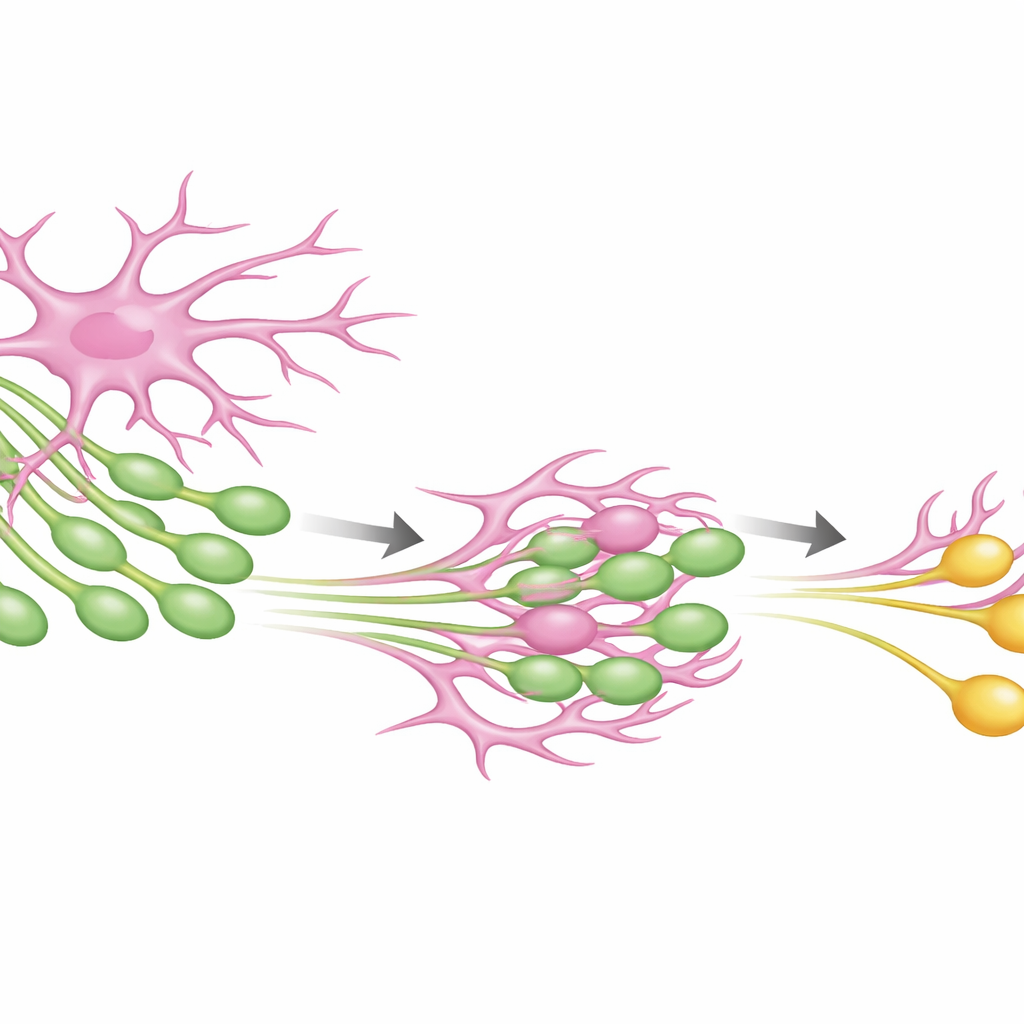
Ein neuer Weg, Gehirnzellen zusammenzubringen
Die Autoren entwickelten ein künstliches „Klett“-System, das ausgewählte Zellen sehr fest aneinander haften lässt. Sie verwendeten ein bekanntes Leuchtprotein, GFP, als „Griff“ auf einem Zelltyp und einen winzigen, Antikörper-ähnlichen Partner (eine Nanobody), der GFP greift, als „Haken“ auf dem anderen Zelltyp. Beide Teile wurden an Zelloberflächen verankert, sodass die Membranen verriegelten, wenn eine GFP-tragende Zelle auf eine Nanobody-tragende Nachbarin traf. Im Reagenzglas löste dieser starke Kontakt einen Prozess aus, der der Trogocytose ähnelte — eine Art zelluläres Nagen — bei dem die Rezeptor-tragende Zelle kleine Membranabschnitte des Partners abknipste und internalisierte sowie nahegelegene Inhalte mitnahm. Je stärker der molekulare Griff zwischen den beiden konstruierten Proteinen war, desto effizienter verlief dieses Nagen, und der Prozess erwies sich als vielseitig über viele Zelltypen hinweg, ohne die Zellen abzutöten.
Astrozyten zum Neuronen-Nagen einsetzen
Das Team wandte sich dann Astrozyten zu, sternförmigen Stützzellen, die sich natürlicherweise um Synapsen legen und helfen, unerwünschte Verbindungen zu entfernen. Sie exprimierten das GFP‑„Ligand“ in Neuronen und den Nanobody‑„Rezeptor“ in Astrozyten. In kultivierten Neuronen nagten Astrozyten wiederholt winzige Stücke neuronaler Membran ab, überall dort, wo ihre Fortsätze Axone, Dendriten oder Zellkörper berührten. Wichtig war, dass synaptische Proteine in der Nähe des GFP‑Tags mit in die Astrozyten hineingezogen wurden, was zeigt, dass die konstruierte Interaktion selektiv synaptisches Material von Neuronen wegziehen kann. Das bestätigte, dass das synthetische System — SynTrogo, für Synthetic Trogocytosis — steuern kann, wie eng Astrozyten mit neuronalen Verbindungen interagieren und welche zellulären Frachtstoffe sie aufnehmen.
Verbindungen in einer Gedächtnisschleife ausdünnen
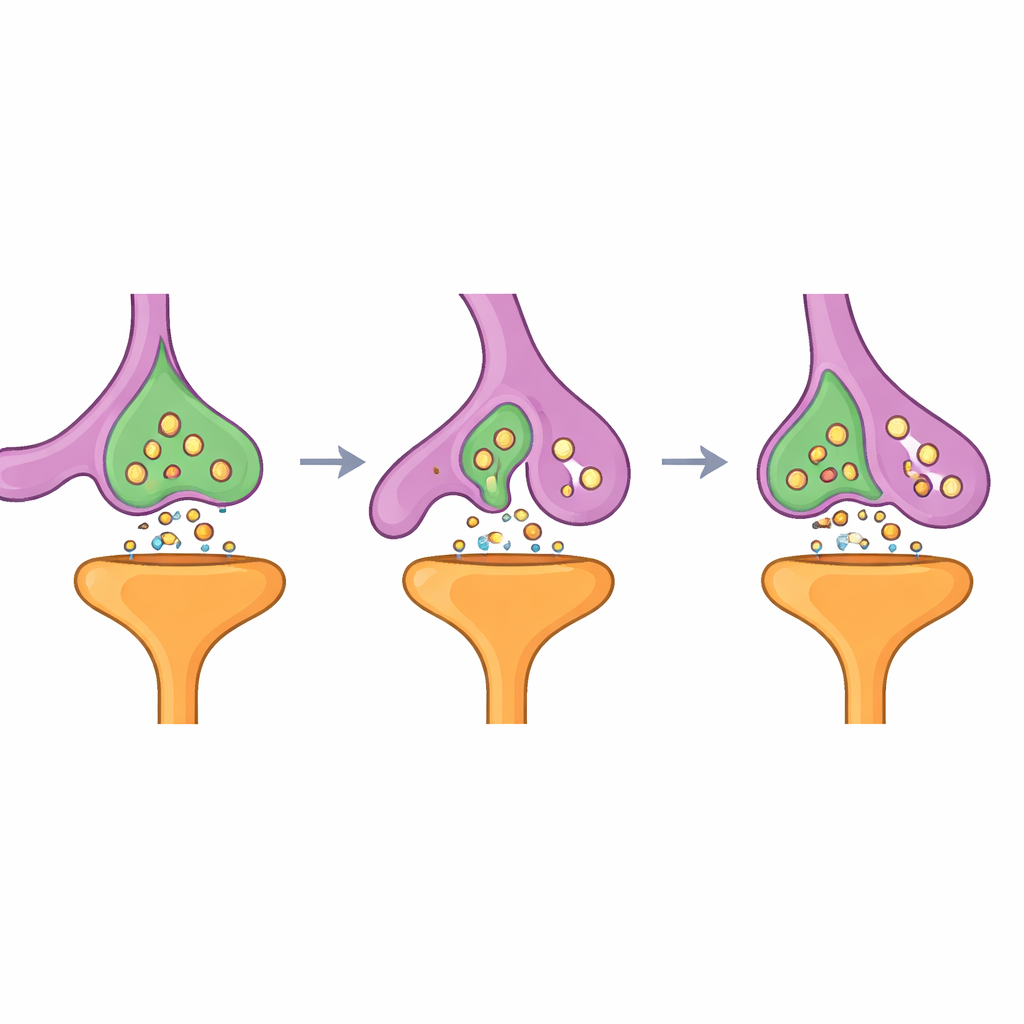
Um zu untersuchen, was SynTrogo im lebenden Gehirn bewirkt, richteten die Forschenden ihr System auf einen klassischen Gedächtnispfad im Maus‑Hippokampus, wo CA3‑Neurone mit CA1‑Neuronen verbunden sind. Sie brachten den GFP‑Griff an CA3‑Axonen an und den Nanobody‑Rezeptor an CA1‑Astrozyten. Unter diesen Bedingungen häufte sich das fluoreszente Signal von CA3‑Axonen in astrozytären Territorien an, was auf aktives Nagen hinwies. Mikroskopie im Nanometerbereich zeigte, dass Astrozytenmembranen ungewöhnlich enge, ineinandergreifende Schnittstellen mit präsynaptischen Boutons bildeten und dabei manchmal Teile des Axons teilweise umschlossen, die Vesikel und andere Organellen enthielten. Entlang dieses Pfades sank die Dichte exzitatorischer Synapsen um etwa ein Viertel, insbesondere dort, wo die konstruierten Astrozyten vorhanden waren, während inhibitorische Verbindungen leicht zunahmen — wodurch sich das Eingangsverhältnis an CA1‑Neuronen änderte, ohne die Axone vollständig zu zerstören.
Stärkere Überlebende und anpassungsfähigere Schaltkreise
Überraschenderweise waren die Synapsen, die nach diesem Beschneiden übrigblieben, nicht schwächer. Elektrische Aufzeichnungen zeigten insgesamt weniger exzitatorische Ereignisse, was der reduzierten Synapsenzahl entsprach, doch die verbleibenden präsynaptischen Terminals setzten Neurotransmitter leichter frei und verfügten über einen größeren sofort freisetzbaren Vesikelpool. Dreidimensionale Rekonstruktionen enthüllten, dass überlebende Boutons größer waren, dichter mit synaptischen Vesikeln und Mitochondrien gepackt und größeren postsynaptischen Dornen gegenüberstanden, die erweiterte Kontaktzonen aufwiesen. Viele dieser Dornen erhielten eine spezialisierte Innenstruktur, das Spine‑Apparat, das mit Kalziumhandling und Rezeptortransport in Zusammenhang steht. Funktionell zeigte dieses umgebaute Netzwerk stärkere Langzeitpotenzierung, ein Kennzeichen synaptischer Plastizität, und die Mäuse schnitten in kontextuellen Furchtgedächtnis‑Tests besser ab, behielten Erinnerungen länger, konnten sie aber durch Training dennoch löschen.
Was das für die Gehirngesundheit bedeuten könnte
Für Nichtfachleute lautet die Kernbotschaft: Eine kontrollierte Reduktion der Anzahl von Synapsen in einem Schaltkreis muss die Gehirnfunktion nicht dämpfen; sie kann sie sogar schärfen. SynTrogo zeigt, dass man, indem man Astrozyten anleitet, selektiv an bestimmten neuronalen Kontakten zu nagen, Verbindungen ausdünnen kann, während die überlebenden Synapsen stärker und flexibler werden. Dieser synthetische Ansatz trennt strukturelles Umbauen von einfachen Veränderungen der elektrischen Aktivität und bietet eine mächtige neue Möglichkeit, zu untersuchen, wie Architektur von Schaltkreisen Lernen, Gedächtnis und Resilienz formt. Langfristig könnten von SynTrogo inspirierte Strategien helfen, übermäßig dichte oder desorganisierte Verbindungen bei Erkrankungen wie Autismus, Schizophrenie oder frühem Alzheimer wieder ins Gleichgewicht zu bringen und kontrollierten Synapsenverlust als Chance für gesünderes Schaltkreis‑Remodelling zu nutzen.
Zitation: Kim, S.H., Won, W., Kim, G.H. et al. Remodeling synaptic connections via engineered neuron-astrocyte interactions. Nat Commun 17, 3490 (2026). https://doi.org/10.1038/s41467-026-71440-w
Schlüsselwörter: synaptisches Pruning, Astrozyten, neurale Plastizität, synthetische Biologie, Hippokampus