Clear Sky Science · sv
Molekylär målinriktning av meningiomcellernas signaleringskrets avslöjar läkemedelssårbarheter inklusive synergi mellan sulforafan och hämmning av fokal adhesionskinas
Varför detta är viktigt för patienter med hjärntumör
Meningiom är bland de vanligaste hjärntumörerna och även om många formellt är "benigna" kan deras läge inuti skallen ändå orsaka allvarliga funktionsnedsättningar. För de flesta patienter är de enda verkliga alternativen kirurgi och strålning, båda med risker och som inte alltid förhindrar att tumörer återkommer. Denna studie undersöker om redan tillgängliga eller experimentella läkemedel kan rikta in sig på meningiomcellernas inre kontrollkretsar, vilket öppnar möjligheten för mildare, läkemedelsbaserade behandlingar som kan komplettera eller en dag delvis ersätta kirurgi.
Att bygga en realistisk laboratoriemodell av tumören
För att undersöka nya behandlingar behövde forskarna först ett labsystem som beter sig som verkliga patienttumörer. De samlade vävnad från tre personer som opererades för grad I eller II meningiom och odlade cellerna i skålar under många veckor. Varje patients celler visade distinkt form och tillväxtmönster, men alla expanderade stadigt i tidiga passager innan de avmattades senare. Teamet bekräftade att dessa kulturer verkligen representerade meningiomvävnad genom att kontrollera för proteiner som vanligtvis finns i dessa tumörer men inte i normala nasala fibroblaster. Denna levande modell gjorde det möjligt att testa hur olika läkemedel påverkar tumörcellernas överlevnad på ett kontrollerat, reproducerbart sätt.
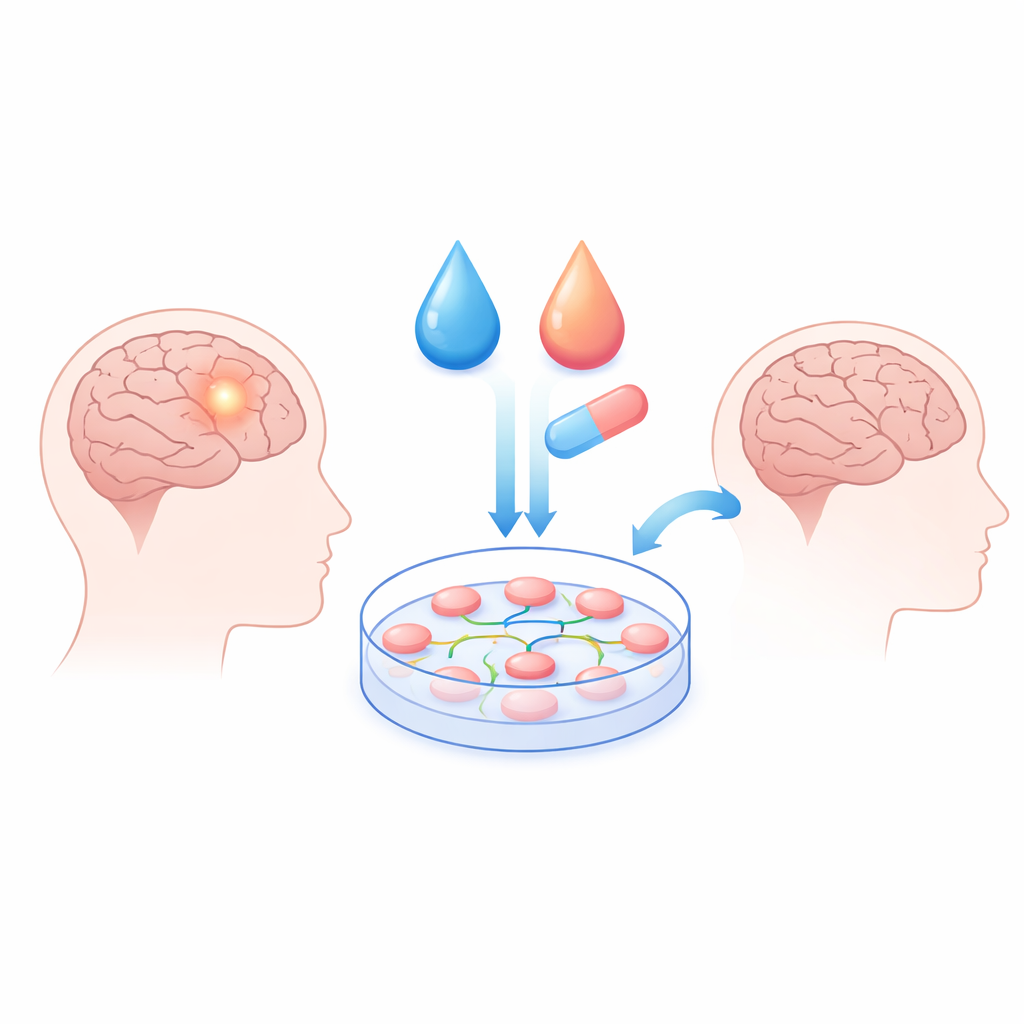
Att slå mot tumörens signalerings"kabeldragning"
Meningiomceller bär ofta skador i en gen som heter NF2, vilken producerar ett protein (Merlin) som normalt håller flera tillväxt- och överlevnadsvägar i schack. När denna broms sviktar kan flera signalvägar—kopplade till inflammation, tillväxtfaktorer och cellfästning—driva tumörtillväxt. Istället för att jaga en ensam mutation riktade författarna in sig på nyckelpunkter längs detta sammankopplade nätverk. De testade ett panel av läkemedel valda för sin förmåga att störa dessa vägar, inklusive ett diabetesläkemedel (metformin), en naturlig förening från korsblommiga grönsaker (sulforafan) samt hämmare av fokal adhesionskinas (FAK) och STAT3, molekyler som hjälper till att förmedla pro-tillväxt- och pro-inflammatoriska signaler inne i cellen.
Att hitta svaga punkter och kraftfulla kombinationer
I initiala skriningar minskade alla testade läkemedel meningiomcellernas livskraft i viss mån, men flera utmärkte sig som konsekvent effektiva över samtliga tre patienthärledda kulturer. Sulforafan, metformin, FAK-hämmaren Y15 och STAT3-hämmaren C188-9 visade var och en tydlig, dosberoende dödlighet på tumörcellerna. Forskarna fokuserade därefter på kombinationer, med tanken att koordinerade angrepp på olika noder i signaleringskretsen kunde vara mer potenta och tillåta lägre doser. Med standardanalys för synergi upptäckte de att sulforafan plus Y15 bildade ett särskilt kraftfullt par: varje läkemedel blev effektivt vid lägre koncentrationer när de användes tillsammans, och deras gemensamma påverkan på cellöverlevnad var större än summan av deras individuella effekter. Mikroskopi visade att denna duo minskade markörer för celldelning och ökade markörer för programmerad celldöd, vilket tyder på en verklig avstängning av tumörcellstillväxt snarare än en tillfällig avmattning.
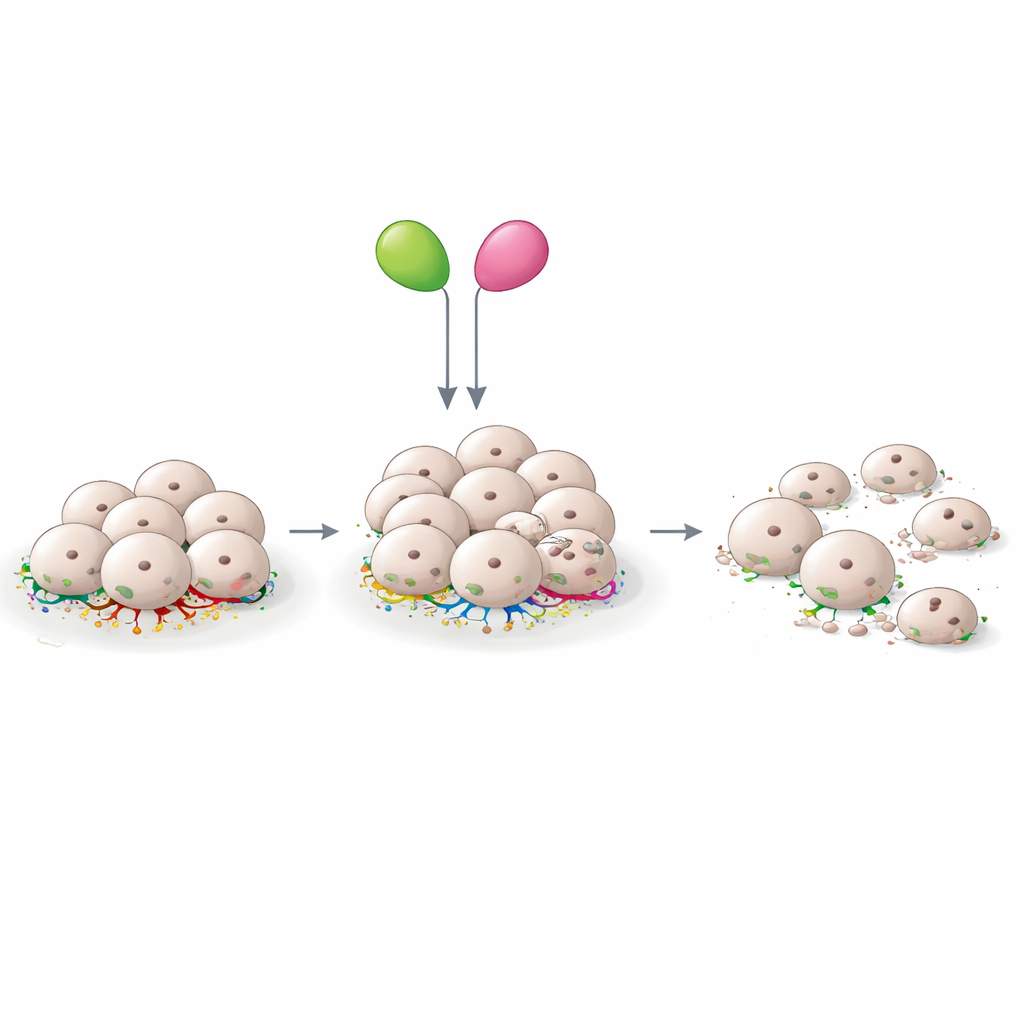
Inflammation, fästning och en lovande naturlig hjälpare
Studien lyfter också fram vikten av inflammatoriska signaler och cellfästningsmaskineri i meningiombiologin. Sulforafan är känt för att dämpa inflammatoriska vägar, medan FAK hjälper celler att känna av och reagera på sin omgivning. Att blockera båda samtidigt tycks göra meningiomceller särskilt sårbara. Noterbart var att denna effekt inte berodde på om de ursprungliga tumörerna visade förlust av Merlin, vilket tyder på att kombinationen kan fungera för en bred patientgrupp. I kontrast gav paret sulforafan och metformin en antagonistisk interaktion i detta system, vilket understryker att inte alla till synes logiska kombinationer är fördelaktiga och att noggrann testning är nödvändig.
Vad detta kan innebära för framtida behandling
Även om dessa experiment gjordes i cellkulturer och fortfarande behöver valideras i djurmodeller och kliniska prövningar är resultaten uppmuntrande. Sulforafan och metformin har redan regulatoriskt godkännande för andra användningsområden, vilket gör dem attraktiva kandidater för omprövning, medan FAK- och STAT3-hämmare går framåt i tidiga utvecklingsstadier. Eftersom meningiom ligger utanför blod-hjärnbarriären kan orala läkemedel nå dem lättare än tumörer som ligger djupare i hjärnan. Sammanvägt tyder arbetet på att riktad behandling av tumörens signaleringskretsar—med kombinationer som sulforafan plus FAK-hämning—eventuellt kan ge meningiompatienter mindre invasiva, mer skräddarsydda behandlingsalternativ för att minska tumörbörda, fördröja återfall och förbättra livskvaliteten.
Citering: Schwab, M.C., Kocas, Y., Gendreizig, S. et al. Molecular targeting of the meningioma cell signaling circuit reveals drug vulnerabilities including synergy between sulforaphane and focal adhesion kinase inhibition. BJC Rep 4, 21 (2026). https://doi.org/10.1038/s44276-026-00204-2
Nyckelord: meningiom, riktad terapi, sulforafan, fokal adhesionskinas, hjärntumörfarmakologi