Clear Sky Science · nl
Moleculaire gerichtheid op het signaalcircuit van meningeoomcellen onthult medicijnkwetsbaarheden, waaronder synergie tussen sulforafaan en remming van focal adhesion kinase
Waarom dit belangrijk is voor patiënten met een hersentumor
Meningeomen behoren tot de meest voorkomende hersentumoren, en hoewel veel ervan technisch gezien “goedaardig” zijn, kan hun ligging binnen de schedel toch ernstige beperkingen veroorzaken. Voor de meeste patiënten zijn de enige reële opties chirurgie en bestraling, beide met risico’s en die niet altijd voorkomen dat tumoren terugkomen. Deze studie onderzoekt of reeds beschikbare of experimentele geneesmiddelen de interne regelcircuits van meningeoomcellen kunnen aanpakken, en daarmee de weg kunnen openen naar mildere, medicamenteuze behandelingen die de chirurgie kunnen aanvullen of op termijn gedeeltelijk vervangen.
Een realistisch laboratoriummodel van de tumor opbouwen
Om nieuwe behandelingen te onderzoeken hadden de onderzoekers eerst een labsysteem nodig dat zich gedraagt als echte patiënttumoren. Ze verzamelden weefsel van drie personen die geopereerd werden aan graad I of II meningeomen en kweekten de cellen wekenlang in kweekschalen. De cellen van elke patiënt hadden een karakteristieke vorm en groeipatroon, maar alle drie groeiden ze in de vroege passages gestaag en vertraagden later. Het team bevestigde dat deze kweek echt meningeoomweefsel vertegenwoordigde door te controleren op eiwitten die vaak in deze tumoren aanwezig zijn en niet in normale neusfibroblasten. Dit levende model maakte het mogelijk om op een gecontroleerde en reproduceerbare manier te testen hoe verschillende medicijnen de overleving van tumorcellen beïnvloeden.
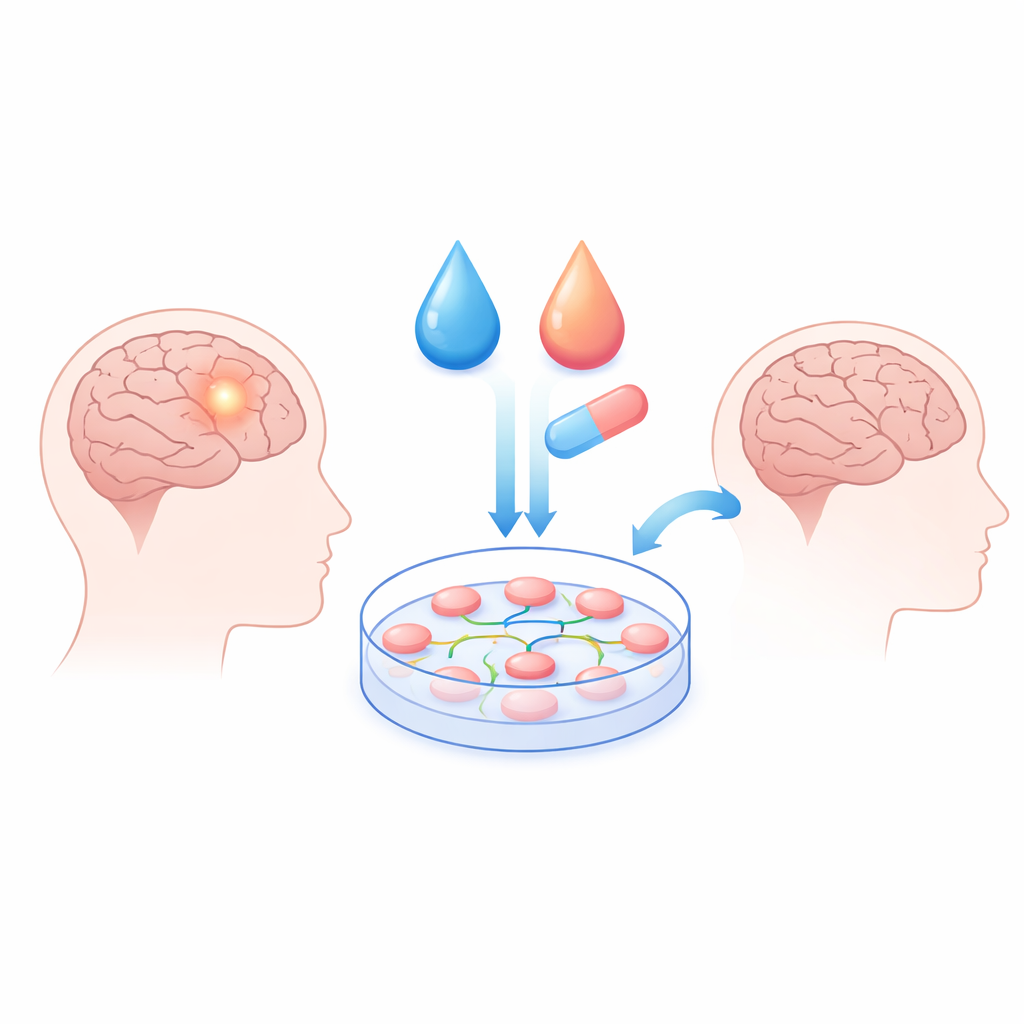
Het signaal‑“bedrading” van de tumor raken
Meningeoomcellen dragen vaak schade in een gen dat NF2 heet, dat een eiwit (Merlin) produceert dat normaal meerdere groeigerelateerde en overlevingsroutes onder controle houdt. Wanneer dit remmende mechanisme wegvalt, kunnen meerdere signaalwegen — gerelateerd aan ontsteking, groeifactoren en celhechting — de tumorgroei stimuleren. In plaats van één enkele mutatie na te jagen, richtten de auteurs zich op sleutelpunten binnen dit onderling verbonden netwerk. Ze testten een reeks geneesmiddelen die zijn geselecteerd vanwege hun vermogen deze paden te verstoren, waaronder een diabetesmiddel (metformine), een natuurlijke verbinding uit kruisbloemige groenten (sulforafaan) en remmers van focal adhesion kinase (FAK) en STAT3, moleculen die pro‑groei en pro‑ontstekingssignalen in de cel doorgeven.
Kwetsbare plekken en krachtige combinaties vinden
In eerste screenings verminderden alle geteste geneesmiddelen in meer of mindere mate de levensvatbaarheid van meningeoomcellen, maar enkele vielen op door consistent effectieve resultaten in alle drie de patiënt-afgeleide kweeklijnen. Sulforafaan, metformine, de FAK-remmer Y15 en de STAT3-remmer C188-9 toonden elk duidelijke dosisafhankelijke doding van tumorcellen. De onderzoekers concentreerden zich daarna op combinaties, met het idee dat gecoördineerde aanvallen op verschillende knooppunten in het signaalcircuit sterker kunnen zijn en lagere doseringen mogelijk maken. Met standaard synergieanalyse ontdekten ze dat sulforafaan plus Y15 een bijzonder krachtig koppel vormde: elk middel werd effectief bij lagere concentraties in combinatie, en hun gezamenlijke effect op celoverleving was groter dan de som van de individuele effecten. Microscopen toonden dat dit duo markeringen van celdeling verminderde en markeringen van geprogrammeerde celdood verhoogde, wat wijst op een daadwerkelijke uitschakeling van tumorgroei en niet slechts een tijdelijke vertraging.
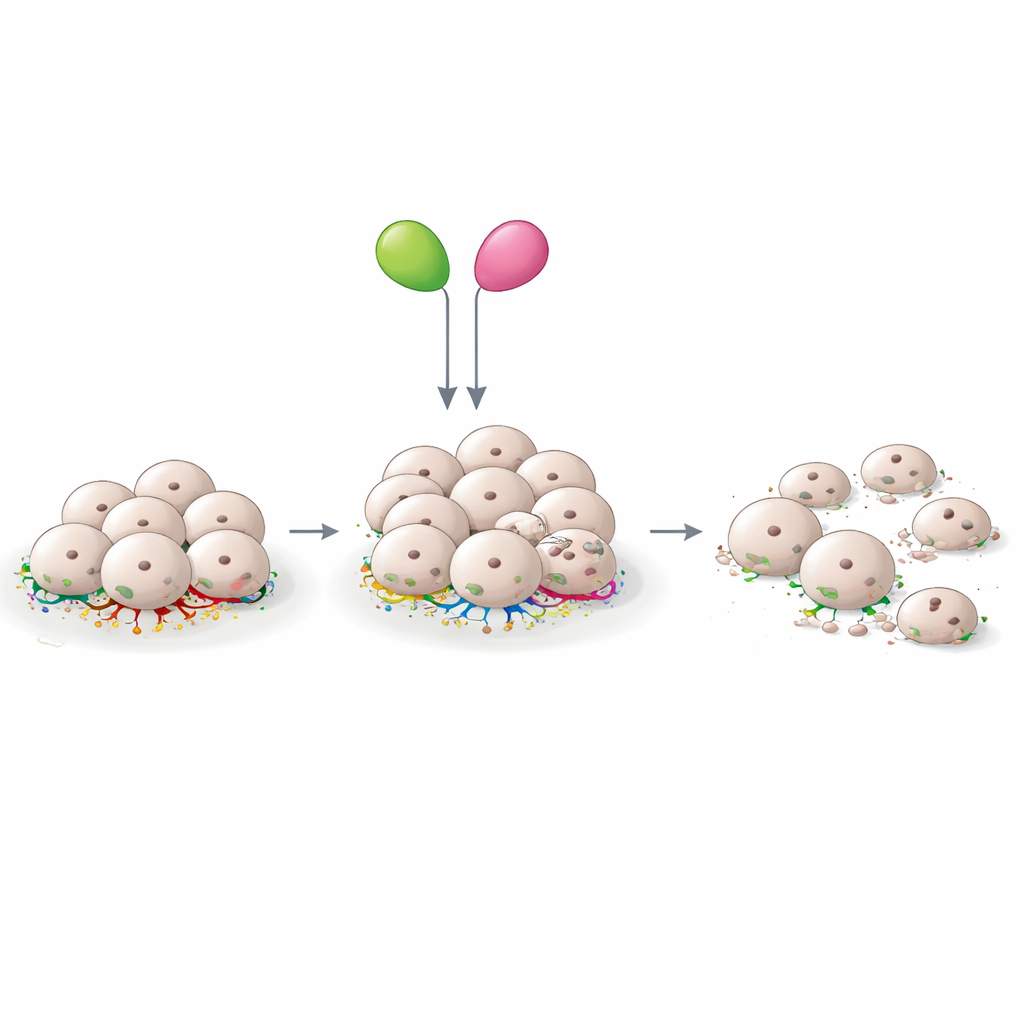
Ontsteking, hechting en een veelbelovende natuurlijke helper
De studie benadrukt ook het belang van ontstekingssignalen en het hechtingsapparaat van cellen in de biologie van meningeomen. Sulforafaan staat bekend om het dempen van ontstekingsroutes, terwijl FAK cellen helpt hun omgeving te voelen en erop te reageren. Het gelijktijdig blokkeren van beide lijkt meningeoomcellen bijzonder kwetsbaar te maken. Opmerkelijk is dat dit effect niet afhing van het al dan niet verlies van Merlin in de oorspronkelijke tumoren, wat suggereert dat de combinatie in een brede patiëntengroep werkzaam zou kunnen zijn. Daarentegen gaf de combinatie van sulforafaan met metformine in dit systeem een antagonistische interactie, wat benadrukt dat niet alle ogenschijnlijk logische samenvoegingen gunstig zijn en dat zorgvuldige testen essentieel blijven.
Wat dit kan betekenen voor toekomstige behandelingen
Hoewel deze experimenten in celkweken zijn uitgevoerd en nog gevalideerd moeten worden in diermodellen en klinische onderzoeken, zijn de resultaten bemoedigend. Sulforafaan en metformine hebben al goedkeuring voor andere toepassingen, wat ze aantrekkelijke kandidaten maakt voor herbestemming, terwijl FAK‑ en STAT3‑remmers zich in vroege ontwikkelingsfasen bevinden. Omdat meningeomen buiten de bloed‑hersenbarrière liggen, kunnen orale geneesmiddelen ze gemakkelijker bereiken dan tumoren die dieper in de hersenen zitten. Samengevat suggereert het werk dat het richten op het signaalcircuit van de tumor — met combinaties zoals sulforafaan plus FAK‑remming — mogelijk minder invasieve, meer op maat gemaakte behandelopties kan bieden om de tumorlast te verminderen, recidief uit te stellen en de kwaliteit van leven te verbeteren.
Bronvermelding: Schwab, M.C., Kocas, Y., Gendreizig, S. et al. Molecular targeting of the meningioma cell signaling circuit reveals drug vulnerabilities including synergy between sulforaphane and focal adhesion kinase inhibition. BJC Rep 4, 21 (2026). https://doi.org/10.1038/s44276-026-00204-2
Trefwoorden: meningeoom, gerichte therapie, sulforafaan, focal adhesion kinase, hersentumor farmacologie