Clear Sky Science · sv
Orbitofrontala PV-interneuroner modulerar social interaktion via dynamik i default mode-nätverket
Varför våra hjärnor behöver andra människor
De flesta av oss upplever att tid med vänner eller familj är bra för vårt psykiska välbefinnande. När den känslan av kontakt försvinner, som vid depression, schizofreni eller Alzheimers sjukdom, drar sig människor ofta undan. Denna studie utforskar en nyckelkrets i hjärnan som stödjer socialt liv. Genom att studera möss visar forskarna hur en liten grupp nervceller i hjärnans främre del kan störa ett bredare ”vilande” hjärnnätverk och därigenom minska normal social interaktion och minne.
Ett tyst hjärnnätverk med ett stort uppdrag
Även när vi sitter stilla och låter tankarna vandra, samverkar vissa hjärnregioner i ett koordinerat mönster känt som default mode-nätverket, eller DMN. Hos människor kopplas detta nätverk till dagdrömmeri, självreflektion, minnesåterkallande och att tänka på andra. Kliniska studier från PRISM-projektet har funnit att personer med schizofreni eller Alzheimers ofta uppvisar försvagade förbindelser inom detta nätverk, och dessa förändringar korrelerar med hur socialt tillbakadragna de är. Den nya studien ställer en kausal fråga: om forskare medvetet stör DMN-liknande konnektivitet i ett djur, påverkas då det sociala beteendet?
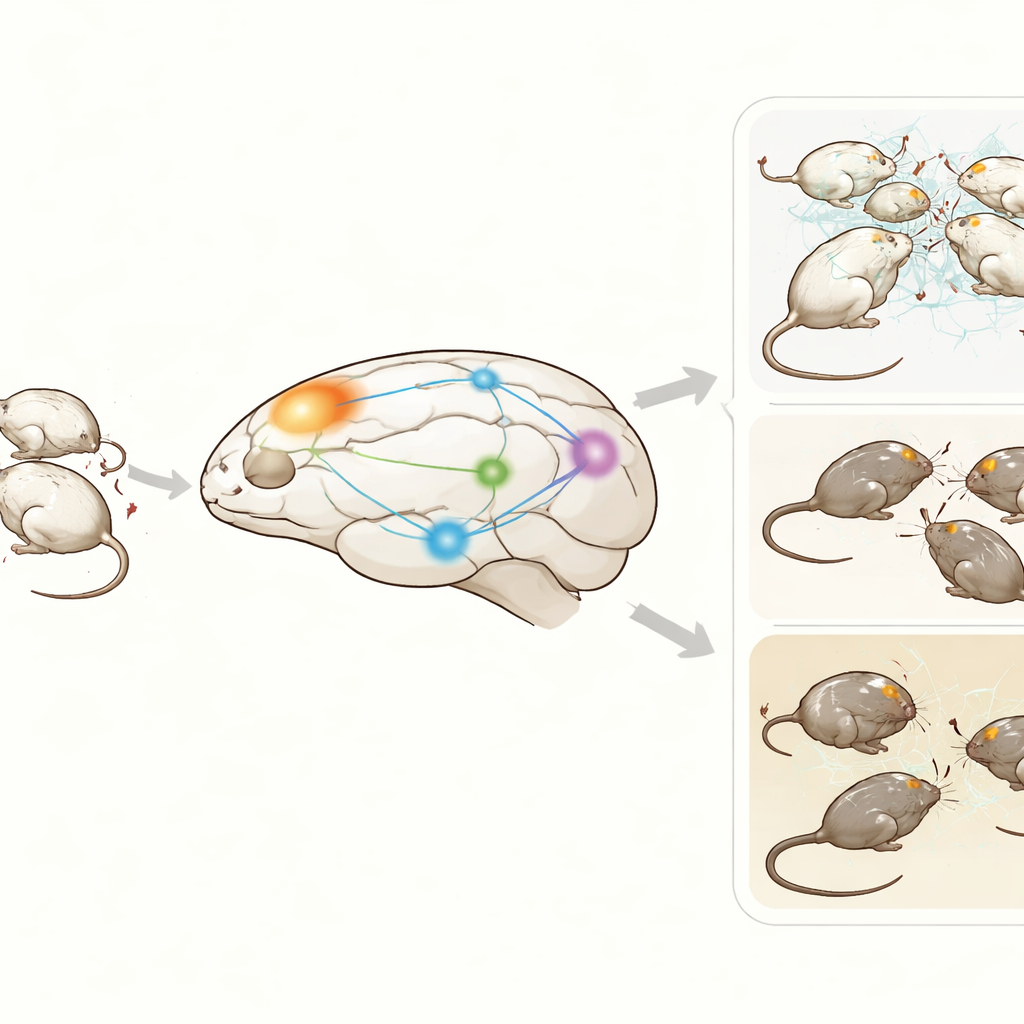
En liten kontrollknutpunkt i den frontala hjärnan
Teamet fokuserade på orbitofrontala cortex, en frontal hjärnregion viktig för att bedöma belöningar och bestraffningar, reglera känslor och forma sociala val. Inom denna region finns parvalbumin-interneuroner—snabba, hämmande nervceller som fungerar som lokala tid- och kontrollenheter. Med en kemogenetisk teknik hos hanmöss gjorde forskarna dessa celler känsliga för ett designerläkemedel. Att ge läkemedlet omvandlade dessa interneuroner till ett mycket aktivt tillstånd under en kort tid, vilket effektivt sänkte utflödet från närliggande excitatoriska celler i orbitofrontala cortex utan att skada vävnaden.
Störda hjärnrytmer i vila
För att se hur denna lokala omkoppling påverkade hela hjärnan använde forskarna högupplöst funktionell ultraljudsbildning, som spårar förändringar i blodvolym som en proxy för neural aktivitet. De mätte aktivitet och koordination mellan 29 hjärnregioner, med särskild uppmärksamhet på områden som bildar en gnagarmotsvarighet till det mänskliga DMN, inklusive hippocampus, thalamus, retrosplenial cortex, cingulumcortex och orbitofrontala cortex själv. Efter att ha aktiverat orbitofrontala interneuroner försvagades förbindelserna mellan många av dessa regioner: nyckelnav som dorsal hippocampus, subiculum, thalamus och retrosplenial cortex var mindre tätt synkroniserade i tid. Några förbindelser ökade, vilket antyder att när huvudnätverket störs så delvis omdirigerar hjärnan trafiken genom alternativa vägar, men helhetsbilden var en minskad koordinering i default mode-nätverket.
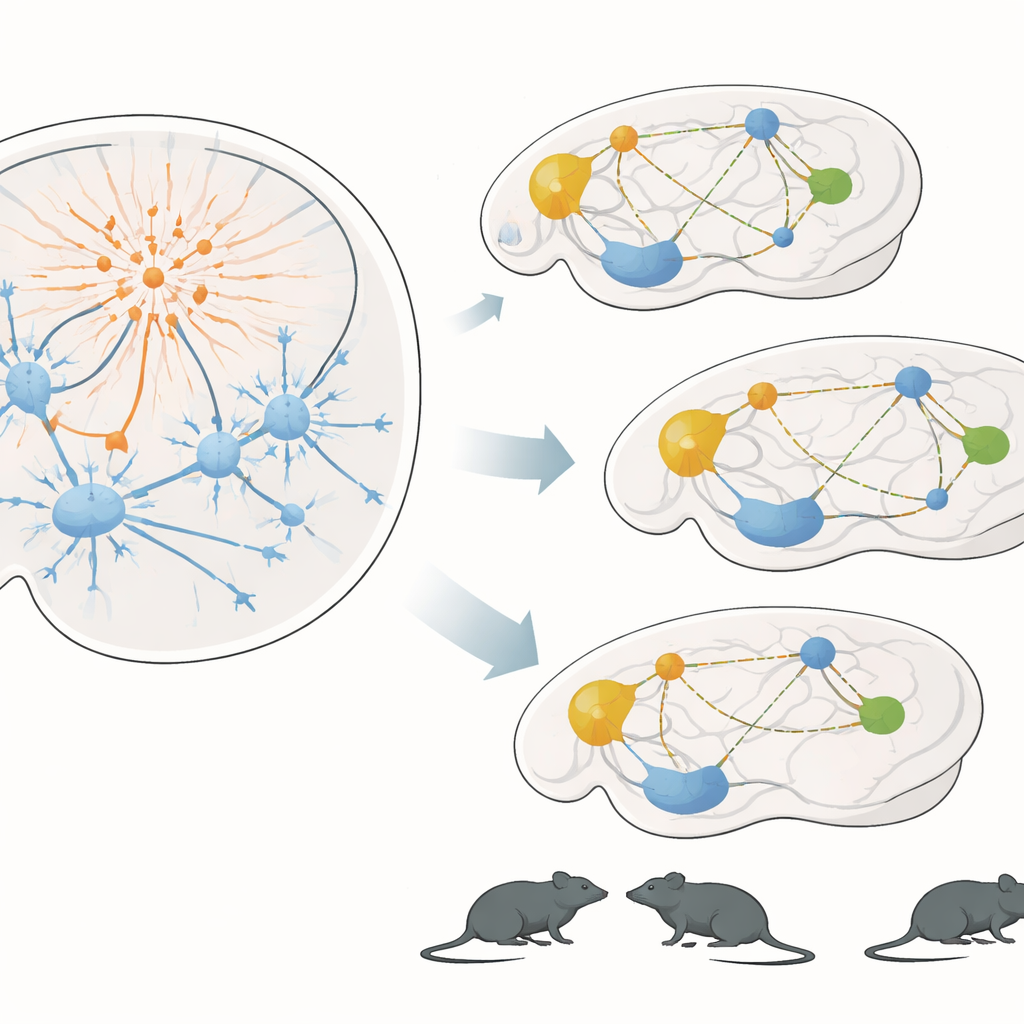
Från hjärnkretsar till socialt liv
Nästa fråga var om denna nätverksstörning gav synliga effekter på djurens vardag. Grupper om fyra möss levde tillsammans i flera dagar i en semi‑naturlig arena utrustad med automatisk spårning. Denna lösning möjliggjorde kontinuerlig övervakning av vem som närmade sig vem, hur ofta de nosade på varandra och hur mycket de rörde sig, utan mänsklig inblandning. När designerläkemedlet gavs till möss med modifierade interneuroner, tillbringade de mindre tid med att närma sig och nosa på burkamraterna under den aktiva nattperioden, även om deras totala rörelse var normal. I ett separat minnestest med bekanta och nya föremål utforskade dessa möss lika mycket som kontroller men visade inte en tydlig preferens för det nya föremålet, vilket tyder på ett specifikt minnesunderskott snarare än enkel slöhet.
Vad detta betyder för människors hälsa
Tillsammans visar fynden att en kortvarig överaktivering av en liten grupp hämmande celler i orbitofrontala cortex kan sprida sig genom hjärnans default-nätverk, försvaga långtidskommunikation och framkalla både socialt tillbakadragande och minnesproblem hos möss. Detta speglar mönster som ses hos människor med allvarliga psykiska och neurodegenerativa sjukdomar, där liknande celltyper och hjärnkretsar antas påverkas. Även om studien inte erbjuder en behandling, utgör den en mekanistisk bro mellan cellnivåförändringar och komplext socialt beteende. Genom att peka ut parvalbumin-interneuroner i orbitofrontala cortex som viktiga grindvakter för sociala hjärnnätverk, antyder arbetet nya riktningar för framtida forskning om hur man kan skydda eller återställa social funktion när dessa kretsar går fel.
Citering: Khatamsaz, E., Ionescu, T.M., Keppler, K. et al. Orbitofrontal PV interneurons modulate social interaction via default mode network dynamics. Commun Biol 9, 573 (2026). https://doi.org/10.1038/s42003-026-10060-y
Nyckelord: socialt beteende, default mode-nätverk, orbitofrontala cortex, parvalbumin-interneuroner, funktionell konnektivitet