Clear Sky Science · es
Interneuronas PV orbitofrontales modulan la interacción social mediante la dinámica de la red por defecto
Por qué nuestros cerebros necesitan a otras personas
La mayoría de nosotros sentimos que pasar tiempo con amigos o familia es beneficioso para la salud mental. Cuando esta sensación de conexión se desvanece, como en la depresión, la esquizofrenia o la enfermedad de Alzheimer, las personas a menudo se aíslan. Este artículo explora un circuito cerebral clave que ayuda a sostener la vida social. Estudiando ratones, los investigadores muestran cómo un pequeño grupo de células nerviosas en la parte frontal del cerebro puede perturbar una red cerebral más amplia «en reposo» y, a su vez, reducir la interacción social y la memoria normales.
Una red cerebral tranquila con una gran función
Incluso cuando nos sentamos quietos y dejamos que la mente divague, ciertas regiones cerebrales funcionan de forma sincronizada en un patrón conocido como red por defecto, o DMN. En las personas, esta red se asocia con soñar despierto, la autorreflexión, recordar el pasado y pensar en los demás. Estudios clínicos del proyecto PRISM han encontrado que las personas con esquizofrenia o enfermedad de Alzheimer suelen mostrar conexiones debilitadas dentro de esta red, y esos cambios se correlacionan con el grado de retraimiento social. El nuevo estudio plantea una pregunta causal: si los científicos alteran deliberadamente la conectividad parecida a la DMN en un animal, ¿se resiente el comportamiento social?
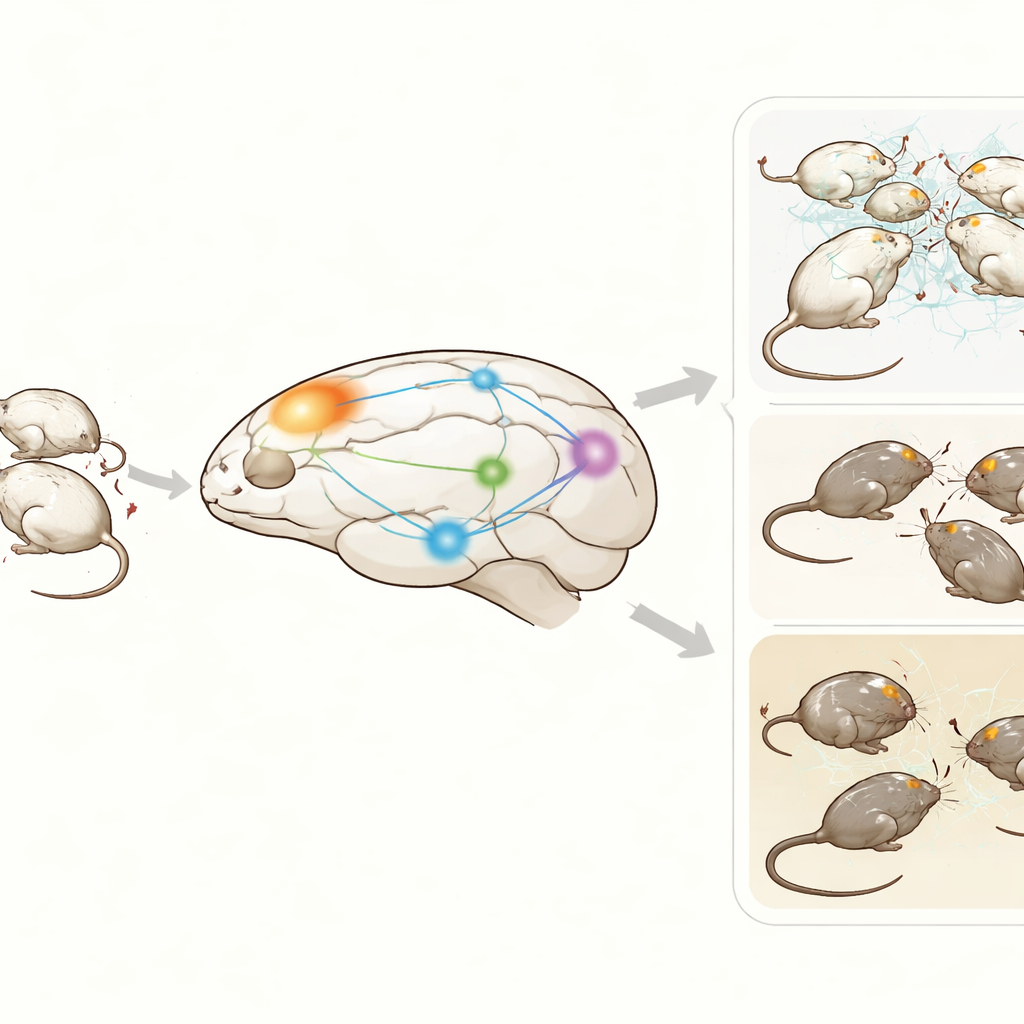
Un pequeño centro de control en la parte frontal del cerebro
El equipo se centró en la corteza orbitofrontal, una región frontal importante para valorar recompensas y castigos, regular las emociones y moldear las decisiones sociales. En esta región residen interneuronas parvalbúmina: células nerviosas inhibitorias rápidas que actúan como unidades locales de temporización y control. Usando una técnica quimio-genética en ratones machos, los investigadores diseñaron estas células para que respondieran a un fármaco diseñador. Administrar el fármaco activó brevemente estas interneuronas, llevándolas a un estado de alta actividad que redujo efectivamente la salida de las células excitatorias vecinas en la corteza orbitofrontal sin dañar el tejido.
Ritmos cerebrales alterados en reposo
Para ver cómo afectaba este interruptor local al cerebro entero, los científicos usaron imagen por ultrasonido funcional de alta resolución, que rastrea cambios en el volumen sanguíneo como proxy de la actividad neuronal. Midieron la actividad y la coordinación entre 29 regiones cerebrales, prestando especial atención a áreas que forman una versión rodente de la DMN humana, incluyendo el hipocampo, el tálamo, la corteza retrosplenial, la corteza cingulada y la propia corteza orbitofrontal. Tras activar las interneuronas orbitofrontales, se debilitó la conectividad entre muchas de estas regiones: nodos clave como el hipocampo dorsal, el subículo, el tálamo y la corteza retrosplenial estuvieron menos sincronizados en el tiempo. Algunas conexiones aumentaron, lo que sugiere que cuando la red principal se ve perturbada el cerebro en parte reencamina el tráfico por vías alternativas, pero el panorama global fue de menor coordinación de la red por defecto.
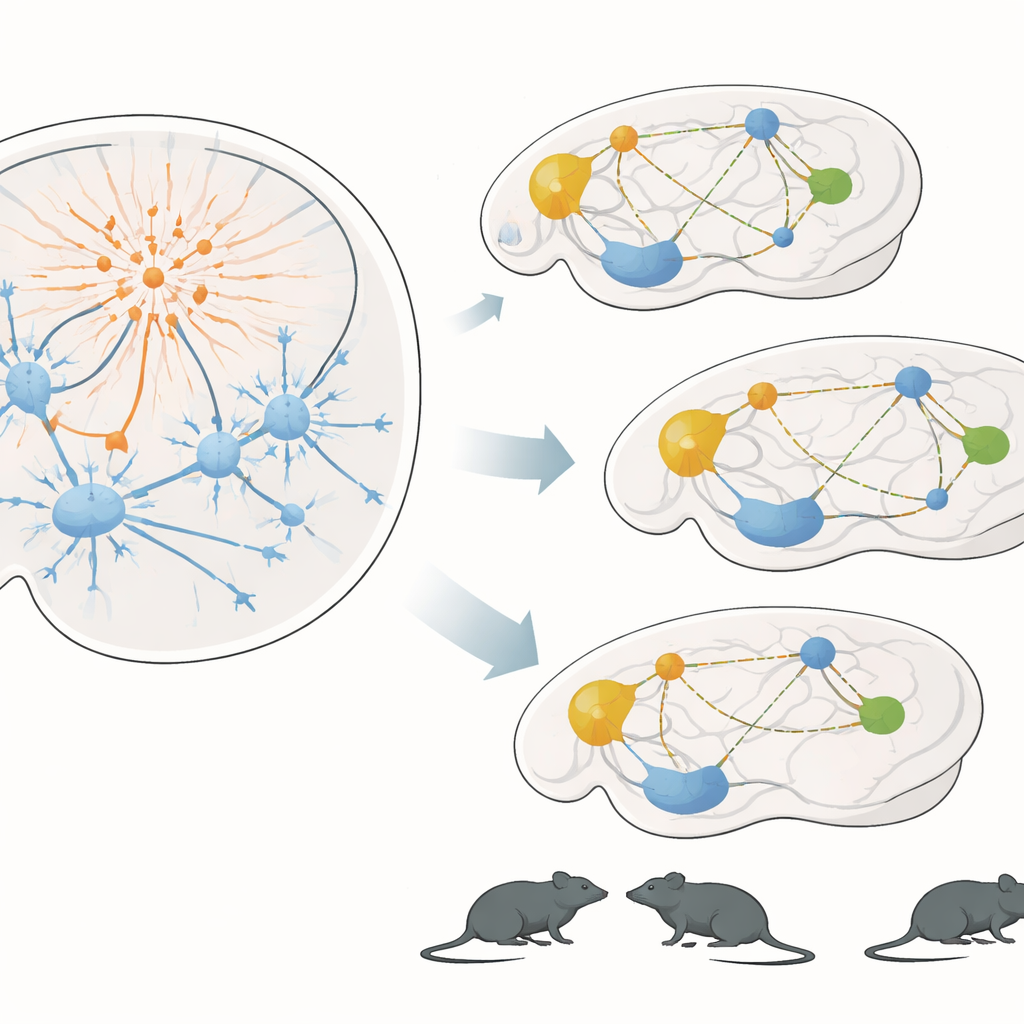
De los circuitos cerebrales a la vida social
La siguiente pregunta fue si esta alteración de la red tenía efectos visibles en la conducta de los animales. Grupos de cuatro ratones convivieron durante días en una arena semi-natural equipada con seguimiento automático. Este montaje permitió monitorizar de forma continua quién se acercaba a quién, la frecuencia de los olfateos entre ellos y cuánto se movían, sin intervención humana. Cuando se administró el fármaco diseñador a ratones con interneuronas modificadas, pasaron menos tiempo acercándose y olfateando a sus compañeros de jaula durante el periodo nocturno activo, aunque su movimiento global se mantuvo normal. En una prueba de memoria separada con objetos familiares y nuevos, estos mismos ratones exploraron tanto como los controles pero no mostraron una preferencia clara por el objeto nuevo, lo que sugiere un déficit específico de memoria más que una simple letargia.
Qué significa esto para la salud humana
En conjunto, los hallazgos muestran que una breve sobreactivación de un pequeño grupo de células inhibitorias en la corteza orbitofrontal puede propagarse por la red por defecto del cerebro, debilitar la comunicación a larga distancia y producir tanto retraimiento social como problemas de memoria en ratones. Esto refleja patrones observados en personas con enfermedades mentales graves y trastornos neurodegenerativos, donde se piensa que tipos celulares y circuitos cerebrales similares están afectados. Aunque este estudio no ofrece un tratamiento, proporciona un puente mecanístico entre cambios a nivel celular y comportamientos sociales complejos. Al identificar a las interneuronas parvalbúmina de la corteza orbitofrontal como guardianes importantes de las redes sociales cerebrales, el trabajo sugiere nuevas direcciones para futuras investigaciones sobre cómo proteger o restaurar la función social cuando estos circuitos fallan.
Cita: Khatamsaz, E., Ionescu, T.M., Keppler, K. et al. Orbitofrontal PV interneurons modulate social interaction via default mode network dynamics. Commun Biol 9, 573 (2026). https://doi.org/10.1038/s42003-026-10060-y
Palabras clave: comportamiento social, red por defecto, corteza orbitofrontal, interneuronas parvalbúmina, conectividad funcional