Clear Sky Science · sv
Bärbara sensorer för övervakning av läkemedels farmakokinetik hos patienter med Parkinsons sjukdom
Varför denna nya bäbara enhet spelar roll
Personer med Parkinsons sjukdom förlitar sig ofta på ett decennier gammalt läkemedel, L‑DOPA, för att hålla rörelserna stabila. Men läkemedlets effekter kan komma och gå oförutsägbart under en dag, vilket gör det svårt för både patienter och läkare att veta när dosen är lagom. Den här studien undersöker ett litet bärbart plåster som läser av läkemedelsnivåer i svett och erbjuder ett smärtfritt sätt att spåra medicinering i realtid och koppla den direkt till symptom som handtremor.
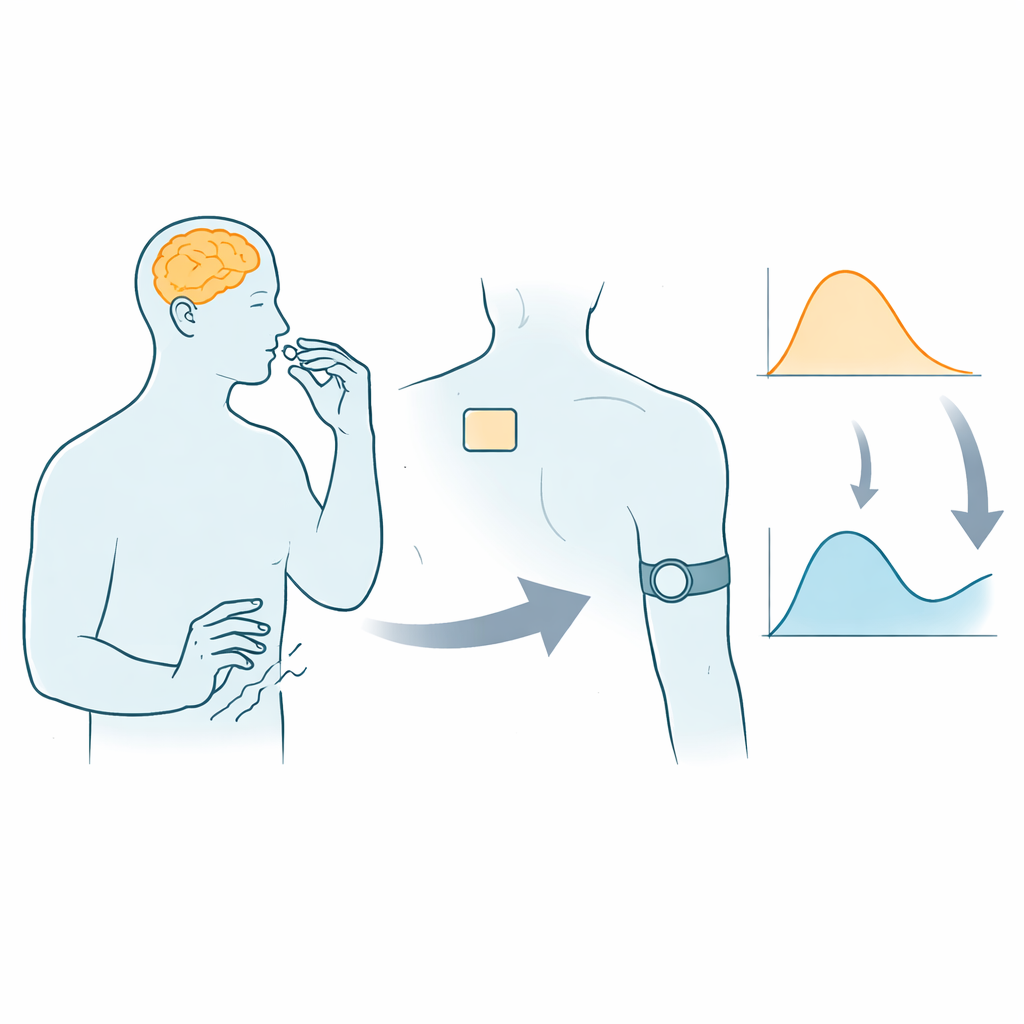
Utmaningen att tajma Parkinsonsmedicin
Parkinsons sjukdom berövar människor gradvis deras smidiga rörelser och kan också påverka sömn, stämning och tänkande. L‑DOPA är fortfarande det mest effektiva läkemedlet för att lindra många av dessa problem, men nyttan beror starkt på hur mycket av läkemedlet som finns i kroppen vid en given tidpunkt. Den nivån kan svänga på grund av skillnader i matsmältning, kost och sjukdomsstadium. I dag justerar läkare oftast doser med hjälp av skattningsskalor och patientdagböcker, som bara ger korta ögonblicksbilder och påverkas av minne och omdöme. Som ett resultat tillbringar många en del av dagen i ett ”off”-tillstånd, när symptomen återkommer, eller i ett överdoserat tillstånd när överdrivna rörelser uppstår.
Att omvandla svett till en läkemedelsavläsning
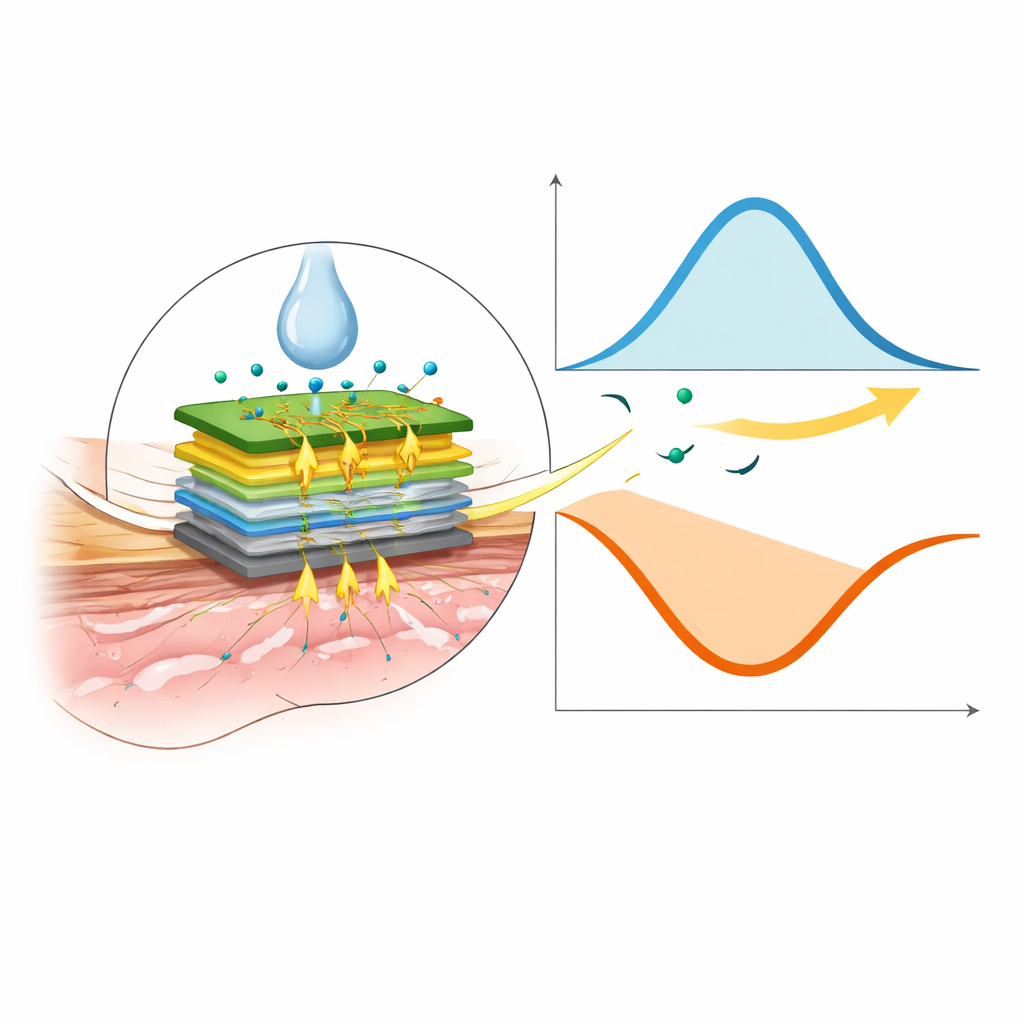
Forskarna försökte bygga en bärbar sensor som skulle kunna spåra L‑DOPA i en lättillgänglig kroppsvätska: svett. De använde en liten kommersiell guldelektrod och belade den med flera mikroskopiska lager, inklusive förgrenade guldkonstruktioner och ett enzym som reagerar med L‑DOPA. När svett når denna yta genererar reaktionen en elektrisk signal vars styrka speglar hur mycket läkemedel som finns. I laboratoriet visade teamet att sensorn svarar linjärt på L‑DOPA över det medicinskt relevanta intervallet, med endast små förändringar orsakade av normala skiftningar i hudtemperatur eller svettens surhetsgrad. Tester i verklig mänsklig svett bekräftade att enheten pålitligt kan skilja L‑DOPA från vanliga störande ämnen som urinsyra, vitamin C och glukos.
Test av plåstret på verkliga patienter
För att se hur tekniken fungerar i vardagsmiljö rekryterade teamet 39 personer med Parkinsons sjukdom på ett sjukhus i Taiwan; 32 slutförde hela studien. Efter att ha hoppat över sina vanliga Parkinsonsmediciner över natten genomgick deltagarna fyra testomgångar med 30 minuters mellanrum. I varje omgång bar de en inertialsensor på armen för att spela in tremor, fick svettplåstret fäst på övre delen av ryggen och utförde en serie rörelseuppgifter som handcykling, promenad i en korridor med smartklocka och att rita cirklar. Efter den första omgången tog de sina vanliga orala L‑DOPA‑tabletter, och de senare omgångarna fångade hur både läkemedelsnivåer och rörelser förändrades när medicinen trädde i kraft och sedan började avta.
Koppla läkemedelsnivåer till kroppsrörelser
För 24 deltagare som producerade tillräckligt med svett för analys jämförde forskarna två tidsförlopp: L‑DOPA‑nivåer från plåstret och tremorintensitet från rörelsesensorn. Hos ungefär fyra av fem av dessa patienter var högre svett‑L‑DOPA‑värden förknippade med svagare tremor, vilket visar en tydlig omvänd relation. Studien grupperade också tremormönster i flera typer, såsom en stadig förbättring direkt efter dosering eller en initial förbättring följd av en återgång när läkemedelsnivån sjönk. Utöver tremor steg och sjönk ofta andra rörelsemått—handcyklingshastighet, gångtempo och tiden som krävdes för att slutföra en rituppgift—i takt med svettens läkemedelsprofil, vilket antyder att en enda biokemisk avläsning kan sammanfatta komplexa fysiska responser.
Vad detta kan innebära för vardagsvård
Denna pilotstudie tyder på att ett tunt svettplåster, i kombination med enkla rörelsesensorer, kan ge en inblick i hur Parkinsonsmedicin beter sig i kroppen utan att ta blodprov. Genom att visa att svett‑L‑DOPA‑nivåer följer förändringar i tremor hos de flesta patienter pekar arbetet mot en framtid där läkare finjusterar doser baserat på objektiva, dygnet‑runt‑data snarare än sporadiska klinikbesök och patientens återgivning. Med vidare validering mot blodmätningar och längre studier skulle sådana bärbara enheter kunna stödja mer personliga behandlingsscheman, minska tiden i handikappande ”off”-perioder och så småningom integreras i smarta, sluten‑loop‑system som automatiskt justerar terapi i takt med att en persons symtom fluktuerar.
Citering: Guo, YJ., Li, CC., Huang, JA. et al. Wearable sensors for monitoring drug pharmacokinetics in patients with Parkinson’s disease. Sci Rep 16, 13332 (2026). https://doi.org/10.1038/s41598-026-43825-w
Nyckelord: Parkinsons sjukdom, bärbara sensorer, svettövervakning, L‑DOPA, tremorövervakning