Clear Sky Science · nl
Draagbare sensoren voor het volgen van geneesmiddel‑farmacokinetiek bij patiënten met de ziekte van Parkinson
Waarom deze nieuwe wearable ertoe doet
Mensen met de ziekte van Parkinson zijn vaak afhankelijk van een decenniaoud middel genaamd L‑DOPA om hun bewegingen stabiel te houden. Toch kunnen de effecten van het middel onvoorspelbaar aan‑ en uitgaan gedurende de dag, waardoor het voor patiënten en artsen moeilijk is te bepalen wanneer de dosis precies goed is. Deze studie onderzoekt een klein draagbaar pleister‑achtig apparaat dat medicijnniveaus uit zweet afleest, en zo een pijnloze manier biedt om medicatie in realtime te volgen en die direct te koppelen aan symptomen zoals handtremor.
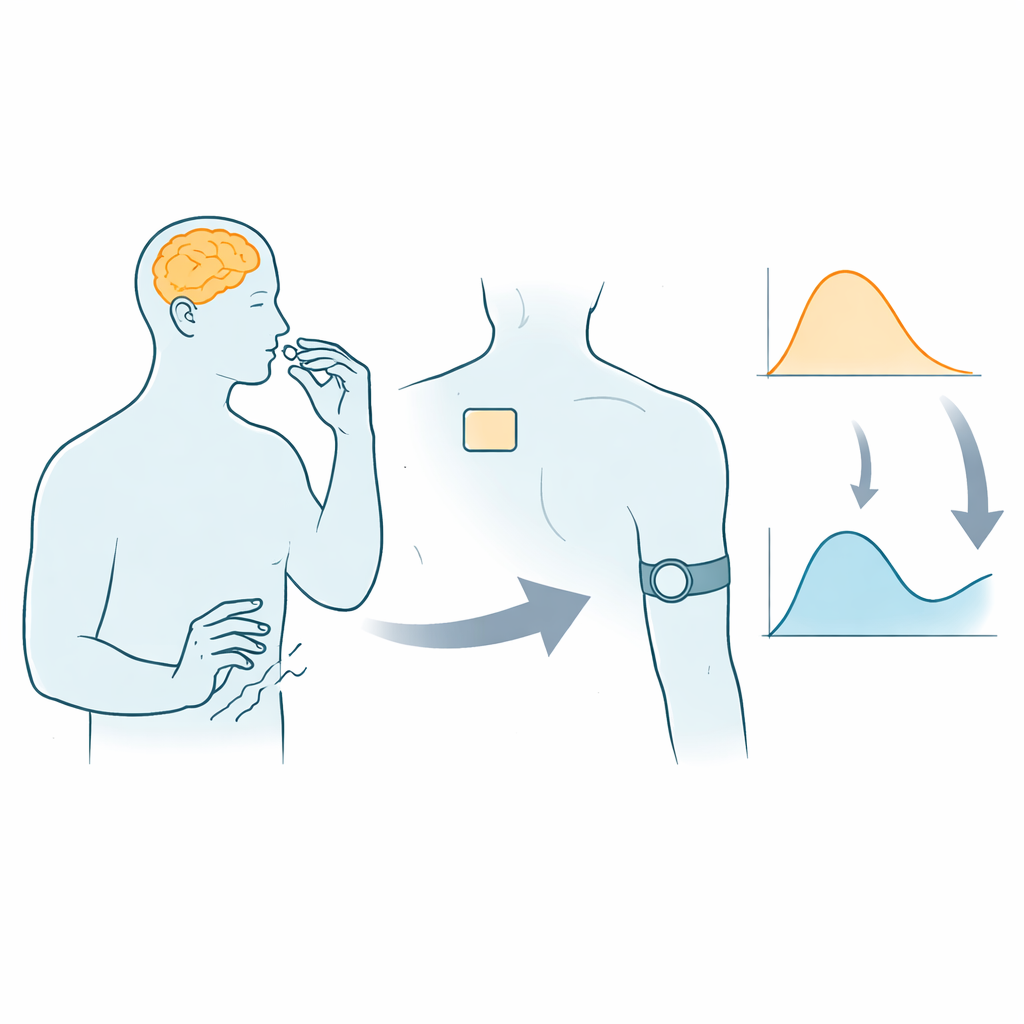
De uitdaging van het timen van Parkinson‑medicatie
De ziekte van Parkinson berooft mensen geleidelijk van vloeiende bewegingen en kan ook slaap, stemming en cognitieve functies aantasten. L‑DOPA blijft het meest effectieve middel om veel van deze klachten te verlichten, maar het effect hangt sterk af van de hoeveelheid geneesmiddel die op een gegeven moment in het lichaam aanwezig is. Dat niveau kan op en neer schommelen door verschillen in maag‑darmpassage, voeding en ziektestadium. Tegenwoordig stellen artsen doseringen voornamelijk bij op basis van beoordelingsschalen en patiëntendagboeken, die slechts korte momentopnames geven en beïnvloed worden door geheugen en beoordeling. Daardoor brengen veel mensen een deel van de dag door in een “off”-periode, wanneer de symptomen terugkeren, of zijn ze “overgedoseerd”, wanneer juist overdreven bewegingen optreden.
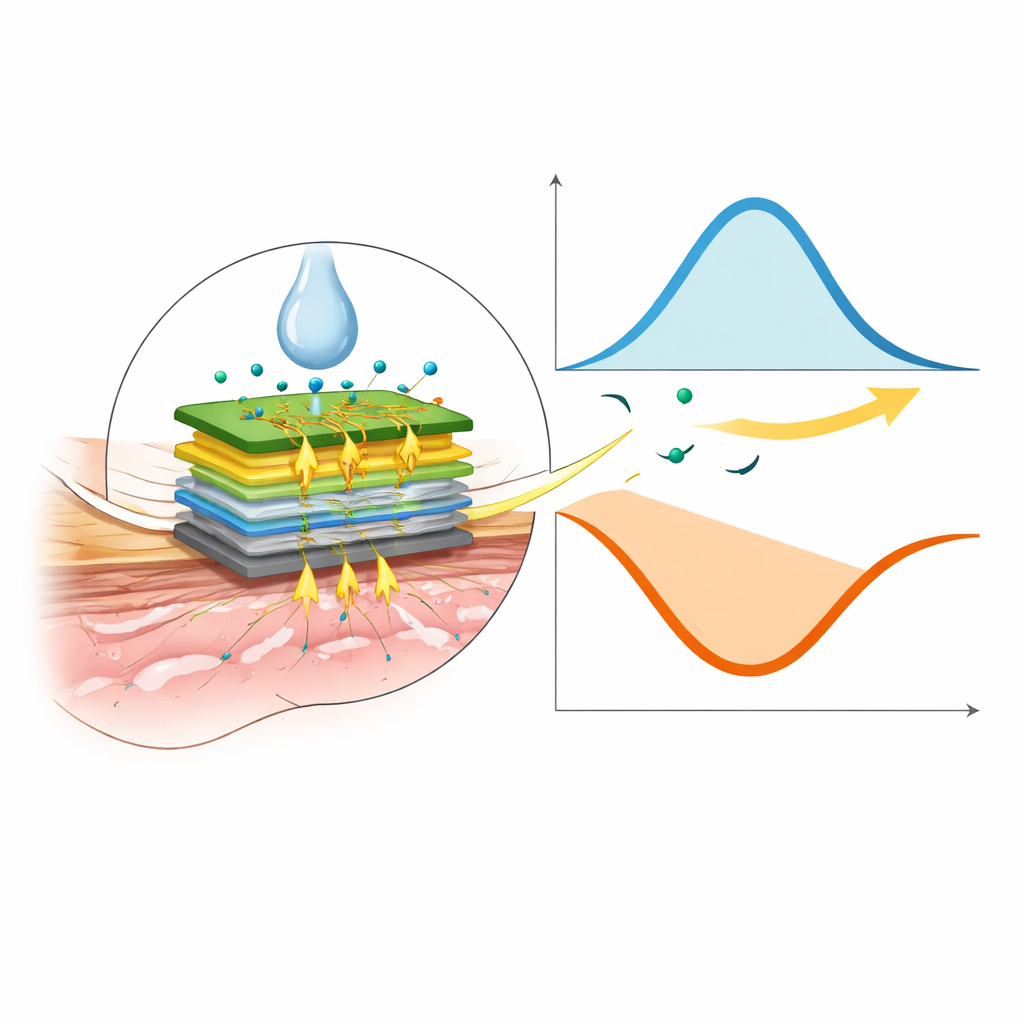
Zweet omzetten in een medicijnaflezing
De onderzoekers wilden een draagbare sensor ontwikkelen die L‑DOPA kan volgen in een gemakkelijk toegankelijke lichaamsvloeistof: zweet. Ze gebruikten een kleine commerciële gouden elektrode en coatten die met meerdere microscopische lagen, waaronder vertakte goudstructuren en een enzym dat reageert met L‑DOPA. Wanneer zweet dit oppervlak raakt, genereert de reactie een elektrisch signaal waarvan de sterkte weerspiegelt hoeveel geneesmiddel aanwezig is. In het lab lieten de onderzoekers zien dat de sensor lineair reageert op L‑DOPA binnen het medisch relevante bereik, met slechts kleine veranderingen door normale schommelingen in huidtemperatuur of zweetzuurgraad. Tests met echt menselijk zweet bevestigden dat het apparaat L‑DOPA betrouwbaar kan onderscheiden van veelvoorkomende storende stoffen zoals urinezuur, vitamine C en glucose.
De pleister testen bij echte patiënten
Om te zien hoe de technologie presteert onder dagelijkse omstandigheden, rekruteerde het team 39 mensen met de ziekte van Parkinson in een ziekenhuis in Taiwan; 32 voltooiden de volledige studie. Nadat ze de gebruikelijke Parkinson‑medicatie een nacht hadden overgeslagen, ondergingen de deelnemers vier rondes van tests met tussenpozen van 30 minuten. In elke ronde droegen ze een traagheidsensor aan de arm om tremor te registreren, werd de zweetpleister op de bovenrug bevestigd en voerden ze een reeks bewegingsopdrachten uit zoals handfietsen, lopen in een gang met een smartwatch en cirkels tekenen. Na de eerste ronde namen ze hun gebruikelijke orale L‑DOPA‑tabletten, en de latere rondes legden vast hoe zowel medicijnspiegels als beweging veranderden naarmate de medicatie begon te werken en later weer afnam.
Geneesmiddelspiegels koppelen aan lichaamsbeweging
Voor 24 deelnemers die genoeg zweet produceerden voor analyse, vergeleken de wetenschappers twee tijdsverlopen: L‑DOPA‑niveaus uit de pleister en tremorintensiteit uit de bewegingssensor. Bij ongeveer vier van de vijf van deze patiënten gingen hogere L‑DOPA‑waarden in zweet samen met zwakkere tremor, wat een duidelijke inverse relatie liet zien. De studie groepeerde tremorpatronen ook in verschillende typen, zoals een gestage verbetering direct na dosering of een aanvankelijke verbetering gevolgd door een terugslag zodra het medicijnniveau daalde. Buiten tremor vertoonden andere bewegingsparameters — handfietssnelheid, loopsnelheid en de tijd die nodig was om een tekentaak te voltooien — vaak gelijke pieken en dalen met het zweet‑medicijnprofiel, wat erop wijst dat één biochemische aflezing complexe fysieke reacties kan samenvatten.
Wat dit kan betekenen voor de dagelijkse zorg
Deze pilotstudie suggereert dat een dunne zweetpleister, gecombineerd met eenvoudige bewegingssensoren, een inkijkje kan geven in hoe Parkinson‑medicatie zich in het lichaam gedraagt zonder bloedafname. Door aan te tonen dat zweet L‑DOPA‑waarden voor de meeste patiënten nauw samenlopen met veranderingen in tremor, wijst het werk op een toekomst waarin artsen dosissen verfijnen op basis van objectieve, continue gegevens in plaats van sporadische kliniekbezoeken en patiëntherinnering. Met verdere validatie ten opzichte van bloedmetingen en langdurigere studies zouden dergelijke wearables meer gepersonaliseerde behandelroosters kunnen ondersteunen, de tijd in invaliderende “off”-periodes kunnen verkorten en uiteindelijk kunnen integreren in slimme, gesloten‑lus systemen die therapie automatisch aanpassen naarmate de symptomen van een persoon fluctueren.
Bronvermelding: Guo, YJ., Li, CC., Huang, JA. et al. Wearable sensors for monitoring drug pharmacokinetics in patients with Parkinson’s disease. Sci Rep 16, 13332 (2026). https://doi.org/10.1038/s41598-026-43825-w
Trefwoorden: Ziekte van Parkinson, draagbare sensoren, <keyword>L‑DOPA, tremorregistratie