Clear Sky Science · sv
Integration av cirkulerande tumör-DNA-data förbättrar lungcancerprediktion hos patienter med KOL
Varför detta är viktigt för personer med kronisk lungsjukdom
Personer som lever med kronisk obstruktiv lungsjukdom (KOL) har en betydligt högre risk att utveckla lungcancer, men att upptäcka cancer tidigt i dessa skadade lungor är notorisk svårt och kräver ofta riskfyllda biopsier. Denna studie undersöker om ett enkelt blodprov som fångar upp små fragment av tumör-DNA, i kombination med moderna datoralgoritmer, kan mer precist flagga vilka KOL-patienter som sannolikt har lungcancer — och göra det på ett sätt som en dag kan skona vissa patienter från invasiva ingrepp.
Letar efter cancermarkörer i blodet
När cancerceller växer släpper de ifrån sig delar av sitt DNA ut i blodet, så kallat cirkulerande tumör-DNA. Forskarna samlade blod från 236 personer med måttlig KOL, ungefär hälften av vilka redan hade lungcancer och hälften inte. Istället för att undersöka hela genomet fokuserade de på 24 gener som ofta är förändrade i lungtumörer. Med en mycket känslig sekvenseringsmetod sökte de i varje blodprov efter typiska mutationer och mätte också hur mycket muterat DNA som fanns samt hur tydligt signalen stod ut från bakgrundsbrus.
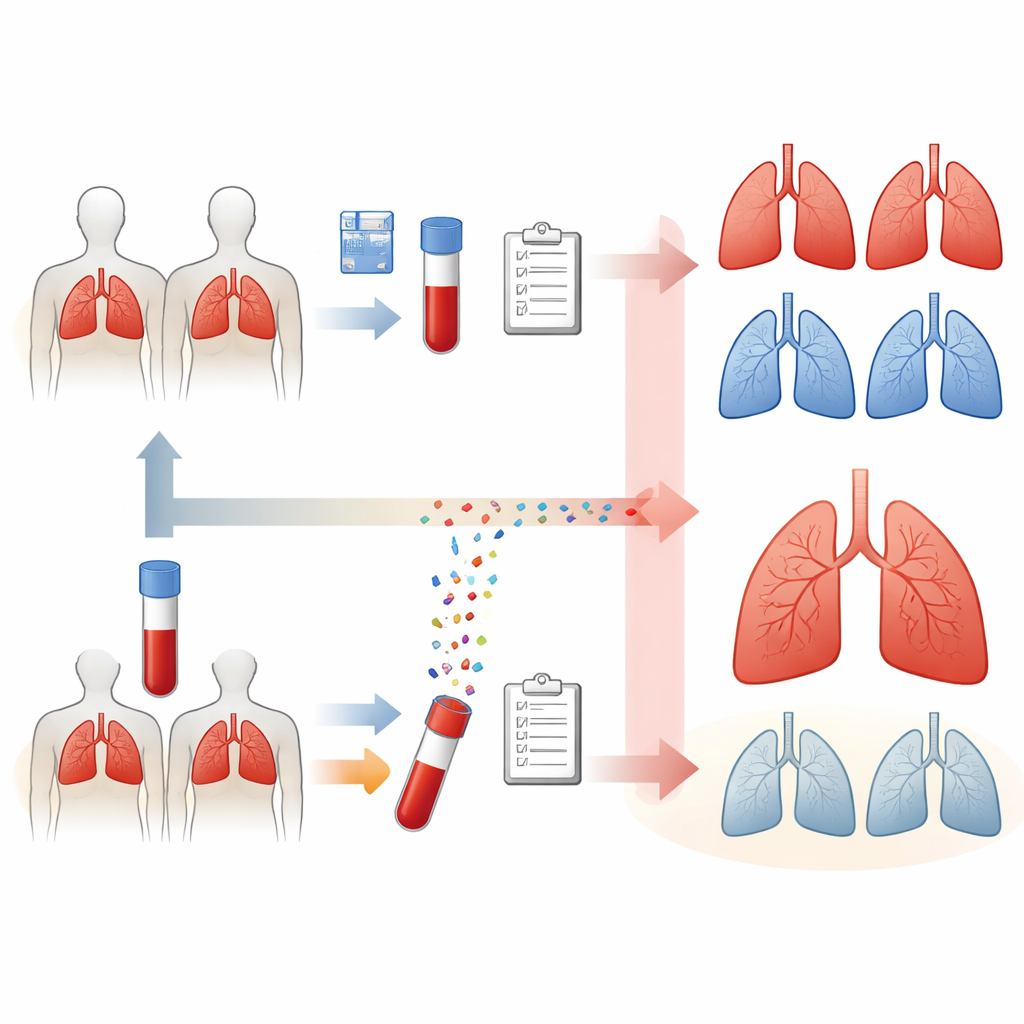
Att lägga till smarta algoritmer till traditionella riskfaktorer
Samtidigt som blodprovet samlade teamet detaljerad klinisk information för varje deltagare, inklusive ålder, kön, rökvanor, lungfunktion, inflammationsmarkörer i blodet och frågeformulär om andningssymtom. De matade sedan 40 informationspunkter — kliniska mått plus genomiska och molekylära egenskaper från blodet — in i nio olika maskininlärningsmodeller. Dessa modeller omfattade välkända statistiska metoder och mer flexibla mönsterigenkänningsmetoder som kan upptäcka subtila, icke-linjära samband mellan variabler. Målet var enkelt: lära datorn att särskilja KOL-patienter med lungcancer från dem utan.
Vad som skiljde cancerpatienterna åt
Flera tydliga skillnader framträdde mellan de två grupperna. KOL-patienter med lungcancer var mer benägna att vara storrökare och att ha högre nivåer av C-reaktivt protein, en blodmarkör kopplad till kronisk inflammation. Överraskande nog rapporterade de färre KOL-symtom än patienter utan cancer, vilket sannolikt speglar skillnader i hur och när varje grupp sökte vård. På DNAnivå var kontrasten ännu starkare: tumörrelaterade mutationer i blodet och klassiska lungcancer–”driver”-gener — särskilt den välkända tumörsuppressorn TP53 — förekom mycket oftare hos dem med cancer, och deras tumör-DNA-fragment visade starkare molekylärt stöd i sekvenseringsdata.
Starkare prediktioner när DNA-data ingår
När forskarna tränade sina modeller enbart med traditionell klinisk information var prediktionens noggrannhet måttlig. Men när de lade till tumör-DNA-signalerna och relaterade molekylära mått förbättrades prestandan tydligt, särskilt för de mer flexibla, icke-linjära modellerna. Den bästa modellen, en radial supportvektormaskin, visade högre sensitivitet (fann fler verkliga cancerfall), bättre balans mellan falska positiva och falska negativa samt en större area under kurvan, ett standardmått på total noggrannhet. Viktigt är att de mest inflytelserika prediktorerna i denna kombinerade modell inte längre bara var rökning och inflammation, utan även förekomst av tumör-DNA-mutationer, styrkan i sekvenseringssignalen och mutationer i TP53.
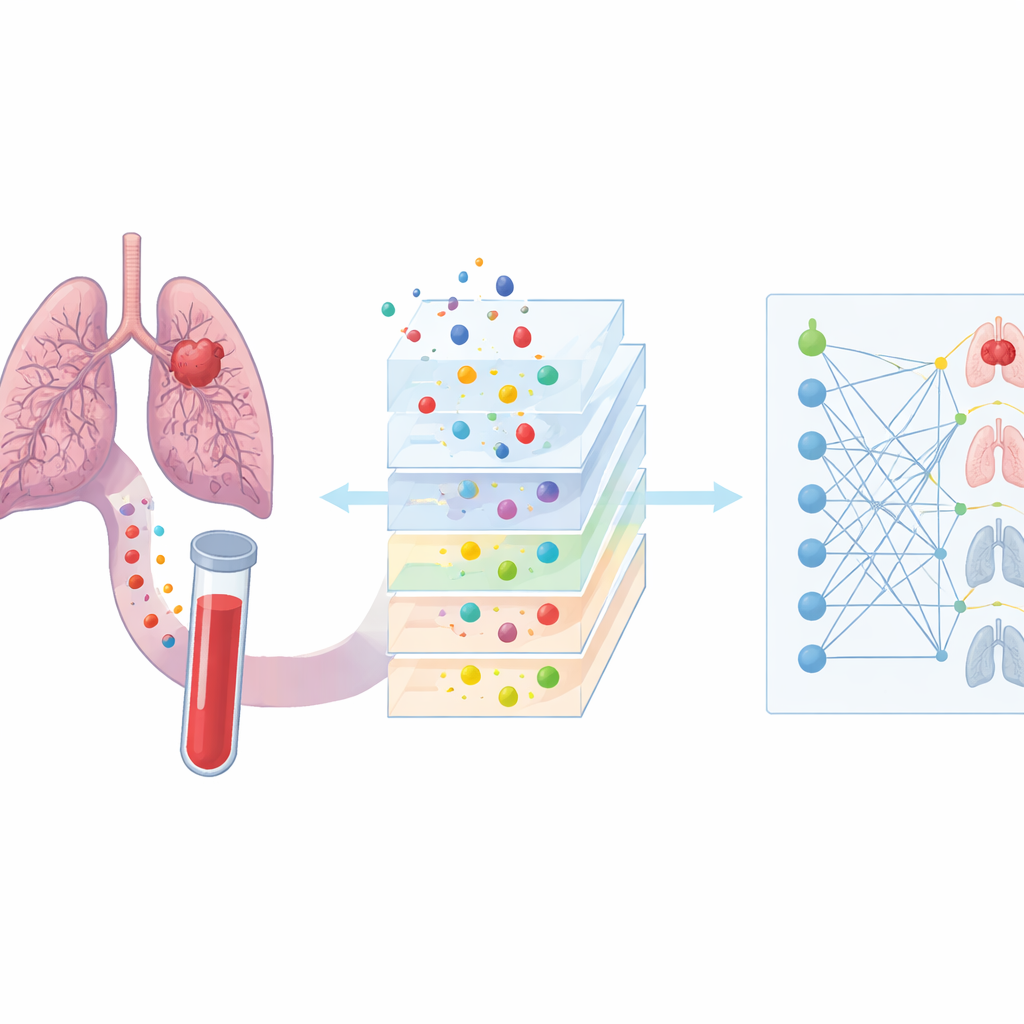
Vad detta skulle kunna innebära för patienter
Studien antyder att integrering av tumör-DNA-signaler från ett blodprov i prediktionsverktyg kan skärpa läkares förmåga att bedöma vilka KOL-patienter som sannolikt har lungcancer. Även om denna metod inte är tillräckligt exakt för att ersätta lågdos-CT eller fungera som ett fristående screeningtest, kan den hjälpa till att tolka osäkra röntgenfynd, minska onödiga invasiva biopsier hos sårbara patienter med sköra lungor och rikta närmare uppföljning mot dem med högst risk. Större, mer mångfacetterade studier och bredare DNA-paneler kommer att behövas, men arbetet pekar mot en framtid där ett enkelt blodprov, tolkat genom avancerade algoritmer, hjälper till att styra säkrare och mer personligt anpassade utvärderingar av lungcancer hos personer med KOL.
Citering: Cha, S., Shin, S.H., Shin, SH. et al. Integration of circulating tumor DNA data enhances lung cancer prediction in patients with COPD. Sci Rep 16, 11806 (2026). https://doi.org/10.1038/s41598-026-41720-y
Nyckelord: KOL, lungcancer, cirkulerande tumör-DNA, likvudbiopsi, maskininlärning