Clear Sky Science · fr
Intégration des données d’ADN tumoral circulant améliore la prédiction du cancer du poumon chez les patients atteints de BPCO
Pourquoi cela compte pour les personnes atteintes de maladie pulmonaire chronique
Les personnes vivant avec une bronchopneumopathie chronique obstructive (BPCO) présentent un risque beaucoup plus élevé de développer un cancer du poumon, mais détecter un cancer tôt dans des poumons déjà endommagés est notoirement difficile et nécessite souvent des biopsies risquées. Cette étude examine si un simple test sanguin captant de minuscules fragments d’ADN tumoral, combiné à des algorithmes informatiques modernes, peut mieux identifier quels patients BPCO sont les plus susceptibles d’avoir un cancer du poumon — et le faire d’une manière qui pourrait un jour épargner certains patients de procédures invasives.
Chercher des indices de cancer dans le sang
Lorsque les cellules cancéreuses se développent, elles libèrent des fragments de leur ADN dans le sang, appelés ADN tumoral circulant. Les chercheurs ont prélevé du sang chez 236 personnes ayant une BPCO modérée, environ la moitié d’entre elles ayant déjà un cancer du poumon et l’autre moitié n’en ayant pas. Plutôt que d’examiner l’ensemble du génome, ils se sont concentrés sur 24 gènes souvent altérés dans les tumeurs pulmonaires. En utilisant une méthode de séquençage très sensible, ils ont analysé chaque échantillon sanguin à la recherche de mutations caractéristiques et ont aussi mesuré la quantité d’ADN muté présente ainsi que la force du signal par rapport au bruit de fond.
Ajouter des algorithmes intelligents aux facteurs de risque traditionnels
En parallèle du test sanguin, l’équipe a rassemblé des informations cliniques détaillées pour chaque participant, incluant l’âge, le sexe, les antécédents tabagiques, la fonction pulmonaire, des marqueurs sanguins d’inflammation et des questionnaires sur les symptômes respiratoires. Ils ont ensuite introduit 40 éléments d’information — mesures cliniques plus caractéristiques génomiques et moléculaires issues du sang — dans neuf modèles d’apprentissage automatique différents. Ces modèles comprenaient des approches statistiques familières et des méthodes de reconnaissance de formes plus flexibles capables de détecter des relations subtiles et non linéaires entre les variables. L’objectif était simple : apprendre à l’ordinateur à distinguer les patients BPCO atteints d’un cancer du poumon de ceux qui ne le sont pas.
Ce qui distinguait les patients atteints de cancer
Plusieurs différences nettes sont apparues entre les deux groupes. Les patients BPCO atteints d’un cancer du poumon étaient plus susceptibles d’être de forts fumeurs et d’avoir des taux plus élevés de protéine C‑réactive, un marqueur sanguin lié à l’inflammation chronique. Fait surprenant, ils déclaraient en général moins de symptômes de BPCO que les patients sans cancer, ce qui reflète probablement des différences dans la manière et le moment où chaque groupe a consulté. Du côté de l’ADN, le contraste était encore plus marqué : les mutations liées à la tumeur dans le sang et les gènes « pilotes » classiques du cancer du poumon — en particulier le bien connu suppresseur de tumeur TP53 — apparaissaient beaucoup plus fréquemment chez les personnes atteintes de cancer, et leurs fragments d’ADN tumoral affichaient un soutien moléculaire plus fort dans les données de séquençage.
Prédictions plus robustes lorsque les données d’ADN sont incluses
Lorsque les chercheurs ont entraîné leurs modèles en n’utilisant que les informations cliniques traditionnelles, la précision des prédictions était modeste. Mais lorsqu’ils ont ajouté les signaux d’ADN tumoral et les mesures moléculaires associées, les performances se sont nettement améliorées, en particulier pour les modèles plus flexibles et non linéaires. Le meilleur modèle, une machine à vecteurs de support radiale, a montré une sensibilité plus élevée (identifiant davantage de vrais cas de cancer), un meilleur équilibre entre faux positifs et faux négatifs, et une aire sous la courbe plus grande, une mesure standard de la précision globale. Fait important, les prédicteurs les plus influents dans ce modèle combiné n’étaient plus seulement le tabagisme et l’inflammation, mais aussi la présence de mutations d’ADN tumoral, la force du signal de séquençage et les mutations de TP53.
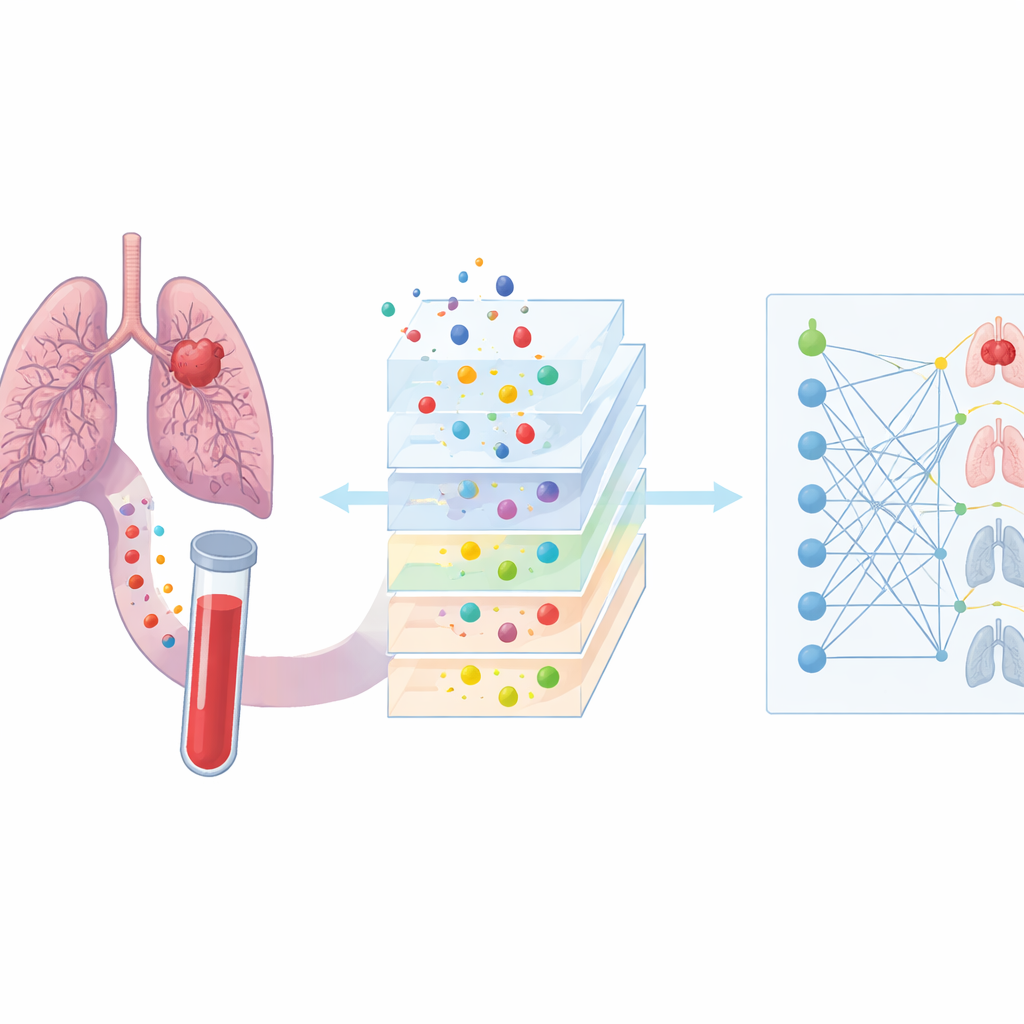
Ce que cela pourrait signifier pour les patients
L’étude suggère qu’intégrer les signaux d’ADN tumoral issus d’un prélèvement sanguin dans des outils de prédiction peut affiner la capacité des médecins à évaluer quels patients BPCO sont les plus susceptibles d’héberger un cancer du poumon. Bien que cette approche ne soit pas encore suffisamment précise pour remplacer les scanners thoraciques basse dose ou servir de test de dépistage autonome, elle pourrait aider à interpréter des résultats d’imagerie incertains, réduire les biopsies invasives inutiles chez des patients vulnérables aux poumons fragiles et concentrer un suivi rapproché sur les personnes à plus haut risque. Des études plus larges et plus diversifiées et des panels d’ADN plus étendus seront nécessaires, mais ce travail ouvre la voie vers un avenir où un simple échantillon de sang, interprété par des algorithmes avancés, contribue à orienter une évaluation du cancer du poumon plus sûre et plus personnalisée chez les personnes vivant avec la BPCO.
Citation: Cha, S., Shin, S.H., Shin, SH. et al. Integration of circulating tumor DNA data enhances lung cancer prediction in patients with COPD. Sci Rep 16, 11806 (2026). https://doi.org/10.1038/s41598-026-41720-y
Mots-clés: BPCO, cancer du poumon, ADN tumoral circulant, biopsie liquide, apprentissage automatique