Clear Sky Science · sv
Fluorescensbaserad kartläggning av kondensaters dielektriska permitivitet avslöjar hydrofobicitetsdrivna membraninteraktioner
Varför droppar inne i celler spelar roll
Inne i våra celler sker många viktiga reaktioner inte i hårda avgränsade fack utan i mjuka, vätskeliknande droppar kallade biomolekylära kondensat. Dessa små droppar hjälper till att organisera cellens trånga inre och styr var och när kemi får ske. Ändå har en grundläggande fråga varit oklar: vad får vissa droppar att fastna vid cellmembran medan andra håller sig borta? Den här studien visar att en enkel fysisk egenskap — hur lätt ett material svarar på elektriska fält, tätt kopplad till hur vattnigt eller oljeaktigt det är — kan förklara och till och med förutsäga hur dessa droppar interagerar med membran.

Att se osynliga egenskaper med ljus
Författarna utvecklade ett sätt att ”se” den lokala elektriska miljön inne i och runt dropparna med hjälp av en särskild fluorescerande färgämne kallat ACDAN. När detta färgämne exciteras av ljus skiftar dess färg beroende på hur fritt närliggande vattenmolekyler kan röra sig och orientera sig, vilket i sin tur speglar den lokala dielektriska permitiviteten — ett mått på hur polärt eller hydrofobt omgivningen är. Genom att spela in ett fullständigt spektrum av utsända färger vid varje pixel i en mikroskopbild och analysera dessa spektra matematiskt, omvandlar teamet färginformationen till en kvantitativ karta över permitivitet med pixelnivåupplösning.
Droppar från oljeaktiga till vattenlika
Med denna optiska metod undersökte forskarna en mängd modellkondensat gjorda av proteiner, korta peptider och polymerer. De upptäckte att dropparna spänner över ett förvånansvärt vidsträckt spektrum av dielektriska permitiviteter, från värden liknande oljor till värden som närmar sig rent vatten. Det innebär att kondensat kan vara mycket mer hydrofoba eller hydrofila än man tidigare uppskattat. De fann också att typen av fasskillnadskemistry (till exempel laddade polymerer som binder ihop kontra neutrala molekyler som separerar) inte räcker för att förutsäga permitiviteten. Istället spelar faktorer som hur mycket vatten som fångas in i den täta fasen och hur proteiner är strukturerade och packade en avgörande roll.
Att följa trängsel och kemiska förändringar
Teamet använde sedan permitivitetskartor för att följa hur droppar och deras omgivning förändras när den övergripande blandningen justeras. I klassiska vattenbaserade blandningar av två polymerer, och i proteinrika kondensat, ändrade ökad trängsel eller saltkoncentration vatteninnehållet och därmed permitiviteten hos både de täta dropparna och den mer utspädda fasen utanför. Tillsats av små mängder ATP — en molekyl mest känd som cellens energivaluta — fungerade som en ”hydrotrop”, som subtilt luckrade upp interaktioner, ökade vatteninnehållet och skiftade permitiviteten hos de samexisterande faserna på olika sätt. Dessa förändringar kunde detekteras känsligt av färgämnet, även när konventionella sammansättningsmätningar vore svåra.
Hur droppar avgör att våta membran
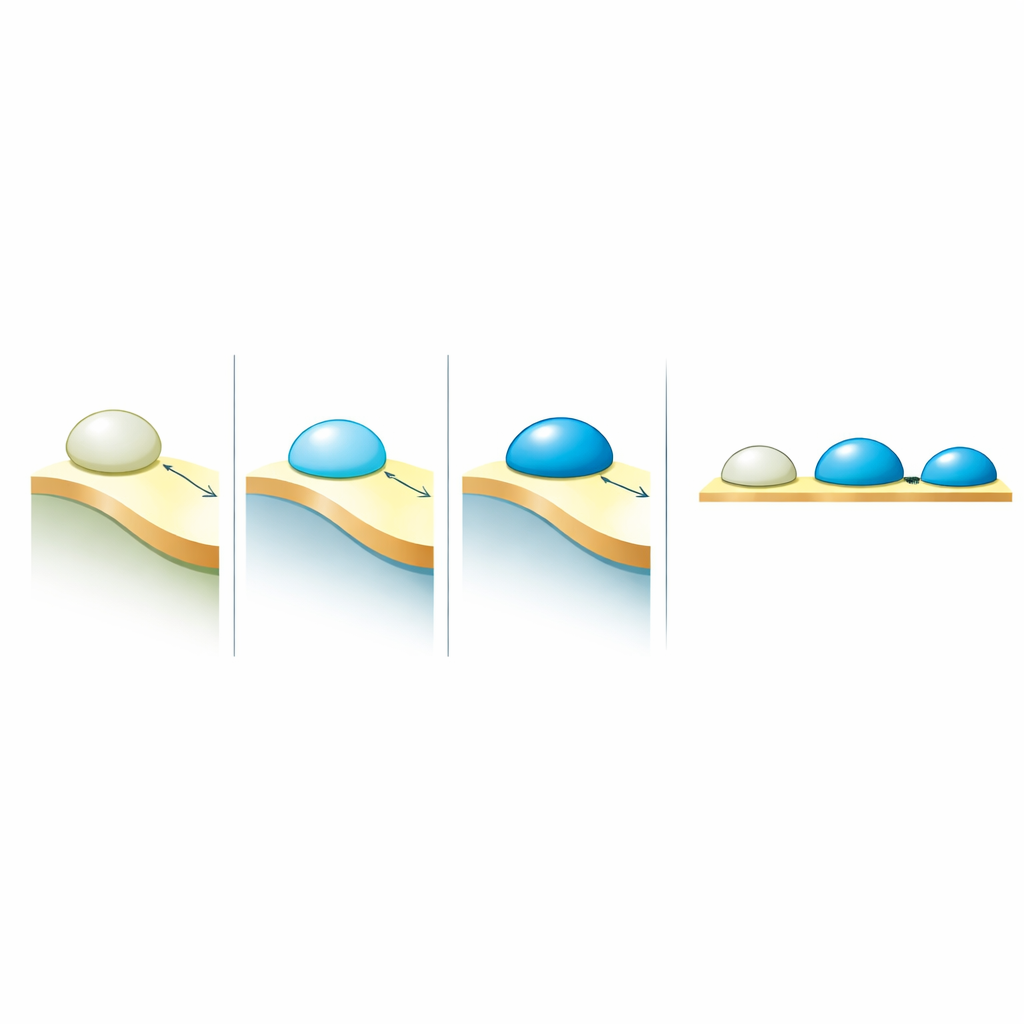
Den centrala biologiska frågan var hur dessa elektriska egenskaper relaterar till hur dropparna beter sig vid membran. När ett kondensat kommer i kontakt med ett lipidmembran kan det knappt fästa, delvis sprida ut sig eller starkt våta och omforma membranet. Detta beteende fångas av en kontaktvinkel — ett geometriskt mått på hur mycket droppen sprider sig. Genom att jämföra många system från tidigare experiment fann författarna en enkel regel: graden av vättning ökar linjärt med permitivitetskontrasten mellan det täta kondensatet och den omgivande utspädda fasen. Med andra ord är det inte den absoluta ”polariteten” hos droppen som främst spelar roll, utan hur annorlunda den är jämfört med det som omger den. Större kontraster ger starkare attraktion till membran, medan mindre kontraster försvagar denna affinitet.
Varför detta är viktigt för celler och sjukdom
Dessa fynd avslöjar en enhetlig fysisk princip för hur mjuka droppar inne i celler interagerar med membran: membranaffinitet bestäms av dielektrisk mismatch mellan samexisterande faser, snarare än av kondensatets egenskaper ensamt. Eftersom molekyler som ATP kan justera denna kontrast genom att förändra lokal vattenstruktur kan celler använda sådana små lösta ämnen för att reglera var kondensat bildas, vilka membran de fäster vid och hur de hjälper till att reparera eller omforma dessa membran. Den kartläggningsmetod som introduceras här, och som är kompatibel med avbildning i levande celler, öppnar ett nytt fönster mot kondensaters dolda elektriska landskap och kan hjälpa till att förklara hur förändringar i trängsel, hydrering och droppåldrande bidrar till hälsa och sjukdom.
Citering: Sabri, E., Mangiarotti, A. & Dimova, R. Fluorescence-based mapping of condensate dielectric permittivity uncovers hydrophobicity-driven membrane interactions. Nat Commun 17, 3155 (2026). https://doi.org/10.1038/s41467-026-71273-7
Nyckelord: biomolekylära kondensat, dielektrisk permitivitet, membranvättning, fluorescensavbildning, cellulär fasskillnad