Clear Sky Science · nl
Fluorescentie-gebaseerde kartografie van de diëlectrische permittiviteit van condensaten onthult hydrofobiciteit-gedreven membraaninteracties
Waarom druppels binnen cellen ertoe doen
Binnen onze cellen vinden veel cruciale reacties niet plaats in harde compartimenten, maar in zachte, vloeibare druppels die biomoleculaire condensaten worden genoemd. Deze kleine druppels helpen het drukke binnenste van de cel te organiseren en bepalen waar en wanneer chemie plaatsvindt. Toch bleef één fundamentele vraag onduidelijk: waarom blijven sommige druppels aan cellulaire membranen kleven terwijl andere wegblijven? Deze studie toont aan dat een eenvoudige fysieke eigenschap — hoe gemakkelijk een materiaal reageert op elektrische velden, nauw verbonden met hoe waterig of olieachtig het is — kan verklaren en zelfs voorspellen hoe deze druppels met membranen interageren.

Onzichtbare eigenschappen zichtbaar maken met licht
De auteurs ontwikkelden een methode om de lokale elektrische omgeving in en rond druppels te “zien” met een speciale fluorescente kleurstof genaamd ACDAN. Wanneer deze kleurstof door licht wordt aangeslagen, verschuift de kleur afhankelijk van hoe vrij nabijgelegen watermoleculen kunnen bewegen en heroriënteren, wat op zijn beurt de lokale diëlectrische permittiviteit weerspiegelt — een maat voor hoe polair of hydrofoob de omgeving is. Door op elk pixel in een microscoopbeeld een volledig spectrum van uitgezonden kleuren op te nemen en die spectra wiskundig te analyseren, zet het team kleurinformatie om in een kwantitatieve kaart van permittiviteit met pixel-niveau resolutie.
Druppels van olieachtig tot waterachtig
Met deze optische methode onderzochten de onderzoekers een verscheidenheid aan modelcondensaten gemaakt van eiwitten, korte peptiden en polymeren. Ze ontdekten dat druppels een verrassend breed spectrum van diëlectrische permittiviteiten bestrijken, van waarden vergelijkbaar met oliën tot waarden die die van puur water benaderen. Dit betekent dat condensaten veel hydrofober of hydrofiler kunnen zijn dan eerder werd gedacht. Ze vonden ook dat het soort fase-scheidingschemie (bijvoorbeeld geladen polymeren die aan elkaar plakken versus neutrale moleculen die scheiden) niet voldoende is om permittiviteit te voorspellen. In plaats daarvan maken factoren zoals hoeveel water in de dichte fase gevangen zit en hoe eiwitten zijn gevouwen en verpakt een groot verschil.
Bevolkings- en chemische veranderingen volgen
Het team gebruikte vervolgens permittiviteitskaarten om te volgen hoe druppels en hun omgeving veranderen wanneer het totale mengsel wordt aangepast. In klassieke waterige mengsels van twee polymeren, en in eiwitrijke condensaten, veranderden toenemende dichtheid of zoutconcentratie het watergehalte en daarmee de permittiviteit van zowel de dichte druppels als de meer verdunde fase eromheen. Het toevoegen van kleine hoeveelheden ATP — een molecuul vooral bekend als de energievaluta van de cel — werkte als een “hydrotroop”, waardoor interacties subtiel werden losgemaakt, het watergehalte toenam en de permittiviteit van de coëxisterende fasen op verschillende manieren verschoven. Deze veranderingen konden gevoelig door de kleurstof worden gedetecteerd, zelfs wanneer conventionele samenstellingsmetingen moeilijk zouden zijn geweest.
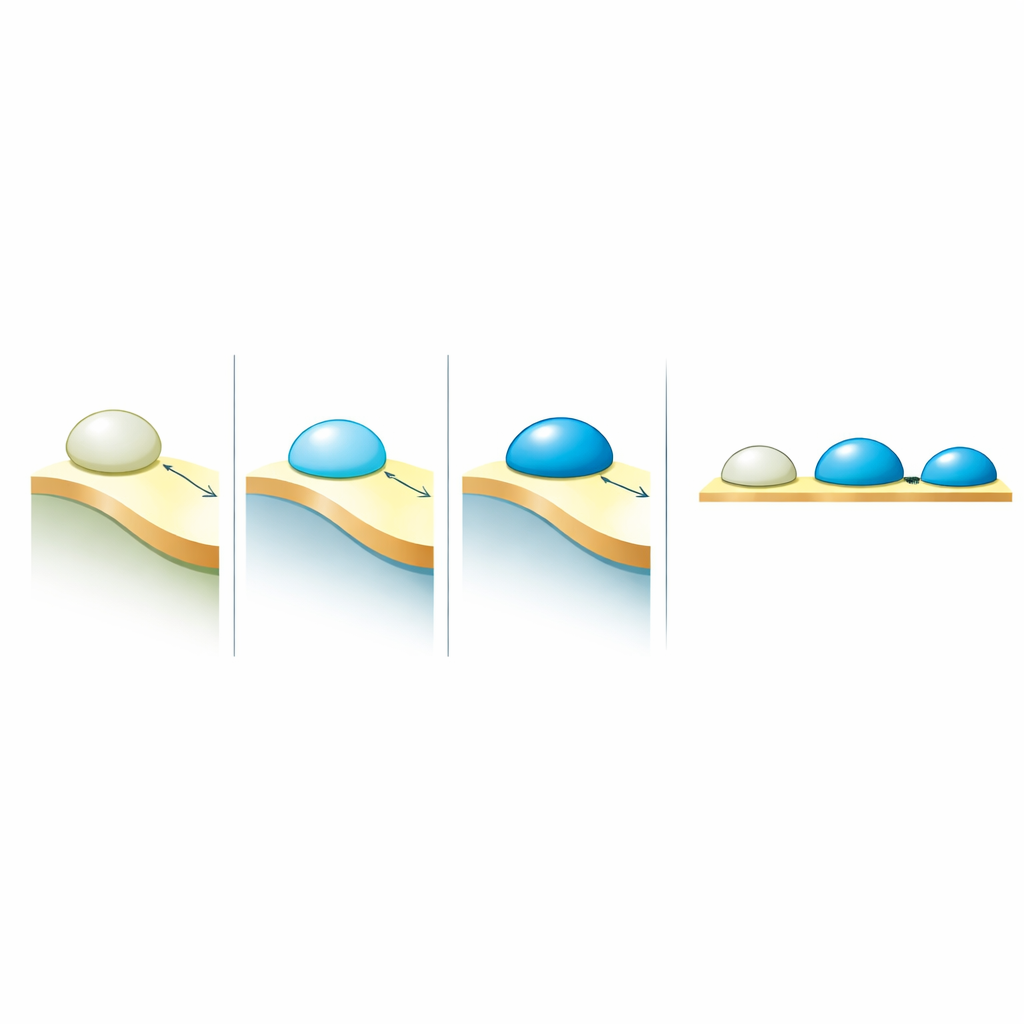
Hoe druppels beslissen membranen te bevochtigen
De belangrijkste biologische vraag was hoe deze elektrische eigenschappen zich verhouden tot het gedrag van druppels aan membranen. Wanneer een condensaat een lipide-membraan raakt, kan het nauwelijks hechten, gedeeltelijk uitspreiden of sterk bevochtigen en het membraan vervormen. Dit gedrag wordt vastgelegd door een contacthoek — een geometrische maat voor hoe ver de druppel zich verspreidt. Door vele systemen uit eerdere experimenten te vergelijken, vonden de auteurs een eenvoudige regel: de mate van bevochtiging neemt lineair toe met het permittiviteitscontrast tussen het dichte condensaat en de omringende verdunde fase. Met andere woorden: het is niet de absolute “polariteit” van de druppel die het meest telt, maar hoe verschillend die is van de omgeving. Grotere contrasten veroorzaken sterkere aantrekking tot membranen, terwijl kleinere contrasten die affiniteit verzwakken.
Waarom dit belangrijk is voor cellen en ziekte
Deze bevindingen onthullen een verenigend fysisch principe voor hoe zachte druppels binnen cellen met membranen interageren: membraanaffiniteit wordt bepaald door het diëlectrische verschil tussen coëxisterende fasen, in plaats van alleen door eigenschappen van het condensaat. Omdat moleculen zoals ATP dit contrast kunnen bijstellen door de lokale waterstructuur te wijzigen, kunnen cellen dergelijke kleine opgeloste stoffen gebruiken om te reguleren waar condensaten ontstaan, aan welke membranen ze zich hechten en hoe ze helpen die membranen te herstellen of te vervormen. De hier geïntroduceerde mappingmethode, compatibel met live-celbeeldvorming, biedt een nieuw venster op de verborgen elektrische landschappen van condensaten en kan helpen verklaren hoe veranderingen in dichtheid, hydratatie en veroudering van druppels bijdragen aan gezondheid en ziekte.
Bronvermelding: Sabri, E., Mangiarotti, A. & Dimova, R. Fluorescence-based mapping of condensate dielectric permittivity uncovers hydrophobicity-driven membrane interactions. Nat Commun 17, 3155 (2026). https://doi.org/10.1038/s41467-026-71273-7
Trefwoorden: biomoleculaire condensaten, diëlectrische permittiviteit, membraanbevochtiging, fluorescentiebeeldvorming, cellulaire fase-scheiding