Clear Sky Science · sv
Dubbel dekonvolution i multiphoton-strukturerad belysningsmikroskopi för djupvävnads superupplösningsavbildning
Se djupare in i levande vävnad
Modern biologi är ofta beroende av att kunna se de minsta detaljerna inne i tjocka vävnadsstycken, som hjärnskivor eller utvecklande embryon. Tyvärr böjs och skruvas ljuset när det färdas genom dessa täta miljöer, vilket gör bilder suddiga precis när forskare allra mest behöver skarpa vyer. Denna artikel presenterar ett sätt att digitalt "avskumma" dessa bilder, vilket gör det möjligt för ett vanligt avancerat mikroskop att avslöja extremt fina strukturer djupt i vävnaden utan att man behöver lägga till dyr och komplex hårdvara.
Varför djupavbildning är så svår
Fluorescensmikroskop låter forskare märka specifika molekyler och följa hur celler och vävnader byggs upp och beter sig. Under de senaste decennierna har flera "superupplösnings"-metoder överträffat de traditionella skärpegränserna och avslöjat detaljer långt under 200 nanometer. De flesta av dessa metoder fungerar dock bara väl nära provytan. I tjocka vävnader, såsom mössens hjärna, förvanskas både det ljus som exciterar fluorescensen och det ljus som avges tillbaka till detektorn av små variationer i vävnadens struktur. Dessa förvrängningar, kallade aberrationer, suddar ut mikroskopets fokus och raderar högdetaljerad information, särskilt på djup större än några tiotals mikrometer.
Från hårdvarulösningar till en mjukvarulösning
Ett vanligt sätt att motverka aberrationer är hårdvarubaserad adaptiv optik, som använder rörliga speglar eller andra enheter för att omforma ljusets vågfront och återställa ett skarpt fokus. Även om dessa system är kraftfulla är de dyra, tekniskt krävande och korrigerar ofta bara för ett färgområde eller en ljusriktning åt gången. Författarna föreslår istället en beräkningsbaserad metod som fungerar med en typ av mikroskop som redan är vanligt i många labb: ett laserskannande multiphoton-mikroskop. Genom att byta ut den vanliga enkla ljusdetektorn mot en kamera spelar de in en rik uppsättning skannade bilder som kodar hur både det inkommande exciteringsljuset och den utgående fluorescensen har förvrängts av vävnaden.
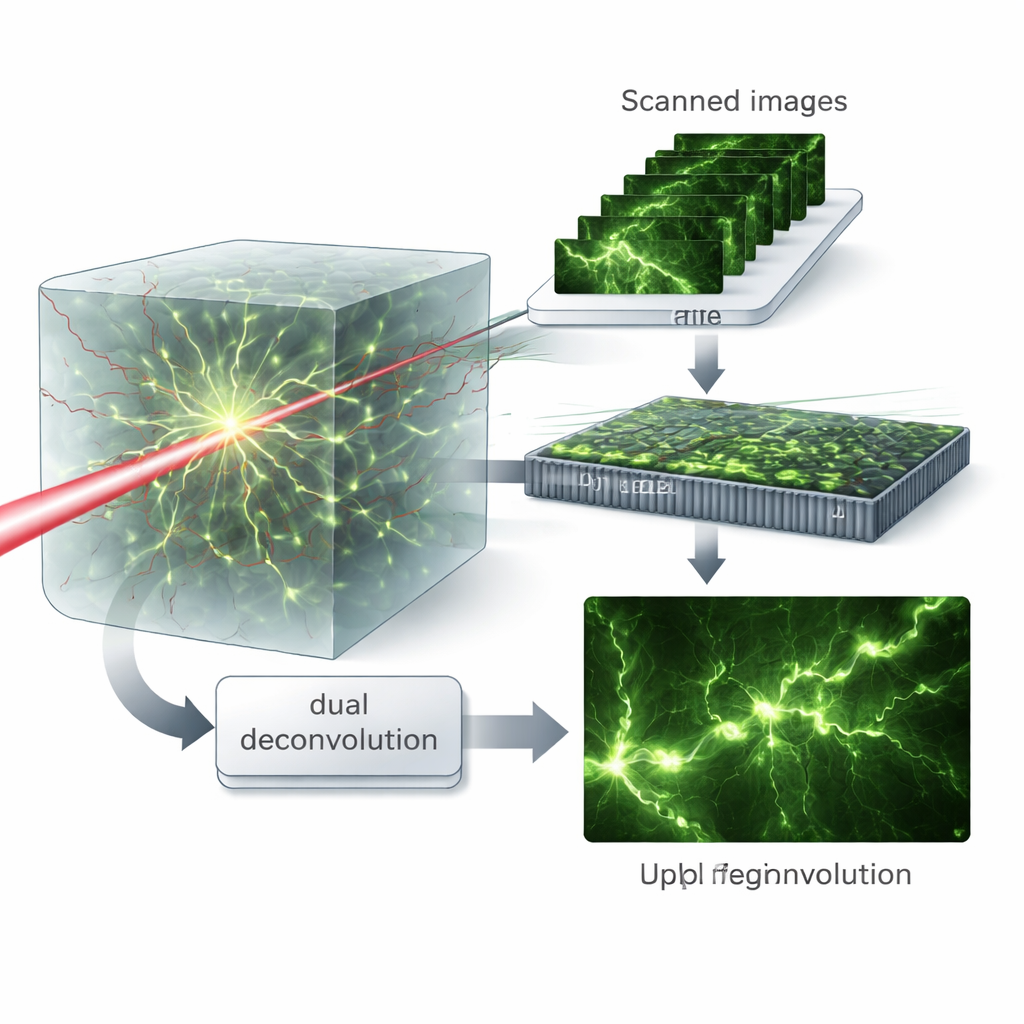
Virtuella mönster och dubbelrensning
Nyckelinsikten är att behandla de skannade bilderna som om provet hade belysts med många olika fina ljusmönster, ett begrepp författarna kallar virtuell strukturerad belysning. Genom att matematiskt återkombinera dessa data i frekvensdomänen kan de separera rollerna för exciterings- och emissionsprocesserna. De introducerar sedan en "dubbel dekonvolution"-algoritm som växelvis skattar och korrigerar oskärpan från vardera sidan — ljuset som går in och ljuset som kommer ut — snarare än att slå ihop dem till en enda effektiv oskärpa. Denna matrisbaserade behandling bevarar fler högfrekventa detaljer och gör det möjligt för algoritmen att återvinna fina strukturer även när aberrationerna är starka.
Skarpare vyer i simuleringar och riktiga prover
För att testa sin metod använde teamet först datorbaserade simuleringar av tvåfotonmikroskopi, en djupavbildningsteknik som använder par av lägre-energi-fotoner för att excitera fluorescens endast i fokuspunkten. Vid kraftiga simulerade förvrängningar gav konventionella tvåfoton- och standard strukturerad belysningsrekonstruktion märkbart suddiga bilder. I kontrast återställde dubbel dekonvolution skarpa mönster med en upplösning som närmade sig en fjärdedel av fluorescensens våglängd — ungefär 130 nanometer — i linje med teoretiska förväntningar. Författarna byggde sedan en specialanpassad tvåfotonuppställning med en vetenskaplig kamera och tillämpade sin algoritm på riktiga prover, inklusive fluorescerande kulor, testmönster gömda bakom spridande lager, cellkulturer, mus hjärnvävnad och helmonterade zebrafiskar. Om och om igen framträdde strukturer som i konventionella bilder verkade utsmetade eller dubbla som klart åtskilda efter bearbetning, och fina neurala element som dendritiska ryggradsspetsar förblev upplösliga på djup upp till 180 mikrometer i mössens hjärna.
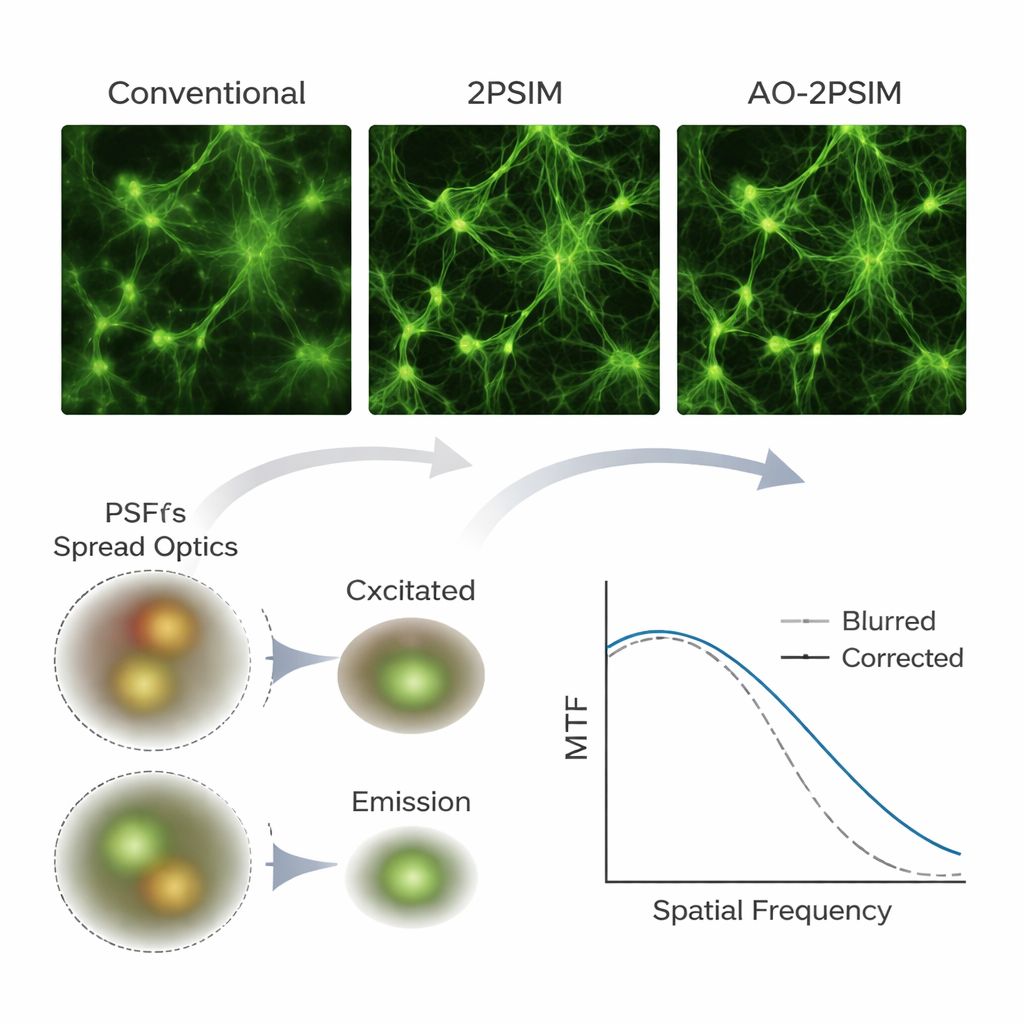
Vad detta betyder för biologisk avbildning
För icke-specialister är huvudbudskapet att författarna har visat hur befintliga multiphoton-mikroskop kan förvandlas till betydligt kraftfullare verktyg för djupvävnadsavbildning främst med hjälp av mjukvara och en kamerauppgradering. Genom att noggrant modellera och korrigera hur vävnader böjer ljus både på in- och utsidan fördubblar deras dubbel dekonvolution den vanliga upplösningsgränsen i utmanande, tjocka prover utan att förlita sig på komplexa adaptiva speglar. Metoden är fortfarande beroende av att samla tillräckligt med signal och kräver i dagsläget relativt långsam skanning, men erbjuder en praktisk och kostnadseffektiv väg mot rutinmässiga, ultraskarpa vyer av hjärnan och andra organ i tre dimensioner, vilket öppnar dörren för mer detaljerade studier av hur biologiska strukturer är organiserade och förändras över tid.
Citering: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Nyckelord: superupplösningsmikroskopi, tvåfotonavbildning, adaptiv optik, djupvävnadsavbildning, beräkningsbaserad avbildning