Clear Sky Science · sv
Acyl‑CoA‑bindande protein (ACBP): en dålig prognos‑biomarkör vid sepsis och ett mål för sjukdomsbegränsning
Varför detta är viktigt för personer med svåra infektioner
Sepsis, en livshotande reaktion på infektion, är fortfarande en av de största dödsorsakerna på intensivvårdsavdelningar. Även med moderna antibiotika och livsuppehållande behandlingar dör många patienter och överlevande drabbas ofta av långvariga hälsoproblem. Denna studie identifierar ett litet protein i blodet, kallat acyl‑CoA‑bindande protein (ACBP), både som en varningssignal för fara och som en aktiv drivkraft i den skada som ses vid sepsis. Den antyder också en ny behandlingsstrategi som kan fungera tillsammans med befintlig steroidbehandling för att rädda fler liv.
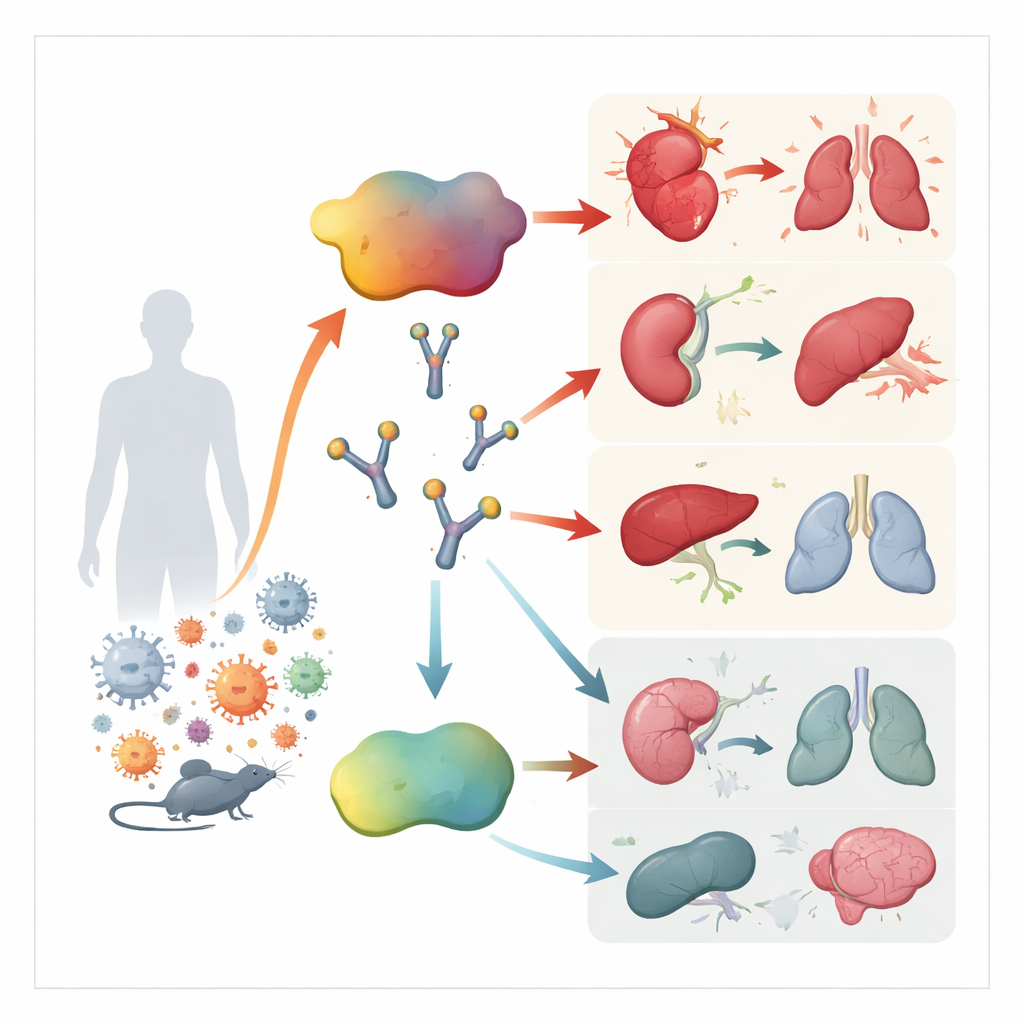
Ett stressignal som blir skadlig
ACBP deltar normalt i hantering av fetter inne i celler, men det kan också släppas ut i blodomloppet som en slags stresshormon. Tidigare arbete visade att höga nivåer av detta protein uppträder hos personer med inflammatoriska sjukdomar och att det kan få immunceller att släppa ut fler inflammatoriska molekyler. Författarna undrade om ACBP kunde vara en del av den okontrollerade immunreaktion som kännetecknar sepsis, och om blockering av proteinet skulle kunna hjälpa till att återställa balansen.
En blodmarkör som följer vilka som blir sjukare
Teamet mätte först ACBP‑nivåer i två patientgrupper: en liten "upptäckts"‑grupp på intensivvård och en mycket större "validerings"‑grupp på akutmottagningen. I båda grupperna hade patienter med sepsis och septisk chock mycket högre ACBP‑nivåer än friska kontrollpersoner eller patienter med icke‑infektiös inflammation. Inom sepsesgrupperna tenderade de som senare avled att ha de högsta ACBP‑koncentrationerna. Dessa nivåer korrelerade väl med etablerade svårighetsgrader och med blodtecken på hjärt‑, njur‑ och leverskador. Faktum är att ACBP förutsade död ungefär lika bra som komplexa poängsystem som används inom intensivvården, och bättre än vanliga blodprover som C‑reaktivt protein och prokalcitonin.
Att blockera proteinet skyddar organ hos djur
För att avgöra om ACBP bara var en markör eller faktiskt bidrog till problemet, använde forskarna flera musemodeller av sepsis. De studerade en steril modell driven av bakteriellt toxin, en infektion med levande Escherichia coli och en polymikrobiell "smutsig kirurgi"‑modell som nära efterliknar mänsklig buksepsis. I samtliga steg steg ACBP‑nivåerna i blodet kraftigt efter utmaning. När mössen behandlades med en monoklonal antikropp som neutraliserar ACBP, eller när ACBP‑genen togs bort, var djuren mycket mer benägna att överleva. De bibehöll kroppstemperaturen bättre, frisatte färre inflammatoriska cytokiner och visade mindre tecken på skador i hjärta, njurar, lever och lungor. Omvänt gjorde tillsats av extra ACBP toxininducerad sepsis mer dödlig, vilket underströk dess skadliga roll.
Hjälper immunceller att rensa bort bakterier mer effektivt
Studien utforskade också hur ACBP påverkar frontlinjens immunceller. I möss infekterade med E. coli eller utsatta för polymikrobiell peritonit minskade blockering av ACBP antalet levande bakterier i blod, peritonealvätska och organ. När makrofager eller neutrofiler uttömdes försvann denna fördel i stor utsträckning, vilket pekar på dessa celler som nyckelaktörer. I provrör gjorde antikroppen neutrofiler och en undergrupp av makrofager mer effektiva på att svälja och döda bakterier. Detaljerad immunprofilering i sepsiska möss visade att neutralisering av ACBP förskjöt myeloida celler från starkt inflammatoriska till mer vävnadsskyddande profiler, samtidigt som breda analyser av genuttryck och metaboliter visade en återgång mot normal funktion i flera organ.
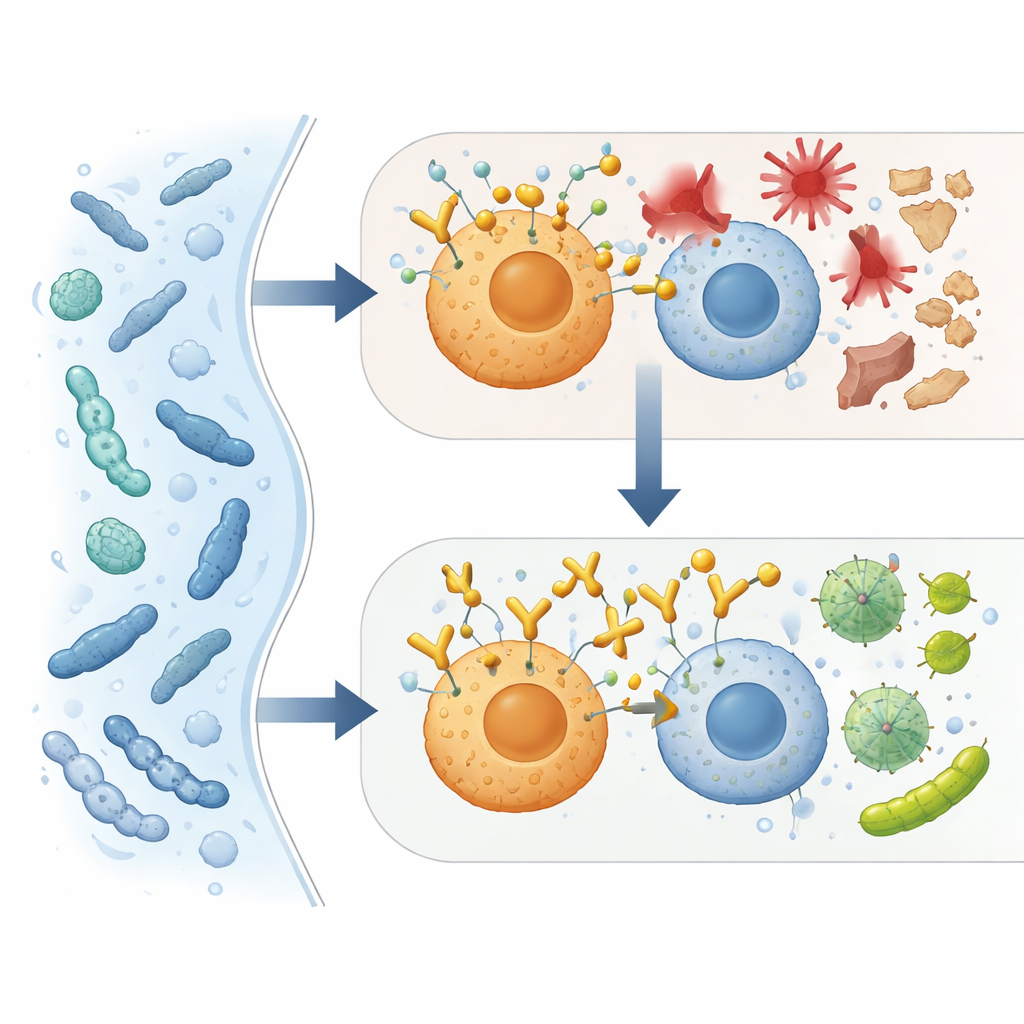
Samarbete med steroider i stället för konflikt
Många patienter med septisk chock får glukokortikoider som dexametason för att dämpa överdriven inflammation, men dessa steroider kan också höja ACBP‑nivåerna och ge skadliga metabola biverkningar. Författarna testade om blockering av ACBP skulle stå i konflikt med eller komplettera steroidbehandling hos möss. I både toxin‑drivna och kirurgiska sepsismodeller förbättrade kombinationen av anti‑ACBP‑antikropp och dexametason i allmänhet överlevnad, kliniska poäng och organfunktion jämfört med någon av behandlingarna ensamma. Viktigt är att steroidernas fördelaktiga antiinflammatoriska effekter bevarades, medan molekylära tecken på skadlig metabol omprogrammering normaliserades av ACBP‑blockaden. Dessa fynd tyder på att ACBP‑inhibering skulle kunna separera steroiders kortsiktiga fördelar från deras långsiktiga nackdelar.
Vad detta kan innebära för framtidens sepsisvård
Sammantaget framträder ACBP som en central förstärkare av de skadliga responser som omvandlar en svår infektion till dödlig sepsis. Höga nivåer av proteinet i blodet varnar kliniker att en patient löper större risk för organsvikt och död, medan experiment i möss visar att neutralisering av ACBP både kan dämpa inflammatorisk överreaktion och stärka kroppens förmåga att avlägsna angripande mikrober. Även om dessa resultat fortfarande måste bekräftas i kliniska studier på människor, pekar de mot en framtid där en riktad antikropp mot ACBP, eventuellt i kombination med standardsteroider, skulle kunna bryta den dödliga spiralen vid septisk chock och förbättra både överlevnad och långsiktig återhämtning.
Citering: Lambertucci, F., Motiño, O., Nogueira-Recalde, U. et al. Acyl-CoA-binding protein (ACBP): a poor-prognosis biomarker in sepsis and a target for disease mitigation. Sig Transduct Target Ther 11, 119 (2026). https://doi.org/10.1038/s41392-026-02670-z
Nyckelord: sepsis, biomarkörer, immunsvar, monoklonala antikroppar, glukokortikoider