Clear Sky Science · ru
Согласование доноров и реципиентов при трансплантации печени с помощью офлайн-обучения с подкреплением
Почему эти решения при трансплантации печени имеют значение
Для людей с тяжёлыми заболеваниями печени получение трансплантата может решить — жить или умереть, — но донорских печеней гораздо меньше, чем пациентов, которым они нужны. Врачи постоянно вынуждены решать: принять ли конкретную печень для данного пациента, продолжать ждать лучшего совпадения или снять человека с листа ожидания, если он поправился или стал слишком болен. В этом исследовании изучается, может ли разновидность искусственного интеллекта, называемая офлайн-обучением с подкреплением, научиться на многолетних данных о трансплантациях предлагать более безопасные и разумные решения по подбору, которые спасают больше жизней и лучше используют каждый донорский орган.
От одноразовых прогнозов к продолжающимся решениям
Большинство современных инструментов, применяемых при трансплантации печени, оценивают лишь один момент времени — например, день операции — и прогнозируют вероятность выживания пациента с данным донорским органом. Они часто опираются на такие показатели, как модель для конечной стадии заболевания печени (MELD), которая сводит результаты лабораторных тестов в число, помогающее отдавать приоритет наиболее тяжёлым пациентам. Но эти инструменты упускают важную часть реальности: состояние пациента меняется в течение недель и месяцев, и каждое решение принять или отклонить предложенный орган влияет на дальнейшее развитие событий, включая риск смерти в ожидании. Авторы вместо этого сформулировали задачу трансплантации как последовательность решений во времени, где каждый выбор — трансплантировать, ждать или снять с листа — ведёт к разным возможным будущим.
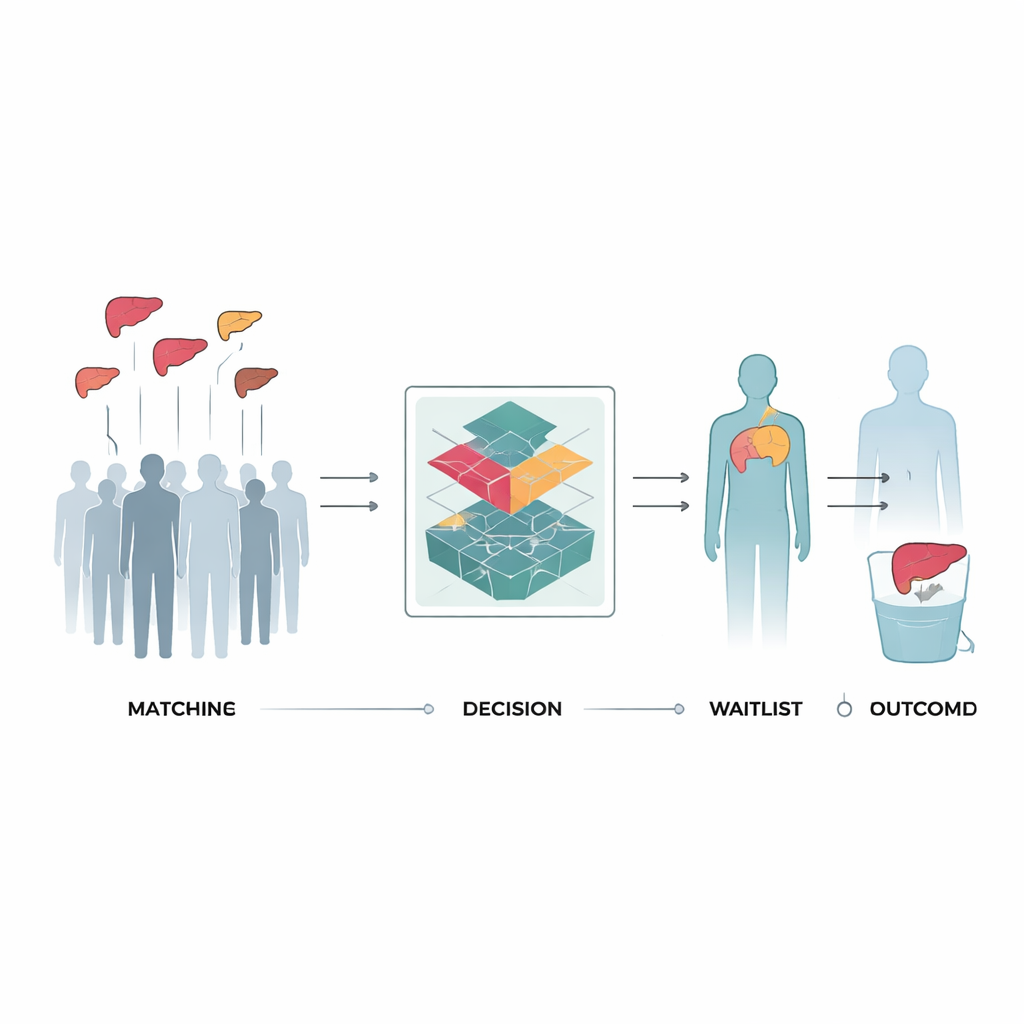
Обучение компьютера на прошлом опыте трансплантаций
Исследователи использовали записи из Американского научного реестра реципиентов трансплантатов (Scientific Registry of Transplant Recipients), сосредоточившись на более чем 43 000 взрослых, включённых в лист ожидания на первичную трансплантацию печени в период с 2017 по 2022 год. Для каждого человека они восстановили временную шкалу показателей MELD и возможных донорских предложений, включая органы, которые в итоге были утилизированы. На каждом шаге компьютер видел характеристики пациента, характеристики потенциального донора и три возможных действия: ждать, трансплантировать или удалить из листа. Затем он получал сигнал вознаграждения на основе того, что произошло позже — улучшилось ли состояние пациента или ухудшилось, была ли трансплантация успешной, неудачной или вообще не состоялась. С помощью метода, называемого Conservative Q-learning, систему обучали отдавать предпочтение решениям, которые, в сумме по множеству таких временных линий, приводили к меньшему числу смертей и неудачных трансплантаций.
Какие изменения дала бы выученная политика
Когда обученная система была протестирована на отдельной группе пациентов, она избегала 73% пар донор–реципиент, которые в реальности приводили к отторжению трансплантата или смерти в течение года после операции, при этом сохраняя 93% успешных трансплантаций. Она также выявила более ранние возможности для трансплантации почти для половины пациентов, умерших в листе ожидания, что говорит о том, что иной выбор времени или донора мог бы улучшить их шансы. Важно, что в отличие от очень агрессивных стратегий, которые просто трансплантируют почти всех при достижении серьёзной степени тяжести, этот подход ограничивал общее число пересадок, при этом улучшая результаты. В более реалистичной симуляции, где каждая донорская печень могла быть использована только один раз, а пациенты покидали пул после трансплантации или удаления, модель всё равно сумела сопоставить большинство пациентов с донорами, уменьшая при этом количество предотвратимых неудач.
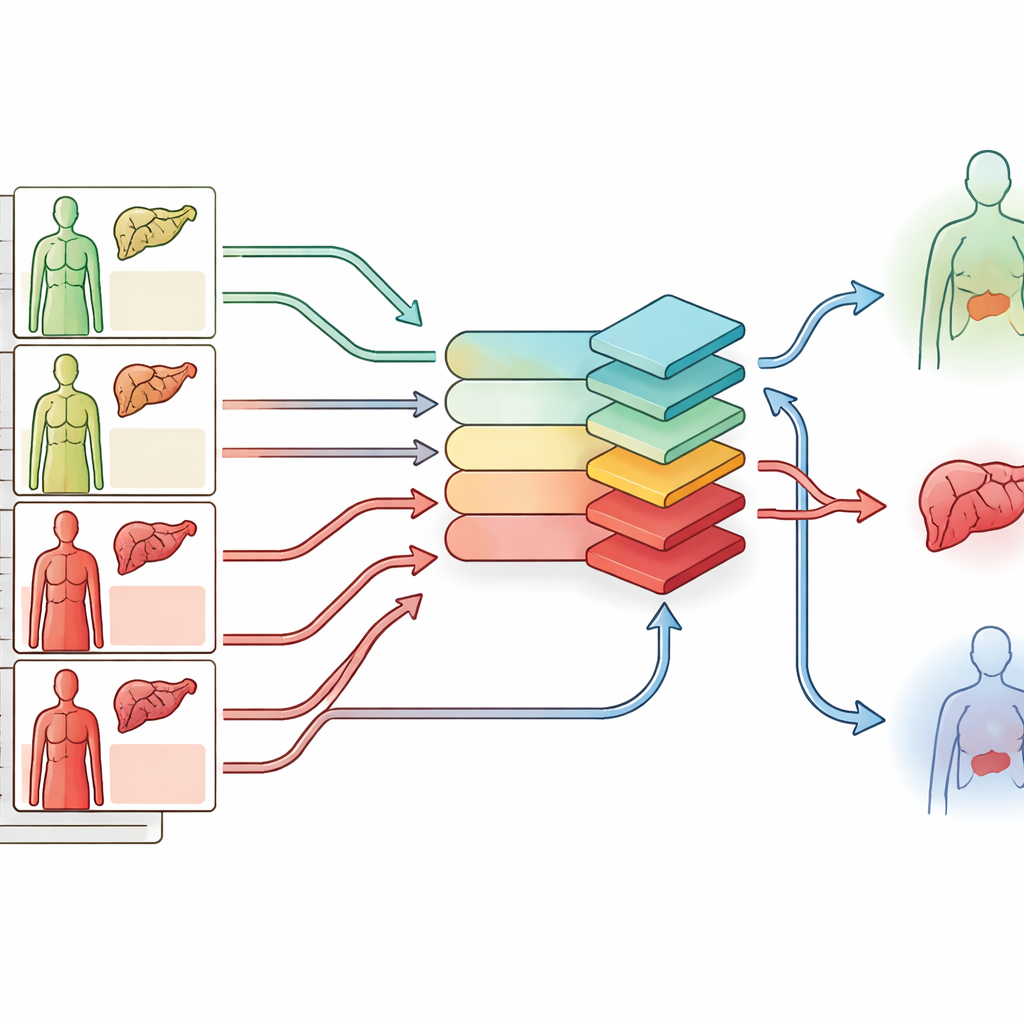
Подсказки к лучшему подбору, скрытые в данных
Помимо чистых показателей производительности, команда проанализировала, какие пары донор–реципиент система предпочитала. По сравнению с простыми правилами на основе MELD, выученная стратегия выбирала пациентов, которые были несколько менее критично больны, и доноров, которые напоминали тех, что участвовали в исторически успешных трансплантациях — меньше маргинальных органов и меньше реципиентов, нуждавшихся в интенсивной поддержке жизненных функций. Поразительно, но система также «спасала» часть печеней, которые на практике были утилизированы, но выглядели относительно качественными. Выборы модели в группах, уже помеченных как «высокий риск» по стандартным оценкам, были связаны с лучшей фактической выживаемостью, хотя сами оценки отличий не показывали, что указывают на то, что алгоритм уловил сложные паттерны, которые пропускают существующие инструменты.
Что это может значить для пациентов и врачей
Эта работа пока не даёт готовой системы для применения у постели больного, но показывает, что метод ИИ, обученный исключительно на прошлых данных, может точнее отражать реальные компромиссы при трансплантации печени — баланс между опасностью слишком долгого ожидания и риском использования плохого совпадения. Научившись говорить «да», «нет» или «не сейчас» на каждое предложение органа, подход снизил количество смоделированных неудач трансплантатов при сохранении большинства успехов и предложил потенциальные спасительные варианты многим, кто иначе мог бы умереть в листе ожидания. При дальнейшем совершенствовании, улучшении данных и тщательной проверке подобные инструменты поддержки принятия решений могли бы помочь командам по трансплантации более разумно использовать каждую донорскую печень и дать большему числу пациентов долгосрочный второй шанс.
Цитирование: Melehy, A., Feng, J., Amara, D. et al. Liver transplant donor-recipient matching with offline reinforcement learning. npj Digit. Med. 9, 351 (2026). https://doi.org/10.1038/s41746-026-02529-1
Ключевые слова: трансплантация печени, распределение органов, обучение с подкреплением, медицинский ИИ, сопоставление донор–реципиент