Clear Sky Science · es
Emparejamiento donante-receptor en trasplantes de hígado con aprendizaje por refuerzo offline
Por qué importan estas decisiones en trasplantes de hígado
Para las personas con enfermedad hepática grave, recibir un trasplante puede marcar la diferencia entre la vida y la muerte, pero hay muchos menos hígados donados que pacientes que los necesitan. Los médicos deben decidir constantemente si aceptar un hígado concreto para un paciente específico, seguir esperando un mejor emparejamiento o retirar a alguien de la lista de espera si mejora o empeora demasiado. Este estudio explora si una forma de inteligencia artificial, conocida como aprendizaje por refuerzo offline, puede aprender de años de datos de trasplantes para sugerir decisiones de emparejamiento más seguras e inteligentes que salven más vidas y aprovechen mejor cada órgano donado.
De predicciones puntuales a decisiones continuas
La mayoría de las herramientas actuales en trasplante hepático analizan un único instante —por ejemplo, el día de la cirugía— y estiman la probabilidad de supervivencia de un paciente con un órgano donante concreto. Con frecuencia se apoyan en puntuaciones como el Model for End-Stage Liver Disease (MELD), que resume pruebas de laboratorio en un número que ayuda a priorizar a los pacientes más graves. Pero estas herramientas omiten una parte crucial de la realidad: la condición del paciente cambia durante semanas y meses, y cada decisión de aceptar o rechazar un órgano ofrecido influye en lo que ocurre después, incluido el riesgo de morir aún en la lista de espera. Los autores, en cambio, enmarcaron el trasplante como una secuencia de decisiones a lo largo del tiempo, donde cada elección de trasplantar, esperar o retirar a un paciente de la lista conduce a futuros posibles distintos.
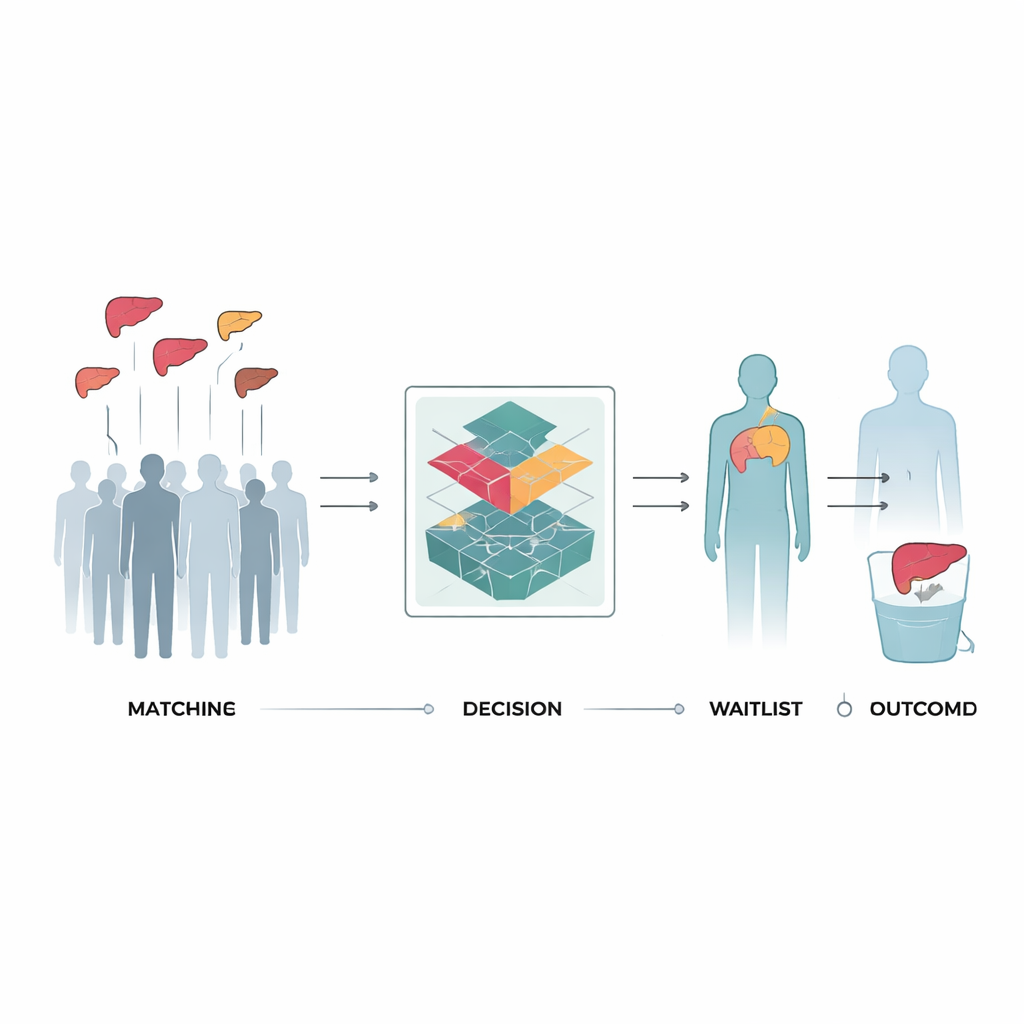
Enseñar a una máquina a aprender de elecciones pasadas en trasplantes
Los investigadores usaron registros del U.S. Scientific Registry of Transplant Recipients, centrados en más de 43.000 adultos inscritos para un primer trasplante de hígado entre 2017 y 2022. Para cada persona reconstruyeron una línea temporal de puntuaciones MELD y de posibles ofertas de donantes, incluidos órganos que finalmente fueron descartados. En cada paso, el equipo informático veía las características del paciente, las del donante potencial y tres acciones posibles: esperar, trasplantar o retirar de la lista. Después recibía una señal de recompensa basada en lo que realmente ocurrió más adelante —si la condición del paciente mejoró o empeoró, si un trasplante tuvo éxito, fracasó o nunca se realizó—. Usando una técnica llamada Conservative Q-learning, el sistema se entrenó para favorecer decisiones que, a lo largo de muchas de esas líneas temporales, condujeron a menos muertes y a menos trasplantes fallidos.
Qué habría cambiado la política aprendida
Cuando el sistema entrenado se probó en un grupo separado de pacientes, evitó el 73% de los emparejamientos donante–receptor que en la vida real condujeron a fallo del injerto o muerte dentro del año tras el trasplante, a la vez que preservó el 93% de los trasplantes exitosos. También identificó oportunidades de trasplante más tempranas para casi la mitad de los pacientes que murieron en lista de espera, lo que sugiere que un tiempo distinto o donantes distintos podrían haber mejorado sus probabilidades. Importante: a diferencia de estrategias muy agresivas que simplemente trasplantan a casi todos una vez que están lo bastante enfermos, este enfoque limitó el número total de trasplantes mientras mejoraba los resultados. En una simulación más realista, donde cada hígado donado solo puede usarse una vez y los pacientes salen del pool tras un trasplante o ser retirados, el modelo aún logró emparejar a la mayoría de los pacientes con donantes mientras reducía fracasos evitables.
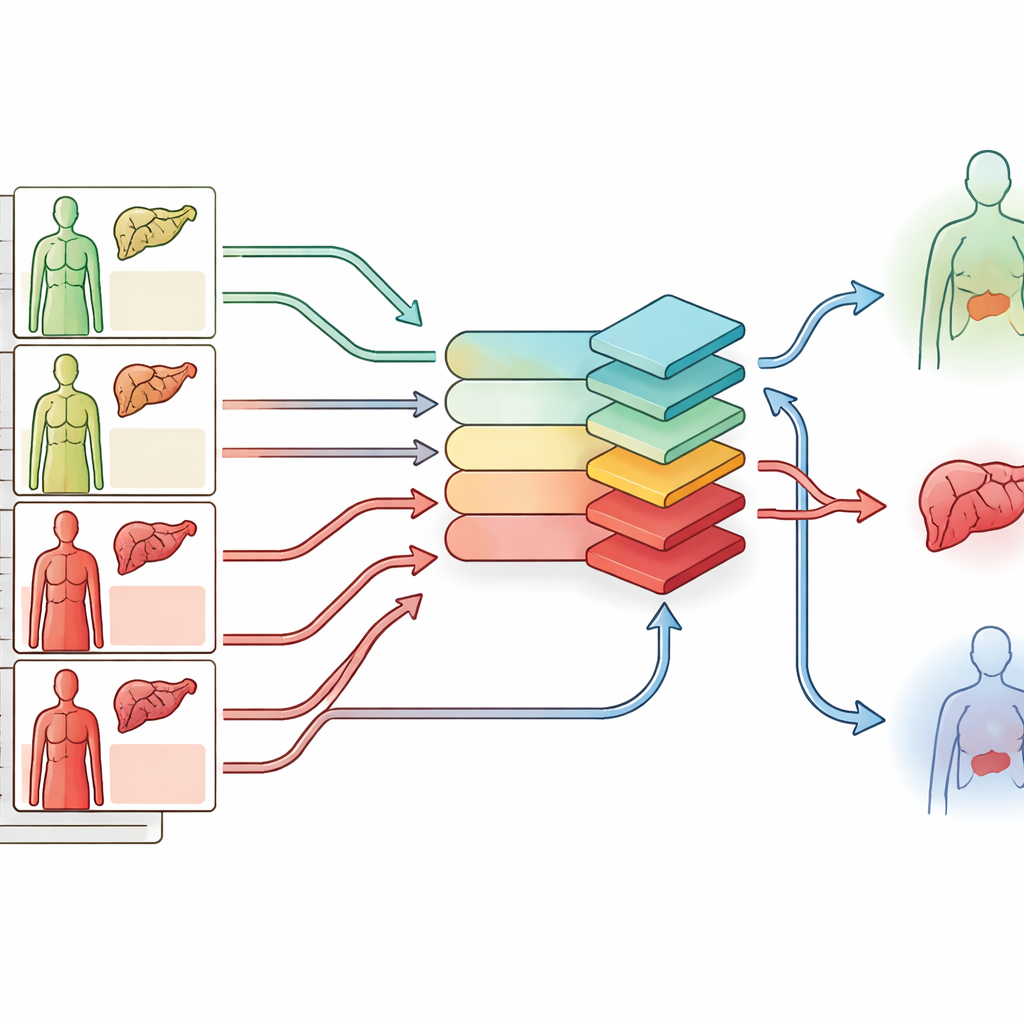
Pistas de mejores emparejamientos ocultas en los datos
Más allá de los números de rendimiento bruto, el equipo examinó qué tipos de parejas donante–receptor tendía a favorecer el sistema. En comparación con reglas simples basadas en MELD, la estrategia aprendida eligió pacientes algo menos críticamente enfermos y donantes que se parecían más a los de trasplantes históricamente exitosos: menos órganos marginales y menos receptores que necesitaban soporte vital intensivo. De forma llamativa, también recuperó un subconjunto de hígados que en la práctica habían sido descartados pero que parecían ser de calidad relativamente buena. Las decisiones de trasplante del modelo dentro de grupos ya etiquetados como «alto riesgo» por puntuaciones estándar se asociaron con mejor supervivencia real, aunque esas puntuaciones por sí solas no diferían, lo que sugiere que el algoritmo había captado patrones complejos que las herramientas existentes pasan por alto.
Qué podría significar esto para pacientes y médicos
Este trabajo aún no entrega un sistema listo para usar en la cabecera del paciente, pero demuestra que un método de IA entrenado exclusivamente con datos pasados puede reproducir con mayor fidelidad las compensaciones reales en el trasplante hepático —equilibrando el peligro de esperar demasiado frente al riesgo de usar una mala coincidencia. Al aprender cuándo decir sí, no o aún no a cada oferta de órgano, el enfoque redujo fallos del injerto en simulaciones mientras mantenía la mayoría de los éxitos y ofreció posibles salvavidas a muchos que de otro modo podrían haber fallecido en la lista de espera. Con refinamiento adicional, datos mejores y pruebas cuidadosas, herramientas de apoyo a la decisión similares podrían ayudar a los equipos de trasplante a usar cada hígado donado con más prudencia y dar a más pacientes una segunda oportunidad duradera.
Cita: Melehy, A., Feng, J., Amara, D. et al. Liver transplant donor-recipient matching with offline reinforcement learning. npj Digit. Med. 9, 351 (2026). https://doi.org/10.1038/s41746-026-02529-1
Palabras clave: trasplante de hígado, asignación de órganos, aprendizaje por refuerzo, IA médica, emparejamiento donante-receptor