Clear Sky Science · ru
Нисин и рутин как потенциальные покровные агенты для оксидных наночастиц железа с целью усиления терапевтическо-диагностических приложений против рака
Новые подходы к прицельной терапии рака
Многие современные методы лечения рака испытывают трудности с тем, чтобы поражать исключительно опухолевые клетки, не затронув здоровые ткани. В этом исследовании рассматривается хитрый прием: покрытие крошечных частиц железа природными соединениями, чтобы они могли одновременно обнаруживать и атаковать рак более точно. Объединяя безопасные молекулы, происходящие из пищи и растений, с медицинскими наночастицами, исследователи стремятся создать инструменты, которые находят раковые клетки, проникают в них и ослабляют одну из их ключевых защит против терапии.
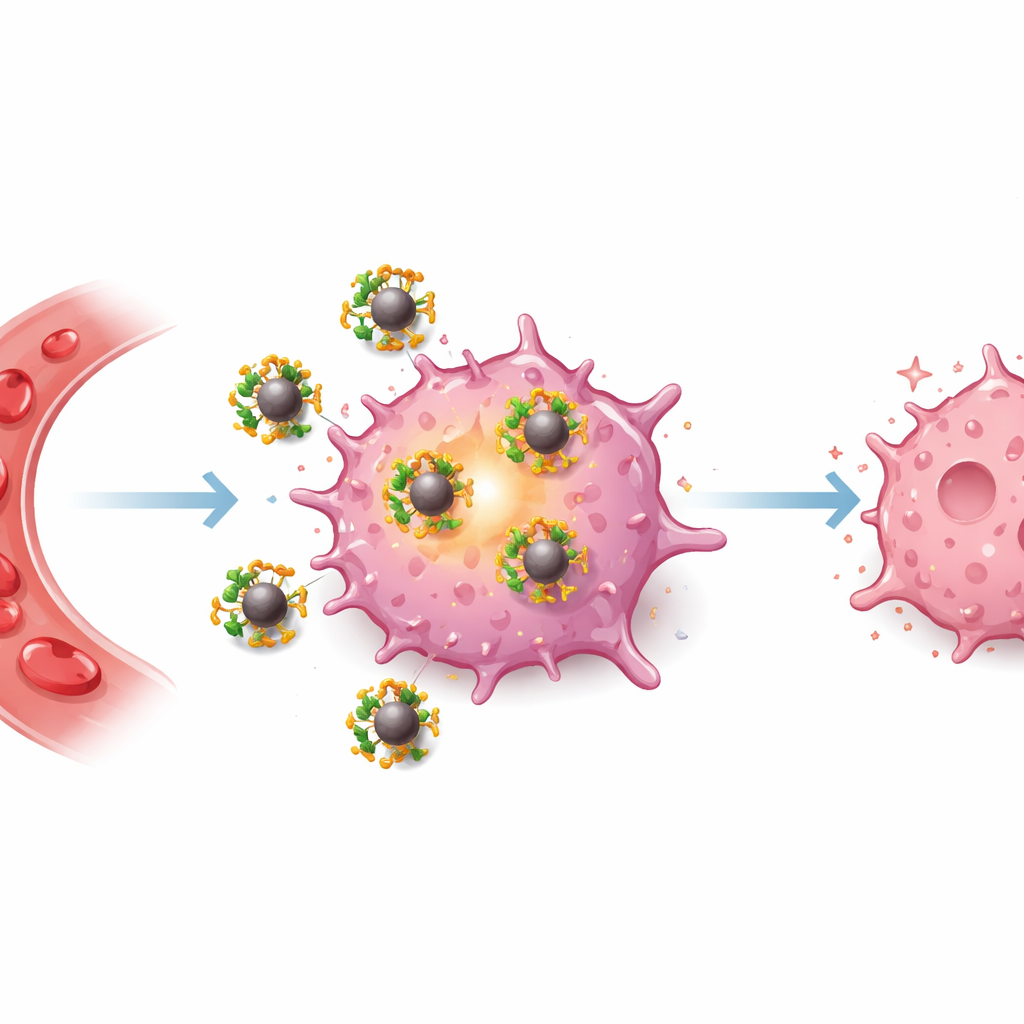
Маленькие магниты как медицинские помощники
Оксидные наночастицы железа — это микроскопические магнитные шарики, уже применяемые в медицине, например в качестве контрастных агентов для МРТ или при лечении железодефицитной анемии. Поскольку врачи могут направлять их или отслеживать с помощью магнитов и визуализации, эти частицы представляют интерес для «тераностики» — материалов, которые одновременно диагностируют и лечат заболевания. Однако поведение частиц в организме во многом определяется тем, как покрыта их поверхность. Хорошее покрытие может обеспечивать стабильность в крови, помогать избегать быстрого выведения и даже направлять частицы непосредственно к тканям опухоли.
Природные покрытия: от цитрусовых растений и дружественных бактерий
Команда сосредоточилась на двух природных веществах в качестве покрытий. Первое, рутин, — растительный пигмент, встречающийся в цитрусовых, долгое время изучавшийся за антиоксидантные и противораковые свойства. Второе, нисин, — небольшая белковая молекула, производимая безвредной молочной бактерией и безопасно используемая в пищевой промышленности как антимикробный агент. Исследователи прикрепили каждое из этих веществ к оксидным наночастицам железа, получив рутин‑покрытые (R‑IONP) и нисин‑покрытые (N‑IONP) частицы. Они тщательно измерили размер частиц, форму, поверхностный заряд и однородность по размерам, используя высокоразрешающую микроскопию и оптические методы. Оба покрытия эффективно покрывали железные ядра и давали стабильные частицы с отрицательным зарядом в нанометровом диапазоне, пригодные для перемещения по кровотоку и взаимодействия с клетками.
Испытание покрытых частиц на раковых клетках
Чтобы выяснить, могут ли новые частицы повреждать раковые клетки, ученые подвергли устойчивую к лечению линию человеческих клеток рака молочной железы (MDA‑MB‑231) воздействию возрастающих доз R‑IONP и N‑IONP. Через два дня они измерили количество выживших клеток. Оба типа покрытых наночастиц замедляли рост раковых клеток, но рутин‑покрытые частицы оказались явно более эффективными: при одинаковых концентрациях они убивали больше клеток, чем версия с нисином. Дозы, требующиеся для сокращения выживаемости клеток наполовину, были примерно вдвое ниже для R‑IONP по сравнению с N‑IONP, что указывает на то, что сочетание рутина с железными наночастицами усиливает его противораковое действие.
Прицеливание на белок стресса на поверхности опухолевых клеток
Многие раковые клетки зависят от вспомогательного белка GRP78, который обычно находится внутри клетки, но часто появляется на поверхности опухолевых клеток и помогает им переживать стресс и сопротивляться препаратам. Исследователи спросили, могут ли рутин или нисин прикрепляться к этому белку, потенциально блокируя его защитную роль. С помощью современных компьютерных моделирований молекулярной динамики и докинга они смоделировали, как каждое соединение встраивается в ключевую область GRP78. Оказалось, что и рутин, и нисин могут образовывать стабильные комплексы с этим белком, но более длинная и гибкая цепь нисина позволяет ему устанавливать больше точек контакта и связываться сильнее. Детальные расчеты энергии показали благоприятные энергии взаимодействия для обоих соединений, с преимуществом у нисина, и выявили конкретные участки белка, которые захватывают каждую из покрывающих молекул.
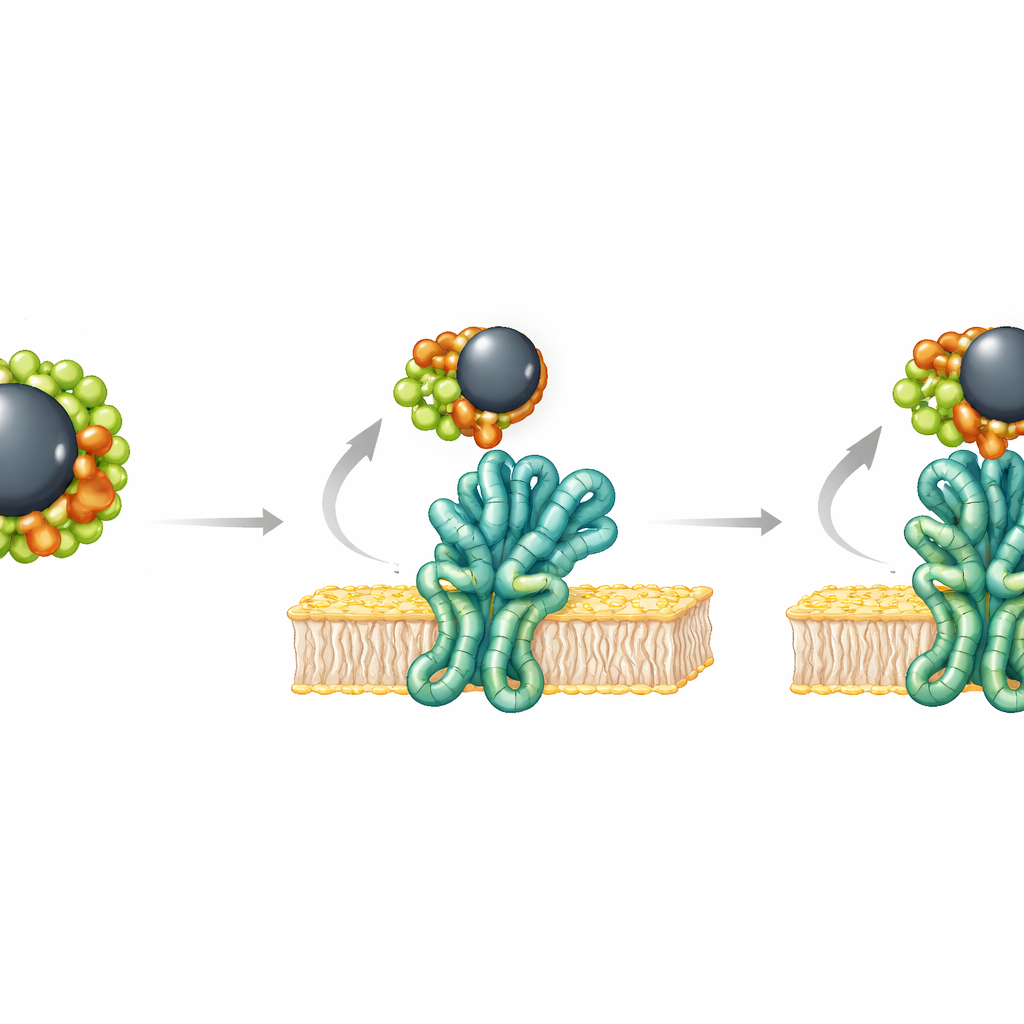
Что это может значить для будущей онкологической помощи
В совокупности эксперименты и моделирования указывают на двунаправленную возможность. Рутин‑покрытые оксидные наночастицы железа продемонстрировали более сильное прямое уничтожение клеток рака молочной железы, тогда как как рутин, так и нисин, по-видимому, способны нацеливаться на GRP78 — белок стресса, который помогает опухолям выдерживать лечение. Это открывает возможность разработки покрытых железных нанолекарств, которые одновременно доставляют терапию и выводят из строя ключевой механизм выживания раковых клеток, повышая эффективность существующих препаратов. Хотя потребуются дальнейшие исследования на животных и клинические испытания, работа подчеркивает, как перепрофилирование привычных природных молекул на хорошо известных магнитных частицах может приблизить более умные и селективные тераностические решения для лечения рака.
Цитирование: Saad, O.A., Elfiky, A.A., Fathy, M.M. et al. Nisin and rutin as potential coating agents for iron oxide nanoparticles for enhanced theranostic applications against cancer. Sci Rep 16, 14036 (2026). https://doi.org/10.1038/s41598-026-49686-7
Ключевые слова: оксидные наночастицы железа, тераностическая онкология, рутнин, ниcин, GRP78