Clear Sky Science · ar
النيزين والروتين كعوامل تغليف محتملة لجسيمات أكسيد الحديد النانوية لتحسين التطبيقات العلاجية‑التشخيصية ضد السرطان
طرق جديدة لاستهداف علاجات السرطان
تواجه العديد من علاجات السرطان الحديثة صعوبة في استهداف الخلايا الورمية فقط مع الحفاظ على الأنسجة السليمة. تستكشف هذه الدراسة تعديلًا ذكيًا: تغليف جسيمات حديدية صغيرة بمركبات طبيعية بحيث تستطيع كلٌّ من الكشف عن السرطان ومهاجمته بدقة أكبر. من خلال الجمع بين جزيئات مأمونة مشتقة من الغذاء والنباتات وجسيمات نانوية طبية، يأمل الباحثون في ابتكار أدوات يمكنها العثور على خلايا السرطان، والدخول إليها، وإضعاف أحد دفاعاتها الرئيسية ضد العلاج.
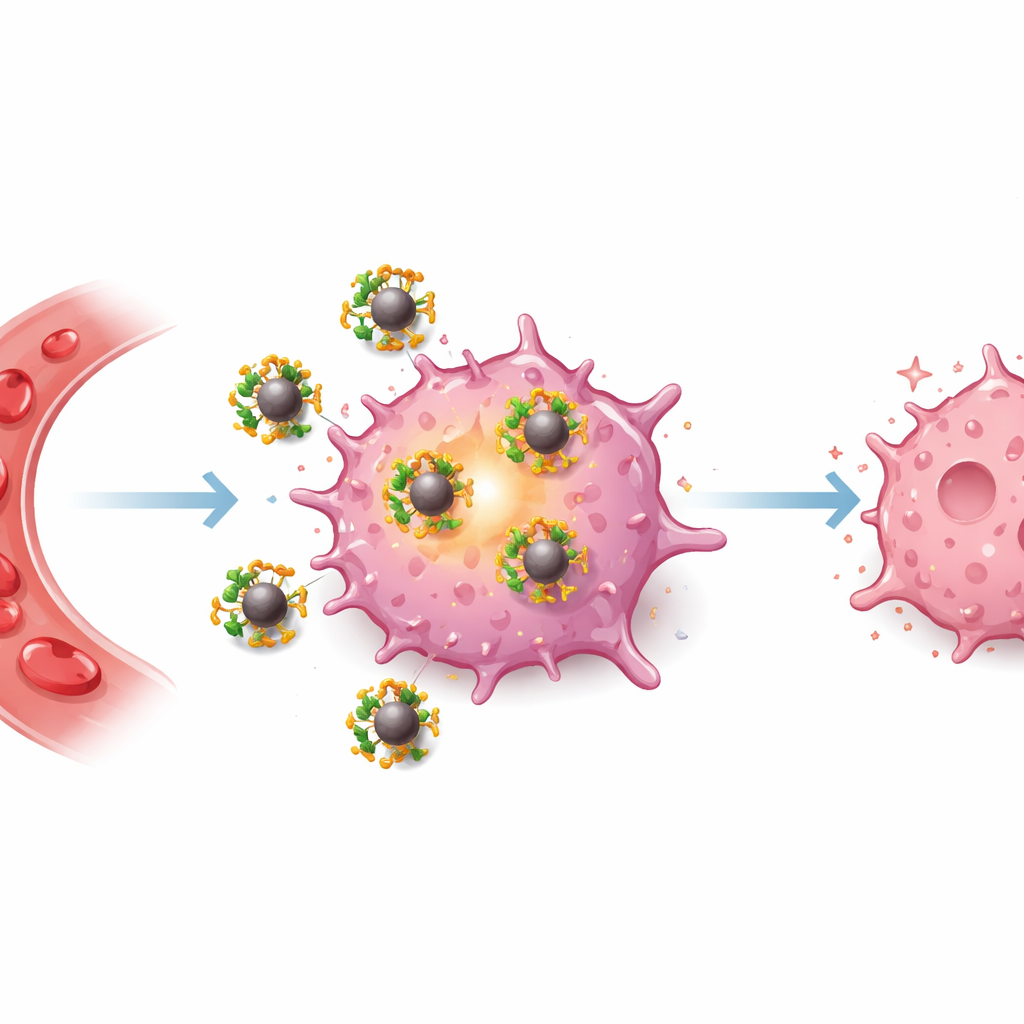
مغانط صغيرة كمساعدين طبيين
جسيمات أكسيد الحديد النانوية هي حبيبات مغناطيسية مجهرية تُستخدم بالفعل في الطب، على سبيل المثال كعوامل تباين في فحوصات التصوير بالرنين المغناطيسي أو لعلاج فقر الدم الناجم عن نقص الحديد. وبما أن الأطباء يستطيعون توجيهها أو تتبعها بالمغانط والتصوير، فإن هذه الجسيمات تمثل مرشحين جذابين لـ«العلاج‑التشخيصي» — وهي مواد يمكنها تشخيص المرض وعلاجه في آن واحد. ومع ذلك، يتوقف سلوكها داخل الجسم بشكل كبير على طريقة تغليف سطحها. يمكن لتغليف جيد أن يحافظ على استقرارها في الدم، ويساعدها على تجنب الإزالة السريعة، وحتى يوجهها بشكل محدد إلى النسيج الورمي.
أغطية طبيعية: من نباتات الحمضيات والبكتيريا النافعة
ركز الفريق على مادتين طبيعيتين كأغطية. الأولى، الروتين، صباغ نباتي يوجد في ثمار الحمضيات ودُرِس طويلاً لتأثيراته المضادة للأكسدة والمضادة للسرطان. الثانية، النيزين، هي بروتين صغير تصنعه بكتيريا ألبان حميدة وتُستخدم بأمان في الغذاء كعامل مضاد للميكروبات. ربط الباحثون كلًا من هاتين المادتين بجسيمات أكسيد الحديد، مكونين جسيمات مغطاة بالروتين (R‑IONP) وجسيمات مغطاة بالنيزين (N‑IONP). ثم قاسوا بدقة حجم الجسيمات وشكلها وشحنة سطحها ومدى تجانس أحجامها، باستخدام مجاهر عالية الدقة وتقنيات ضوئية. غطت الطبقتان نوى الحديد بكفاءة وأنتجتا جسيمات مستقرة ذات شحنة سالبة ضمن مقياس النانومتر، مناسبة للسير عبر مجرى الدم والتفاعل مع الخلايا.
اختبار الجسيمات المغلفة ضد السرطان
لمعرفة ما إذا كانت الجسيمات الجديدة تستطيع إتلاف خلايا السرطان، عرّض العلماء سلالة بشرية صعبة العلاج من سرطان الثدي (MDA‑MB‑231) لجرعات متزايدة من R‑IONP وN‑IONP. بعد يومين، قاسوا عدد الخلايا الحية المتبقية. أبطأت كلا نوعي الجسيمات المغلفة نمو الخلايا السرطانية، لكن الجسيمات المغلفة بالروتين كانت أقوى بوضوح: عند نفس التركيزات، قتلت عددًا أكبر من الخلايا مقارنةً بنسخة النيزين. كانت الجرعات المطلوبة لخفض بقاء الخلايا إلى النصف أقل بنحو الضعف بالنسبة لـR‑IONP مقارنةً بـN‑IONP، ما يشير إلى أن الجمع بين الروتين وجسيمات الحديد يعزز تأثيره المضاد للسرطان.
استهداف بروتين الإجهاد على خلايا الأورام
تعتمد العديد من خلايا السرطان على بروتين مساعد يُدعى GRP78، والذي يعيش عادةً داخل الخلايا لكنه يظهر كثيرًا على سطح خلايا الورم ويساعدها على تحمل الإجهاد ومقاومة الأدوية. تساءل الباحثون عما إذا كان الروتين أو النيزين يمكن أن يرتبط بهذا البروتين، مما قد يعيق دوره الوقائي. باستخدام محاكاة حاسوبية متقدمة لحركة الجزيئات والربط، نمذجوا كيف يتناسب كل مركب مع منطقة رئيسية في GRP78. وجدوا أن كلاً من الروتين والنيزين يمكن أن يشكل مركبات مستقرة مع البروتين، لكن سلسلة النيزين الأطول والمرنة تسمح لها بإجراء نقاط اتصال أكثر والارتباط بقوة أكبر. أظهرت حسابات طاقية مفصلة أن طاقات التفاعل كانت ملائمة لكليهما، مع تفوق طفيف للنيزين، وحددت أجزاء محددة من البروتين التي تمسك بكل جزيء تغليف.
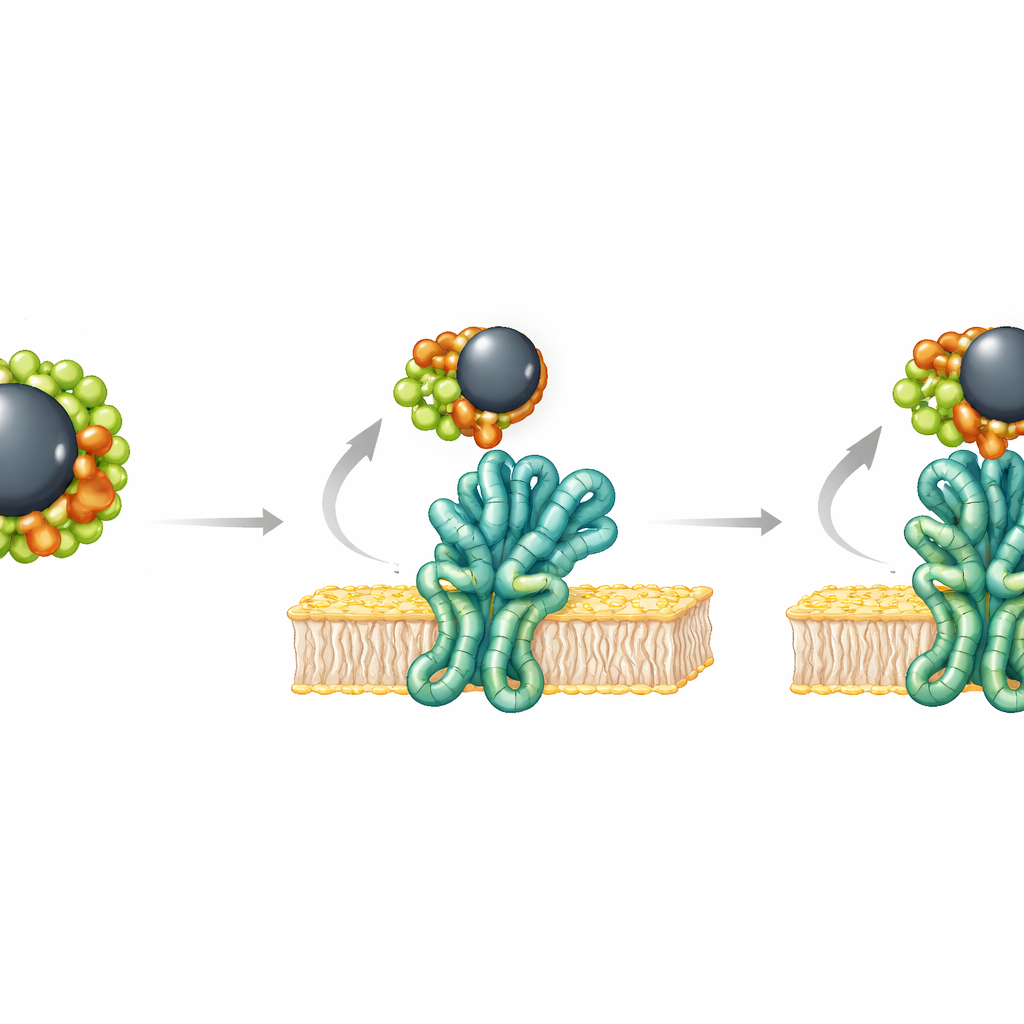
ماذا قد يعني هذا لرعاية السرطان المستقبلية
تشير النتائج المجمعة من التجارب والمحاكاة إلى فرصة مزدوجة. أظهرت جسيمات أكسيد الحديد المغطاة بالروتين قدرة أقوى على قتل خلايا سرطان الثدي مباشرة، بينما يبدو أن كلًا من الروتين والنيزين قادران على استهداف GRP78، وهو بروتين إجهاد يساعد الأورام على الصمود أمام العلاج. يفتح هذا الباب أمام تصميم أدوية نانوية حديدية مغلفة تتيح توصيل العلاج وتعطيل آلية بقاء رئيسية في خلايا السرطان، ما قد يحسن أثر الأدوية الحالية. وعلى الرغم من الحاجة لمزيد من الدراسات على الحيوان والسريرية، تبرز هذه الدراسة كيف أن إعادة توظيف جزيئات طبيعية مألوفة على جسيمات مغناطيسية معروفة قد يقرب من واقع العلاج‑التشخيصي الذكي والأكثر انتقائية للسرطان.
الاستشهاد: Saad, O.A., Elfiky, A.A., Fathy, M.M. et al. Nisin and rutin as potential coating agents for iron oxide nanoparticles for enhanced theranostic applications against cancer. Sci Rep 16, 14036 (2026). https://doi.org/10.1038/s41598-026-49686-7
الكلمات المفتاحية: جسيمات أكسيد الحديد النانوية, العلاج‑التشخيصي للسرطان, روتين, نيزين, GRP78