Clear Sky Science · ru
Гомолог ланмодулина из Mesorhizobium qingshengii J19, участвующий в иммобилизации иттрия
Почему это важно для повседневных технологий
Редкоземельные элементы скрываются внутри многих устройств и зелёных технологий, на которых мы полагаемся — от телефонов и ветряных турбин до электромобилей и медицинских томографов. Добыча и переработка этих металлов дорогостоящи и загрязняют окружающую среду, поэтому учёные ищут более мягкие способы извлечения их из потоков отходов и загрязнённых вод. В этом исследовании изучается, как белок из почвенной бактерии может захватывать один из таких металлов, иттрий, и помогать фиксировать и возвращать его более чистым способом.
Металлы, питающие современную жизнь
Редкоземельные элементы составляют семейство металлов, которые ведут себя похоже в водной среде, что затрудняет их разделение друг от друга и от других ионов. Иттрий и его «родственники» необходимы для сильных магнитов, батарей, экранов и лазеров. В последние годы исследователи обнаружили, что некоторые бактерии действительно нуждаются в редкоземельных элементах для работы ключевых ферментов, помогающих им использовать простые углеродные соединения в качестве пищи. Это означает, что в природе уже существуют молекулы, которые с удивительной точностью отбирают эти металлы, что даёт подсказки для новых инструментов переработки.
Бактериальный белок с особым «захватом»
Команда сосредоточилась на бактерии Mesorhizobium qingshengii J19, ранее показанной как способной переносить и иммобилизовать высокие уровни иттрия. Сканируя её геном, учёные нашли ген, кодирующий небольшой белок, связывающий металлы, родственный ланмодулину — хорошо известному захватчику редкоземельных элементов из другой бактерии. Новый белок, сформированный из так называемых мотивов EF-hand, которые обычно связывают кальций, отличается в ключевых позициях своей последовательности: вместо часто встречающегося пролина там стоит треонин. Исследователи предположили, что это изменение может повлиять на предпочтения по металлам и на силу связывания. 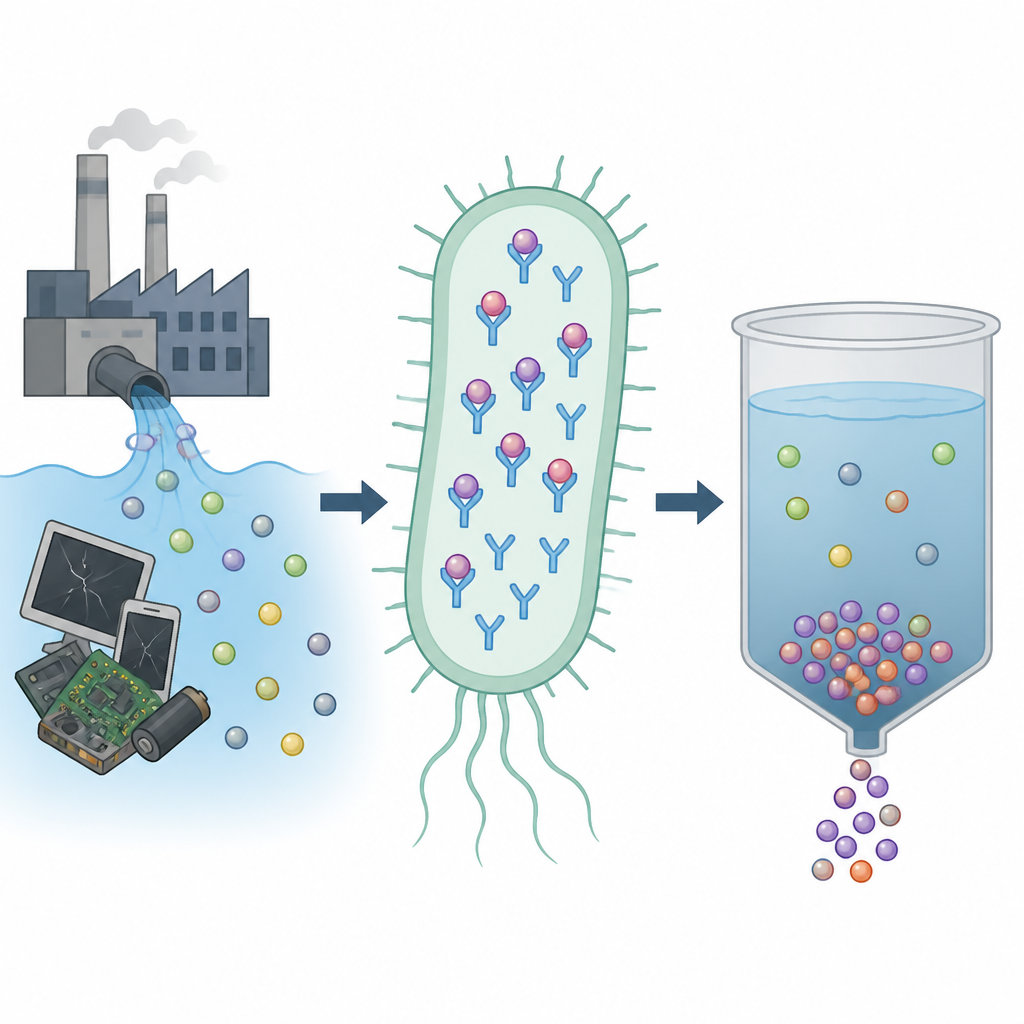
Превращение обычных лабораторных бактерий в «губки» для металлов
Чтобы проверить белок, учёные вставили его ген в Escherichia coli, стандартную лабораторную бактерию, и побудили клетки синтезировать большие количества белка в пространстве между внутренней и внешней мембранами. По сравнению с обычными E. coli модифицированные клетки накапливали значительно больше иттрия и также больше неодима, когда оба металла присутствовали одновременно; при этом они не показали повышенной способности аккумулировать скандий. Такая картина указывает на то, что белок предпочитает ионы металлов определённого размера, отдавая преимущество иттрію и неодиму по сравнению с более мелкими или немного более крупными родственниками.
Измерение «вкуса» белка к металлам
После очистки белка команда провела серию тестов связывания, в которых смешивала его с известными количествами иттрия и затем отделяла связанный с белком металл от свободного металла. Они обнаружили, что при умеренных концентрациях белок связывал большие количества иттрия, особенно при слабощелочном pH и комнатной температуре. При наилучших условиях его кажущаяся ёмкость по удержанию иттрия была значительно выше, чем ранее сообщавшиеся значения для ланмодулина, связывающего другой редкоземельный элемент — лантан, хотя авторы подчёркивают, что методы и металлы различаются. Дополнительные тесты показали, что белок также может связывать неодим, но когда иттрий и неодим предлагались вместе, преимущество оставалось за иттрием, что указывает на умеренную селективность в его пользу. 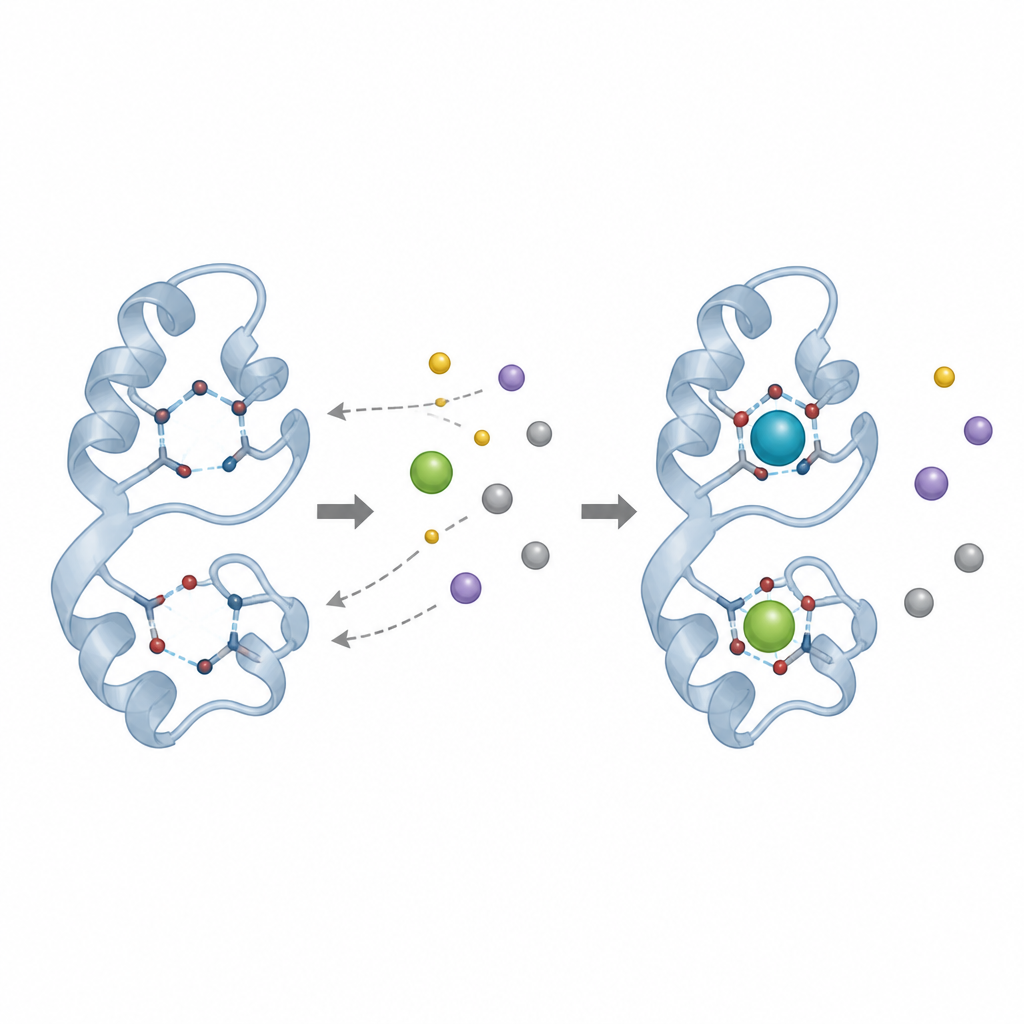
От лабораторных испытаний к более чистым методам извлечения
Поскольку клетки M. qingshengii J19 могут фиксировать иттрий на своих поверхностях и даже образовывать богатые иттриями минеральные частицы, а её EF-hand белок так хорошо связывает иттрий в растворе, авторы видят несколько возможных применений. Инженерные клетки E. coli, несущие этот белок, могли бы размещаться за селективными мембранами и действовать как живые фильтры, захватывающие редкоземельные элементы из разбавленных, смешанных потоков, таких как сточные воды шахт или выщелоченные растворы электронных отходов. Альтернативно очищенный белок можно было бы закрепить на твёрдых носителях или мембранах и повторно использовать в контролируемых циклах захвата и высвобождения металлов, применяя мягкие изменения кислотности или солёности для снятия металлов и их последующей переработки.
Что это значит простыми словами
По сути, исследование показывает, что белок, заимствованный у почвенного микроорганизма, может действовать как крошечный «клешня», предпочитающая удерживать иттрий и, в меньшей степени, неодим. Понимая, при каких условиях эта «клешня» работает лучше всего и насколько она селективна, учёные приближаются к созданию биооснованных фильтров, которые смогут очищать и возвращать ценные редкоземельные металлы из водных отходов. Такие подходы в будущем могут дополнять или частично заменять агрессивные химические процессы, помогая обеспечить доступ к критически важным материалам для современной техники при снижении экологических издержек их добычи.
Цитирование: Coimbra, C., Morais, P.V. & Branco, R. A lanmodulin homologous protein, from Mesorhizobium qingshengii J19, involved in yttrium immobilization. Sci Rep 16, 15015 (2026). https://doi.org/10.1038/s41598-026-45294-7
Ключевые слова: редкоземельные элементы, иттрий, гомолог ланмодулина, биотехникa очистки, белок, связывающий металлы