Clear Sky Science · fr
Une protéine homologue de la lanmoduline, issue de Mesorhizobium qingshengii J19, impliquée dans l’immobilisation du yttrium
Pourquoi cela compte pour la technologie de tous les jours
Les éléments de terres rares se trouvent dans de nombreux appareils et technologies vertes que nous utilisons, des téléphones et des éoliennes aux voitures électriques et aux appareils d’imagerie médicale. Leur extraction et leur raffinage sont coûteux et polluants, si bien que les scientifiques cherchent des méthodes plus douces pour les extraire des flux de déchets et des eaux contaminées. Cette étude examine comment une protéine issue d’une bactérie du sol peut se lier à l’un de ces métaux, le yttrium, et aider à le piéger et à le récupérer de manière plus propre.
Les métaux qui alimentent la vie moderne
Les éléments de terres rares forment une famille de métaux qui se comportent de façon similaire en solution, ce qui complique leur séparation les uns des autres et vis-à-vis d’autres ions. Le yttrium et ses pairs sont essentiels pour les aimants puissants, les batteries, les écrans et les lasers. Ces dernières années, des chercheurs ont découvert que certaines bactéries ont réellement besoin de terres rares pour activer des enzymes clés leur permettant d’utiliser des composés carbonés simples comme source d’énergie. Cela signifie que la nature contient déjà des molécules capables de sélectionner ces métaux avec une précision surprenante, ce qui offre des pistes pour de nouveaux outils de recyclage.
Une protéine bactérienne qui a une prise spéciale
L’équipe s’est concentrée sur une bactérie appelée Mesorhizobium qingshengii J19, montrée auparavant comme tolérante et capable d’immobiliser de fortes quantités de yttrium. En explorant son génome, ils ont identifié un gène codant une petite protéine de liaison aux métaux apparentée à la lanmoduline, un capteur de terres rares bien connu provenant d’une autre bactérie. Cette nouvelle protéine, formée de motifs dits « EF-hand » qui se lient habituellement au calcium, diffère à des positions clés de sa séquence en remplaçant un résidu couramment observé (proline) par un autre (thréonine). Les chercheurs ont supposé que ce changement pouvait modifier les préférences métalliques de la protéine et la force avec laquelle elle les retient. 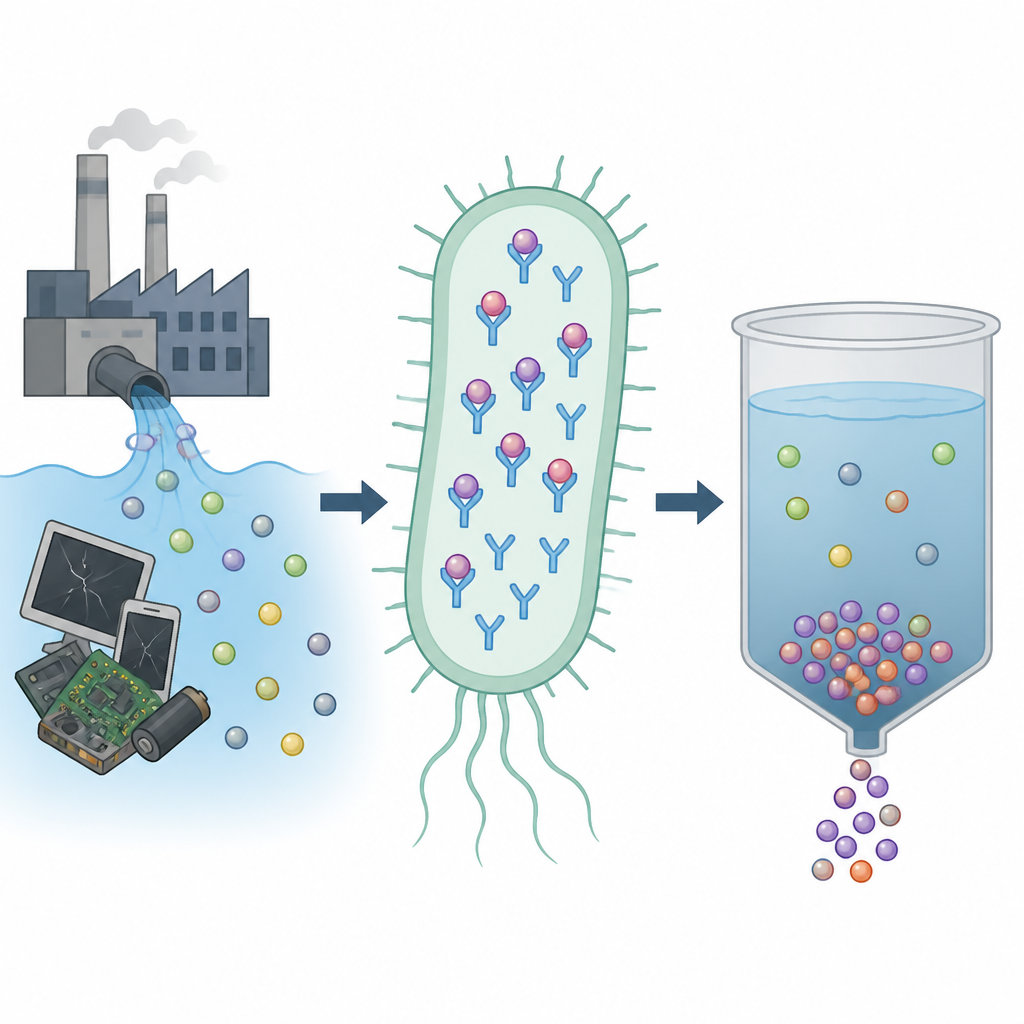
Transformer des bactéries de laboratoire en éponges à métaux
Pour tester la protéine, les scientifiques ont inséré son gène dans Escherichia coli, une bactérie standard utilisée en laboratoire, et ont poussé les cellules à produire de grandes quantités de la protéine dans l’espace périplasmique (entre membrane interne et externe). Par rapport à E. coli normales, les cellules modifiées ont accumulé beaucoup plus de yttrium et aussi davantage de néodyme lorsque les deux métaux étaient présents simultanément, alors qu’elles n’ont pas montré d’augmentation pour le scandium. Ce profil suggère que la protéine a une préférence pour des ions métalliques d’une certaine taille, favorisant le yttrium et le néodyme par rapport à des apparentés plus petits ou légèrement plus gros.
Mesurer l’appétence de la protéine pour les métaux
Après avoir purifié la protéine, l’équipe a réalisé une série d’essais de liaison où ils l’ont mélangée à des quantités connues de yttrium puis séparé le métal lié à la protéine du métal libre. Ils ont constaté qu’à des concentrations modérées, la protéine liait de grandes quantités de yttrium, notamment à pH légèrement alcalin et à température ambiante. Dans les meilleures conditions, sa capacité apparente à retenir le yttrium était bien supérieure aux valeurs rapportées précédemment pour la lanmoduline liée à un autre élément rare, le lanthane, bien que les auteurs soulignent que les méthodes et les métaux diffèrent. Des tests supplémentaires ont montré que la protéine peut aussi lier le néodyme, mais quand yttrium et néodyme étaient proposés ensemble, le yttrium l’emportait, suggérant une préférence modeste pour ce métal. 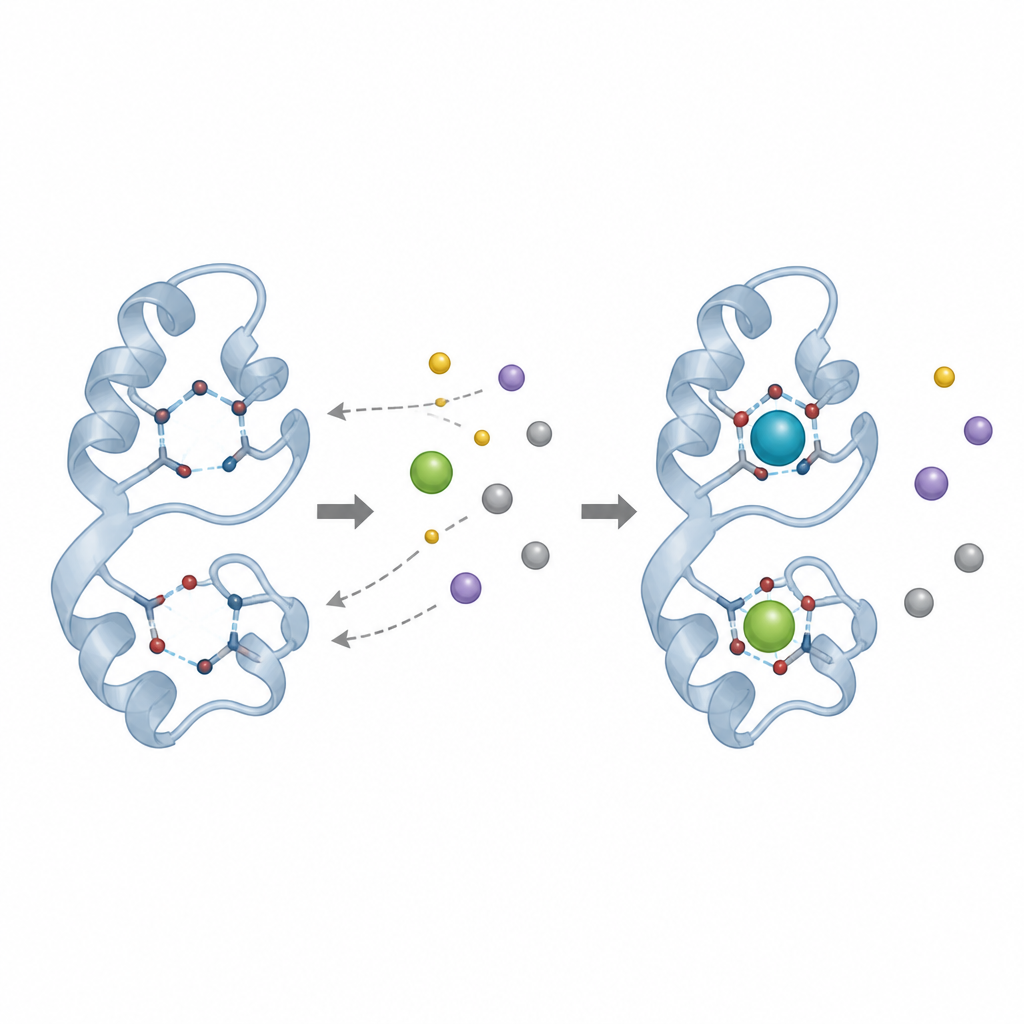
Des essais en laboratoire à des méthodes de récupération plus propres
Parce que les cellules de M. qingshengii J19 peuvent piéger le yttrium à leur surface et même former des particules minérales riches en yttrium, et parce que sa protéine EF-hand lie si bien le yttrium en solution, les auteurs envisagent plusieurs applications. Des cellules d’E. coli génétiquement modifiées portant la protéine pourraient être placées derrière des membranes sélectives et agir comme des filtres vivants capturant les terres rares dans des flux métalliques dilués et mixtes, tels que les effluents miniers ou les lixiviats de déchets électroniques. Alternativement, la protéine purifiée pourrait être fixée sur des supports solides ou des membranes et réutilisée dans des cycles contrôlés de capture et de libération des métaux, en jouant sur de légers changements d’acidité ou de salinité pour détacher les métaux en vue de leur recyclage.
Ce que cela signifie en termes simples
Essentiellement, l’étude montre qu’une protéine empruntée à un microbe du sol peut agir comme une petite pince qui préfère retenir le yttrium et, dans une moindre mesure, le néodyme. En comprenant quand cette pince fonctionne le mieux et quelle est sa sélectivité, les chercheurs se rapprochent de la conception de filtres bio‑inspirés capables de nettoyer et de récupérer des métaux de terres rares précieux à partir de déchets aqueux. De telles approches pourraient un jour compléter ou remplacer partiellement des procédés chimiques agressifs, contribuant à sécuriser des matériaux critiques pour la technologie moderne tout en réduisant leur coût environnemental d’extraction.
Citation: Coimbra, C., Morais, P.V. & Branco, R. A lanmodulin homologous protein, from Mesorhizobium qingshengii J19, involved in yttrium immobilization. Sci Rep 16, 15015 (2026). https://doi.org/10.1038/s41598-026-45294-7
Mots-clés: éléments de terres rares, yttrium, homologue de la lanmoduline, bioremédiation, protéine de liaison aux métaux