Clear Sky Science · ru
Разработка металлическо‑органических каркасов на основе β‑ЦД, загруженных олапарибом: новый подход к лечению рака шейки матки
Почему важна более продуманная доставка противораковых препаратов
Рак шейки матки по‑прежнему представляет серьёзную угрозу женскому здоровью во всём мире, и многие пациентки всё ещё получают лечение, которое повреждает не только опухоль, но и здоровые ткани. Исследователи ищут способы более эффективно доставлять современные таргетные препараты, чтобы большая часть лекарства попадала в раковые клетки, а не терялась или вызывала побочные эффекты в других частях тела. В этом исследовании рассматривается новый способ «упаковать» противораковый препарат олапариб внутрь крошечного губкообразного носителя, созданного из сахароподобного каркаса, с целью повысить стабильность препарата, его всасывание и цитотоксичность для клеток рака шейки матки в лабораторных условиях.
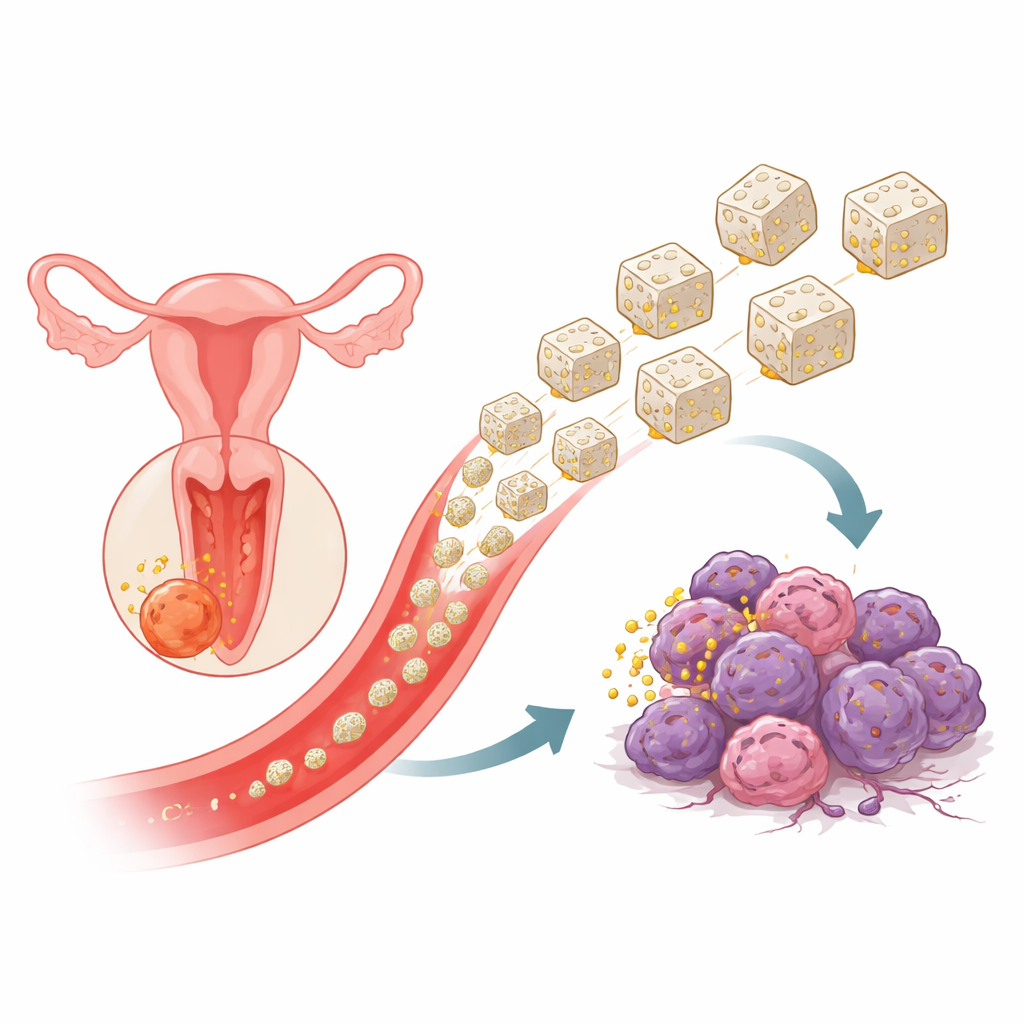
Новый дом для современного противоракового препарата
Олапариб — таблетка, применяемая при опухолях с нарушениями репарации ДНК, таких как некоторые формы рака яичников и молочной железы, и он может быть полезен при раке шейки матки. Однако у олапариба есть недостатки: он плохо растворяется, быстро выводится из организма и может воздействовать на здоровые ткани. Чтобы справиться с этими ограничениями, авторы создали высокопористый «металло‑органический каркас» (MOF) на основе бета‑циклодекстрина — кольцеобразной сахарной молекулы, уже используемой во многих лекарствах — в сочетании с ионами калия. Эта структура ведёт себя как микроскопическая губка, полная крошечных полостей и каналов, способных улавливать молекулы препарата. Команда затем загрузила олапариб в частицы β‑CD MOF, получив твёрдый порошок, состоящий из микро‑губок, заполненных лекарством.
Изучение крошечных губок
Исследователям сначала нужно было подтвердить, что носитель действительно удерживает препарат и меняет его поведение. Они определили, сколько олапариба способен вместить каркас, и обнаружили высокую эффективность инкапсуляции — около 76%, что означает, что большая часть препарата оказалась внутри пор, а не в свободном виде. С помощью комплекса физических методов — включая измерения тепловых потоков, анализ потери массы при нагревании, инфракрасную спектроскопию и рентгеновскую дифракцию — они заметили, что острый кристаллический сигнал чистого олапариба приглушился или исчез после помещения в каркас. Это изменение свидетельствовало о том, что препарат перестал существовать в виде крупных кристаллов и вместо этого распределился внутри пористой структуры MOF, что может улучшить его стабильность и растворимость.
Как носитель высвобождает и защищает препарат
Далее команда изучила, как олапариб выходит из каркаса в средах, имитирующих условия в организме. По сравнению со свободным препаратом, олапариб внутри β‑CD MOF растворялся более полно и продолжал высвобождаться равномерно в течение 24 часов, особенно при слегка кислых условиях, подобным тем, что характерны для многих опухолей. Эти результаты позволяют предположить, что пористый сахароподобный каркас может регулировать скорость выхода препарата, предотвращая начальный «всплеск» и обеспечивая более равномерное и продолжительное воздействие. Термальные испытания также показали, что загрузанные препаратом каркасы были более устойчивы к термическому разложению, чем свободный препарат или пустой носитель, что указывает на дополнительную защиту молекул олапариба при инкапсуляции.
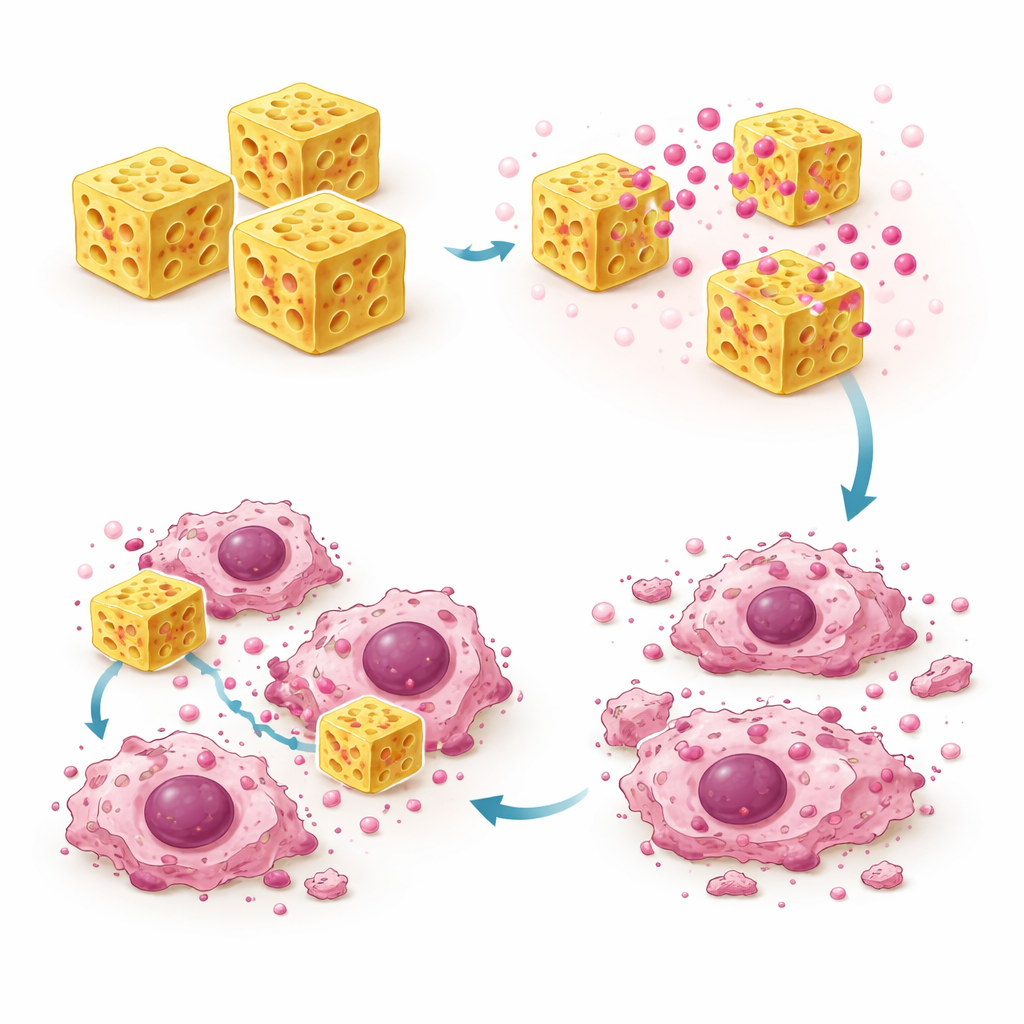
Более эффективная атака на клетки рака шейки матки
Чтобы проверить, привела ли эта «умная» доставка к лучшему уничтожению раковых клеток, авторы подвергли клетки TC‑1 рака шейки матки, выращенные в чашках, воздействию либо свободного олапариба, либо препарата, загруженного в β‑CD MOF. По стандартному тесту жизнеспособности клеток они обнаружили, что MOF‑формула сильнее снижала выживаемость раковых клеток при тех же дозах. Концентрация, необходимая для уничтожения половины клеток (IC50), примерно сократилась вдвое — с примерно 28 наномоляр для свободного олапариба до примерно 14 наномоляр для версии, загруженной в MOF. Микроскопия подтвердила, что обработанные клетки уменьшались в размерах, округлялись и отставали от поверхности — классические признаки стресса и программируемой клеточной гибели. Измерения двух ключевых белков, связанных с гибелью клеток — p53 и каспазы‑9 — показали более высокую активность у клеток, подвергшихся воздействию препарата в MOF, чем у клеток, обработанных только олапарибом, что поддерживает идею о более выраженной апоптозе, т.е. контролируемом клеточном самоубийстве.
Что это может значить для будущих методов лечения
Проще говоря, работа показывает, что упаковка олапариба в крошечные сахароподобные «губки» может сделать его более эффективным против клеток рака шейки матки в лабораторных условиях, обеспечивая при этом более равномерное высвобождение и повышенную стабильность. Хотя эти результаты ограничиваются испытаниями в пробирке и на клеточных культурах и ещё не доказывают преимущества у пациентов, они указывают на перспективную стратегию: использование биосовместимых пористых каркасов для доставки современных таргетных препаратов прямо в опухоль и их постепенного высвобождения. Если дальнейшие исследования на животных и клинические испытания подтвердят эти преимущества, такие формы могут позволить снизить дозы, уменьшить побочные эффекты и расширить применение олапариба и похожих препаратов в борьбе с раком шейки матки.
Цитирование: Alsulays, B.B., Anwer, M.K., Hatata, M.N. et al. Development of β-CD metal organic frameworks loaded with olaparib: a novel approach for the treatment of cervical cancer. Sci Rep 16, 12911 (2026). https://doi.org/10.1038/s41598-026-43779-z
Ключевые слова: рак шейки матки, олапариб, доставка препаратов, металло‑органические каркасы, циклодекстрин