Clear Sky Science · de
Entwicklung von β-CD-Metall‑organischen Gerüsten beladen mit Olaparib: ein neuartiger Ansatz zur Behandlung von Gebärmutterhalskrebs
Warum eine intelligentere Wirkstoffabgabe bei Krebs wichtig ist
Gebärmutterhalskrebs bleibt weltweit eine bedeutende Bedrohung für die Gesundheit von Frauen, und viele Patientinnen sind weiterhin auf Behandlungen angewiesen, die neben den Tumoren auch gesundes Gewebe schädigen können. Forschende suchen nach Wegen, moderne zielgerichtete Wirkstoffe effizienter zu verabreichen, damit mehr des Medikaments die Krebszellen erreicht und weniger verschwendet wird oder anderswo Nebenwirkungen verursacht. Diese Studie untersucht eine neue Methode, das Krebsmedikament Olaparib in einem winzigen, schwammartigen Träger aus einem zuckerbasierten Gerüst zu verpacken, mit dem Ziel, das Medikament stabiler, besser aufnehmbar und im Labor wirksamer gegen Gebärmutterhalskrebszellen zu machen.
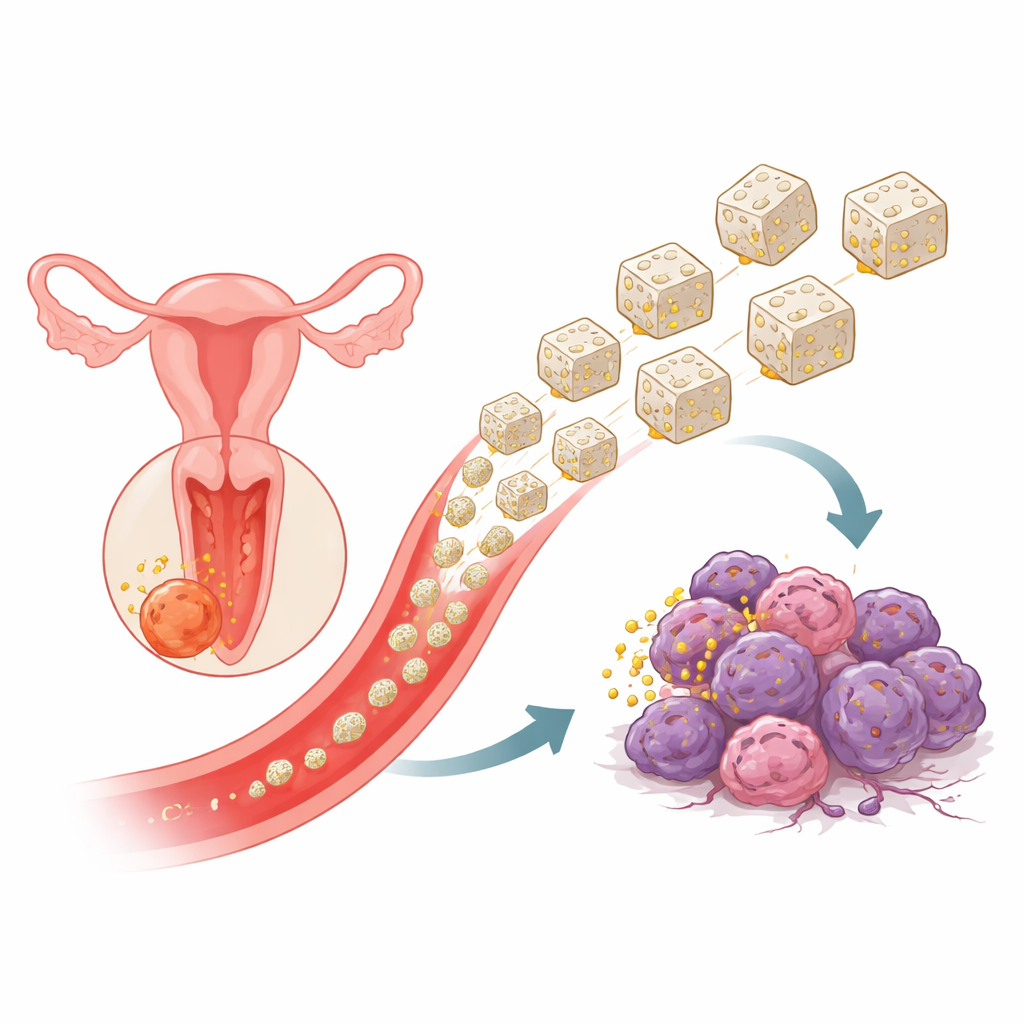
Ein neues Zuhause für ein modernes Krebsmedikament
Olaparib ist eine Tablette zur Behandlung von Tumoren mit eingeschränkter Fähigkeit zur Reparatur beschädigter DNA, etwa bei bestimmten Eierstock‑ und Brustkrebserkrankungen, und könnte auch bei Gebärmutterhalskrebs hilfreich sein. Allein hat Olaparib jedoch Nachteile: es löst sich schlecht, wird rasch aus dem Körper entfernt und kann gesundes Gewebe beeinträchtigen. Um dem zu begegnen, bauten die Autorinnen und Autoren ein hochporöses „metall‑organisches Gerüst“ (MOF) aus Beta‑Zyklodextrin, einem ringförmigen Zuckermolekül, das bereits in vielen Arzneimitteln Verwendung findet, in Kombination mit Kaliumionen. Dieses Gerüst verhält sich wie ein mikroskopischer Schwamm, voller winziger Hohlräume und Tunnel, die Wirkstoffmoleküle einschließen können. Das Team lud anschließend Olaparib in diese β‑CD‑MOF‑Partikel ein und erzeugte so ein festes Pulver mit gefüllten Mikroschwämmen.
Untersuchung der winzigen Schwämme
Die Forschenden mussten zunächst bestätigen, dass ihr Träger den Wirkstoff tatsächlich einschloss und dessen Eigenschaften veränderte. Sie bestimmten, wie viel Olaparib das Gerüst aufnehmen konnte, und fanden eine hohe Verkapselungseffizienz von etwa 76 %, was bedeutet, dass der Großteil des Medikaments in den Poren und nicht frei verblieb. Mithilfe einer Reihe physikalischer Tests – darunter kalorimetrische Messungen, Gewichtsverlust bei Erwärmung, Infrarot‑Spektren und Röntgenbeugung – beobachteten sie, dass das scharfe kristalline Signal von reinem Olaparib abgeschwächt war oder verschwand, sobald es im Gerüst untergebracht war. Diese Veränderung zeigte, dass der Wirkstoff nicht mehr als große Kristalle vorlag, sondern innerhalb der porösen Struktur des MOF verteilt war, was seine Stabilität und Löslichkeit verbessern kann.
Wie der Träger das Medikament freisetzt und schützt
Als Nächstes untersuchte das Team, wie Olaparib aus dem Gerüst in Flüssigkeiten entwich, die Körperbedingungen nachahmen. Im Vergleich zum freien Wirkstoff löste sich Olaparib innerhalb des β‑CD‑MOF vollständiger und wurde über 24 Stunden gleichmäßiger freigesetzt, insbesondere unter leicht sauren Bedingungen, wie sie in der Umgebung vieler Tumoren vorkommen. Diese Befunde deuten darauf hin, dass das poröse, zuckerbasierte Gerüst die Freisetzungsrate regulieren kann, einen anfänglichen Ausstoß verhindert und stattdessen eine gleichmäßigere, anhaltende Exposition bietet. Thermische Tests zeigten außerdem, dass die mit Wirkstoff beladenen Gerüste hitzebedingten Abbau besser widerstanden als der freie Wirkstoff oder das leere Gerüst, was darauf hinweist, dass die Verkapselung den Olaparib‑Molekülen zusätzlichen Schutz bietet.
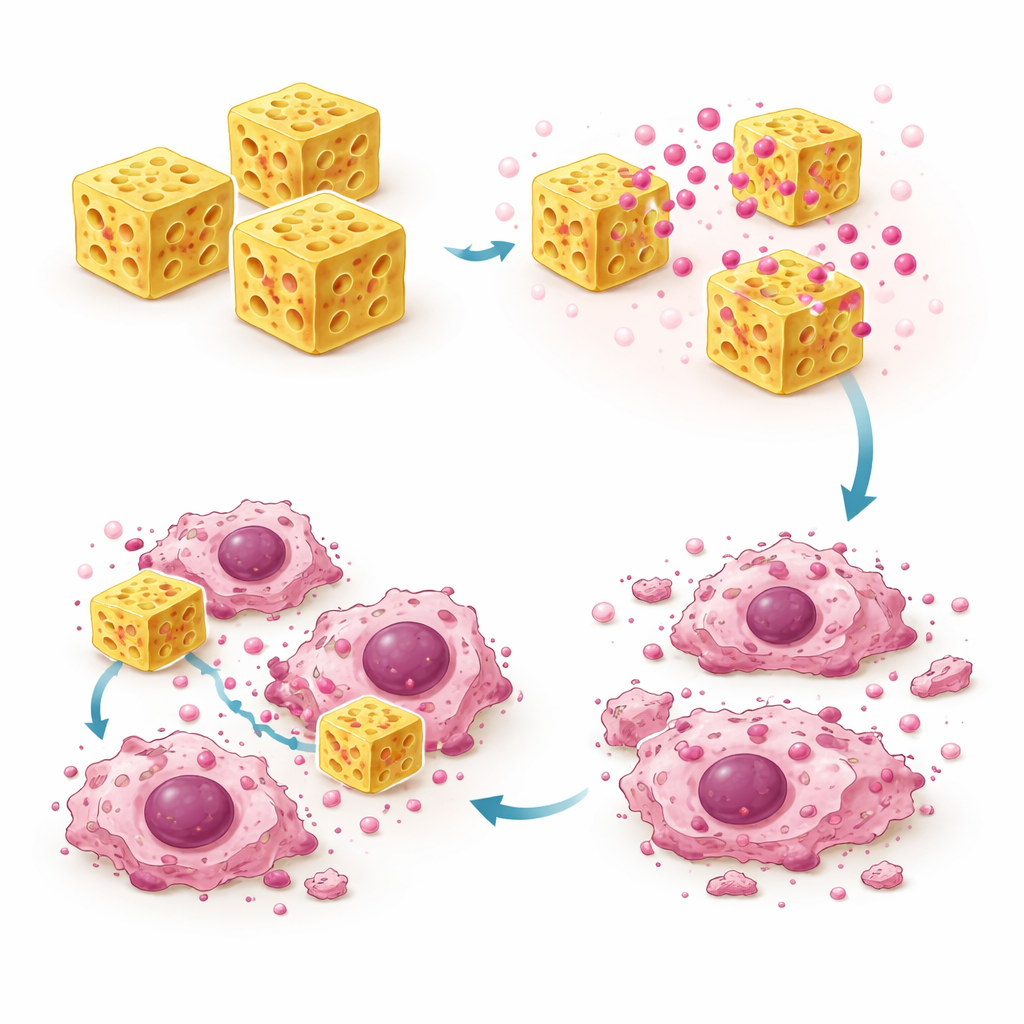
Stärkerer Angriff auf Gebärmutterhalskrebszellen
Um zu prüfen, ob diese intelligentere Abgabe in einer besseren Krebswirksamkeit resultiert, setzten die Autorinnen und Autoren TC‑1‑Gebärmutterhalskrebszellen, die in Kultur gezüchtet wurden, entweder freiem Olaparib oder dem in das β‑CD‑MOF geladenen Wirkstoff aus. Mit einem standardisierten Zellvitalitätstest stellten sie fest, dass die MOF‑Formulierung das Überleben der Krebszellen bei gleichen Dosen stärker reduzierte. Die zur Halbierung der Zellzahl erforderliche Konzentration (IC50) wurde ungefähr halbiert – von etwa 28 Nanomolar für freies Olaparib auf etwa 14 Nanomolar für die MOF‑beladene Version. Mikroskopische Untersuchungen bestätigten, dass behandelte Zellen schrumpften, rundlicher wurden und sich von der Oberfläche ablösten – klassische Anzeichen von Stress und programmierter Zellteilung. Messungen zweier Schlüsselfaktoren des Zelltods, p53 und Caspase‑9, zeigten, dass ihre Aktivität in Zellen, die dem MOF‑beladenen Wirkstoff ausgesetzt waren, stärker anstieg als bei Olaparib allein, was dafür spricht, dass die neue Formulierung eine intensivere Apoptose, also kontrollierten Zelltod, auslöst.
Was das für zukünftige Therapien bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass das Verpacken von Olaparib in winzige, zuckerbasierte Schwämme es im Labor wirksamer gegen Gebärmutterhalskrebszellen machen kann, zugleich eine gleichmäßigere Freisetzung und verbesserte Stabilität bietet. Obwohl diese Ergebnisse auf Reagenzglas‑ und Zellkulturversuche beschränkt sind und noch keinen Nachweis für Vorteile beim Menschen liefern, weisen sie auf eine vielversprechende Strategie hin: biokompatible, poröse Gerüste zu verwenden, um moderne zielgerichtete Wirkstoffe direkt zu Tumoren zu transportieren und schrittweise freizusetzen. Bestätigen weitere Tier‑ und klinische Studien diese Vorteile, könnten solche Formulierungen helfen, Dosen zu senken, Nebenwirkungen zu verringern und die Einsatzmöglichkeiten von Olaparib und ähnlichen Wirkstoffen im Kampf gegen Gebärmutterhalskrebs zu erweitern.
Zitation: Alsulays, B.B., Anwer, M.K., Hatata, M.N. et al. Development of β-CD metal organic frameworks loaded with olaparib: a novel approach for the treatment of cervical cancer. Sci Rep 16, 12911 (2026). https://doi.org/10.1038/s41598-026-43779-z
Schlüsselwörter: Gebärmutterhalskrebs, Olaparib, Arzneistofffreisetzung, metall-organische Gerüste, Zyklodextrin