Clear Sky Science · ru
Синтез, спектроскопическое исследование, теоретические выводы на основе DFT и биологическая оценка некоторых изатин-основанных металлических комплексов
Почему важны новые лекарства на основе металлов
Многие современные препараты основаны на углеродсодержащих молекулах, но перспективный класс средств возникает из неожиданных источников — металлов. В этом исследовании авторы спроектировали и протестировали три содержащие металл молекулы, созданные на основе небольшого циклического соединения изатина. Они задали простой, но важный вопрос: могут ли тщательно подобранные металлы, присоединённые к подходящему органическому остову, дать препараты, которые эффективнее борются с диабетом, раком печени и бактериальными инфекциями, чем исходная молекула?
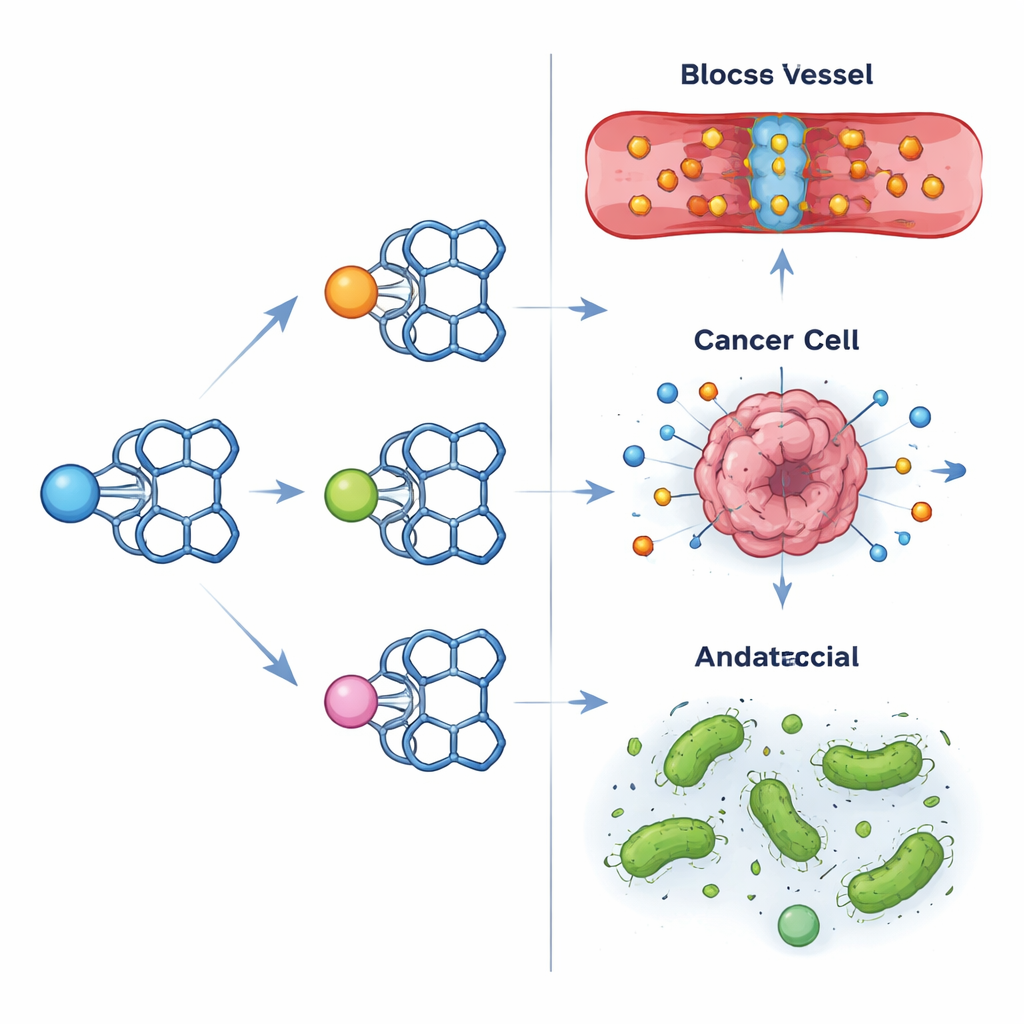
Создание гибкого химического остова
Сначала команда получила новый изатин-основанный «остов», химически связав два фрагмента изатина гибким эфирным мостиком. Эта структура, известная как шиф-основание (шлиф-основание), может захватывать ионы металлов в определённых позициях, подобно клешне. Затем к этому лиганду присоединили три разных металла — ванадий, никель и медь, сформировав три отдельных комплекса. С помощью набора аналитических методов, включая инфракрасную и УФ–видимую спектроскопию, магнитные измерения и термический анализ, они определили положение каждого металла в молекуле. Комплекс ванадия принял квадратную пирамида‑подобную конфигурацию, никель образовал тетраэдр, а медь — искажённую квадратную планарную форму. Эти тонкие различия в форме и связях оказались решающими для их биологического поведения.
Заглядывая в молекулы с помощью теории
Поскольку комплексы было трудно получить в виде кристаллов для рентгеноструктурных исследований, исследователи обратились к квантовой химии и использовали теорию функционала плотности (DFT) для моделирования структур в деталях. Расчёты показали, что лиганд предпочитает определённую «кето»-форму, в которой сохраняются два двойных C=O, и что атомы кислорода особенно привлекательны для ионов металлов. Анализ распределения электронов в высших заполненных и низших пустых молекулярных орбиталях показал, что координация металлов сужает энергетический разрыв между этими орбиталями. Это делает комплексы электронно «мягче» и более реакционноспособными по сравнению со свободным лигандом — признак, часто связанный с более сильными взаимодействиями в биологических системах. Иными словами, добавление металлов изменило не только форму молекул, но и то, насколько легко они могут вступать во взаимодействие с ферментами, клеточными мембранами и другими мишенями.
Испытания на действие в отношении уровня сахара, раковых клеток и бактерий
Чтобы оценить практический потенциал, авторы проверили лиганд и его металлические комплексы в трёх биологических моделях. Для антидиабетической активности они изучали, насколько хорошо каждое соединение блокирует α‑амилазу — пищеварительный фермент, расщепляющий крахмал до сахаров и способствующий скачкам уровня глюкозы в крови. Комплекс ванадия оказался явным лидером, значительно ингибируя фермент сильнее, чем лиганд, и приближаясь по эффективности к стандартному препарату, тогда как комплекс меди проявил умеренную активность, а комплекс никеля был в основном неактивен. В параллельных тестах против клеток рака печени (HepG-2) ванадиевый комплекс снова показал наибольшую активность, за ним следовала медь, а никель и свободный лиганд демонстрировали более слабые или пренебрежимые эффекты. Важно, что лиганд и никелевый комплекс оказались значительно менее токсичными для нормальных клеток лёгкого, что указывает на некоторую селективность.
Борьба с вредными микроорганизмами
Команда также оценивала антибактериальную активность в отношении грамположительных и грамотрицательных бактерий. Немодифицированный лиганд существенно не замедлял рост бактерий, но координация с металлами кардинально изменила ситуацию. Все три комплекса показали улучшенную активность, причём медный комплекс дал наибольшие зоны подавления роста для нескольких клинически значимых видов, включая Staphylococcus aureus, Escherichia coli и Klebsiella pneumoniae. Авторы предполагают, что хелатирование металлами делает молекулы более липофильными, помогая им проникать через жировые слои бактериальных мембран и нарушать жизненно важные процессы внутри клетки. Различия в размере, заряде и геометрии металлов дополнительно модифицируют способность каждого комплекса проникать и действовать на разные микроорганизмы.
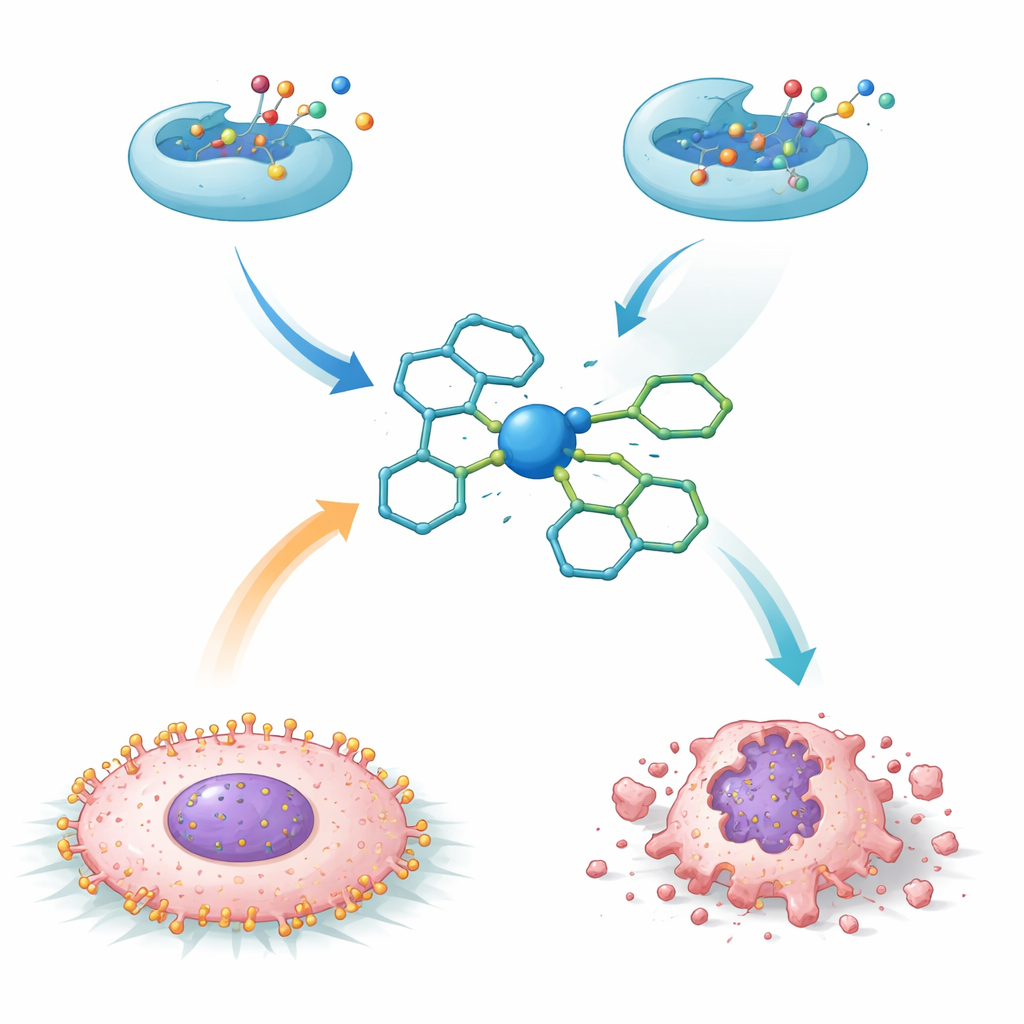
Что означают эти результаты для будущих терапий
В целом исследования показывают, что тщательно спроектированные изатин-основанные металлические комплексы могут превосходить исходный органический остов в различных биологических ролях. Ванадий, связанный с лигандом, выделяется как перспективный кандидат с двойным действием — сильная ингибиция ключевого фермента, связанного с диабетом, в сочетании с мощной активностью против клеток рака печени, тогда как координация с медью особенно эффективна против бактерий. Хотя эти результаты находятся на ранней лабораторной стадии и далеки от клинического применения, они демонстрируют, как замена и расположение ионов металлов на единой молекулярной платформе позволяет настраивать свойства для разных медицинских целей. Эта стратегия открывает путь к созданию универсальной платформы для разработки препаратов следующего поколения, содержащих металлы, для лечения метаболических заболеваний, рака и инфекций.
Цитирование: EL-Gammal, O.A., El-Boraey, H.A. & Tolan, D.A. Synthesis, spectroscopic investigation, theoretical insights via DFT and biological assessment of some isatin-based metal complexes. Sci Rep 16, 13151 (2026). https://doi.org/10.1038/s41598-026-41979-1
Ключевые слова: изатиновые металлические комплексы, терапевтические препараты на основе ванадия, металлооснованные противораковые агенты, ингибиторы ферментов при диабете, координационные соединения с антибактериальной активностью