Clear Sky Science · de
Synthese, spektroskopische Untersuchung, theoretische Einblicke mittels DFT und biologische Bewertung einiger isatin-basierter Metallkomplexe
Warum neue metallbasierte Medikamente wichtig sind
Viele heute verwendete Medikamente bestehen aus kohlenstoffbasierten Molekülen, doch eine wirksame neue Klasse von Therapeutika entsteht aus einer unerwarteten Quelle: Metallen. In dieser Studie entwarfen und testeten die Forschenden drei metallhaltige Moleküle auf Basis einer kleinen ringförmigen Verbindung namens Isatin. Sie stellten eine einfache, aber weitreichende Frage: Können sorgfältig ausgewählte Metalle, an das richtige organische Gerüst gebunden, Wirkstoffe erzeugen, die Diabetes, Leberkrebs und bakterielle Infektionen effektiver bekämpfen als das Ausgangsmolekül allein?
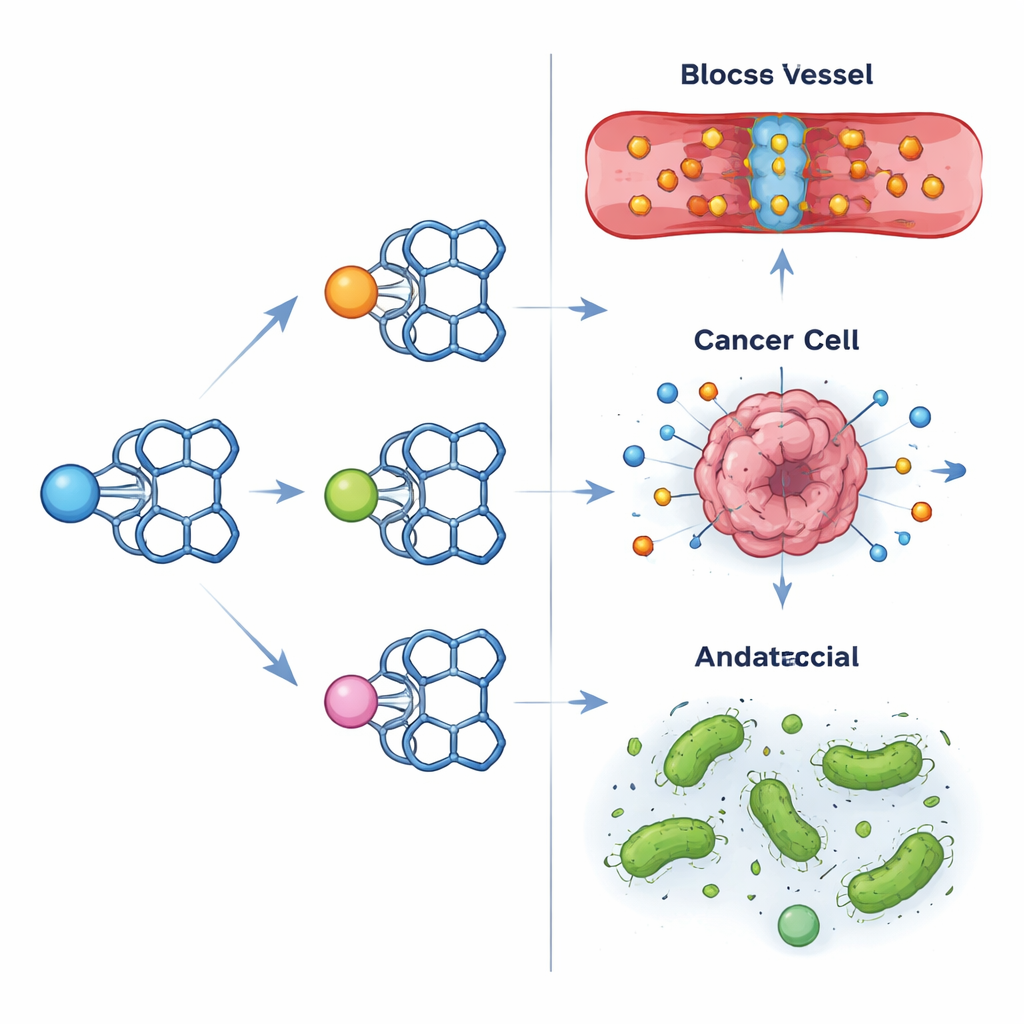
Aufbau eines flexiblen chemischen Gerüsts
Das Team stellte zunächst ein neues isatinbasiertes „Gerüst“ her, indem zwei Isatin-Einheiten über eine flexible Etherbrücke chemisch verknüpft wurden. Diese Struktur, bekannt als Schiffsbasenligand, kann Metallionen an bestimmten Positionen greifen, ähnlich einer Klaue. Anschließend banden sie drei verschiedene Metalle – Vanadium, Nickel und Kupfer – an diesen Liganden und bildeten drei separate Komplexe. Mithilfe eines Instrumentariums aus Infrarot- und Ultraviolett–sichtbarer Spektroskopie, magnetischen Messungen und thermischer Analyse bestimmten sie, wie jedes Metall im Molekül angeordnet war. Der Vanadiumkomplex nahm eine quadratisch-pyramidale Anordnung an, während Nickel eine tetraedrische Struktur und Kupfer eine verzerrt quadratisch-planare Gestalt bildete. Diese subtilen Unterschiede in Form und Bindungsverhalten erwiesen sich als entscheidend für ihr biologisches Verhalten.
Ein Blick in die Moleküle mit theoretischen Methoden
Da die Komplexe sich nur schwer für Röntgenstudien kristallisieren ließen, wandten sich die Forschenden der Quantenchemie zu und verwendeten die Dichtefunktionaltheorie (DFT), um die Strukturen im Detail zu modellieren. Die Rechnungen zeigten, dass der Ligand eine bestimmte „Keto“-Form bevorzugt, in der zwei Kohlenstoff–Sauerstoff-Doppelbindungen intakt sind, und dass die Sauerstoffatome besonders attraktiv für Metallionen sind. Durch die Untersuchung der Elektronenverteilung in den höchsten besetzten und den niedrigsten unbesetzten Molekülorbitalen fand das Team heraus, dass die Koordination der Metalle die Energielücke zwischen diesen Orbitalen verringert. Das macht die Komplexe elektronisch weicher und reaktiver als den freien Liganden, eine Eigenschaft, die oft mit stärkeren Wechselwirkungen in biologischen Systemen einhergeht. Mit anderen Worten: Das Hinzufügen von Metallen veränderte nicht nur die Form der Moleküle, sondern stellte auch ein, wie leicht sie mit Enzymen, Zellmembranen und anderen Zielstrukturen interagieren können.
Tests zu Wirkungen auf Blutzucker, Krebszellen und Bakterien
Um das realweltliche Potenzial zu prüfen, testeten die Forschenden den Liganden und seine Metallkomplexe in drei biologischen Kontexten. Für die antidiabetische Aktivität untersuchten sie, wie gut jede Verbindung α‑Amylase blockierte, ein Verdauungsenzym, das Stärke in Zucker zerlegt und zu Blutzuckerspitzen beiträgt. Der Vanadiumkomplex war der klare Favorit: Er hemmte das Enzym deutlich stärker als der Ligand und kam nahe an die Leistung eines Standardmedikaments heran, während der Kupferkomplex moderate Aktivität zeigte und der Nickelkomplex weitgehend inaktiv war. In parallelen Tests an Leberkrebszellen (HepG-2) erwies sich erneut der Vanadiumkomplex als am wirksamsten, gefolgt vom Kupferkomplex; Nickel und der freie Ligand zeigten schwächere oder vernachlässigbare Effekte. Wichtig ist, dass der Ligand und der Nickelkomplex deutlich weniger toxisch gegenüber normalen Lungenzellen waren, was auf eine gewisse Selektivität hindeutet.
Bekämpfung schädlicher Mikroben
Das Team bestimmte außerdem die antibakterielle Aktivität gegen grampositive und gramnegative Bakterien. Der unveränderte Ligand verlangsamte das bakterielle Wachstum nicht signifikant, doch die Metallkoordination veränderte dieses Bild dramatisch. Alle drei Komplexe zeigten verbesserte Wirkung, wobei der Kupferkomplex die größten Hemmzonen gegen mehrere klinisch relevante Arten, darunter Staphylococcus aureus, Escherichia coli und Klebsiella pneumoniae, erzeugte. Die Autorinnen und Autoren vermuten, dass die Chelatbildung mit Metallen die Moleküle lipophiler macht, sodass sie leichter durch die fettigen Schichten bakterieller Membranen gelangen und dort lebenswichtige Prozesse stören können. Unterschiede in Metallgröße, Ladung und Geometrie modulieren zudem, wie gut jeder Komplex in verschiedene Mikroben eindringt und wirkt.
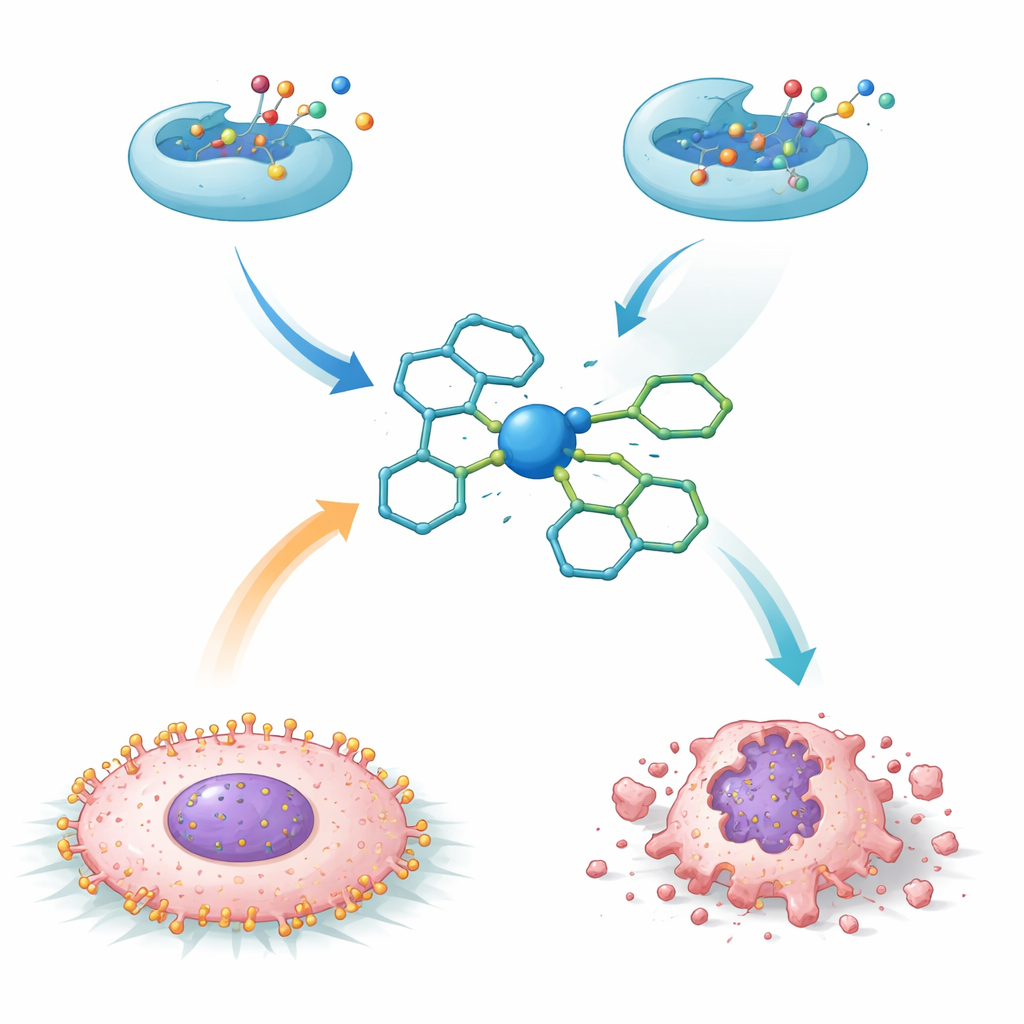
Was diese Befunde für künftige Therapien bedeuten
Insgesamt zeigt die Arbeit, dass sorgfältig konstruierte isatin‑basierte Metallkomplexe das ursprüngliche organische Gerüst in mehreren biologischen Rollen übertreffen können. An den Liganden gebundenes Vanadium sticht als vielversprechender Kandidat mit Doppelwirkung hervor: starke Hemmung eines diabetesrelevanten Schlüsselenzyms und gleichzeitig kräftige Aktivität gegen Leberkrebszellen, während Kupferkoordination besonders gegen Bakterien brilliert. Obwohl diese Ergebnisse noch in einem frühen, laborbasierten Stadium und weit von einer klinischen Anwendung entfernt sind, verdeutlichen sie, wie das Auswählen und Anordnen von Metallionen auf einem einzigen molekularen Rahmen Eigenschaften für verschiedene medizinische Ziele gezielt einstellen kann. Diese Strategie weist auf eine vielseitige Plattform zur Entwicklung der nächsten Generation metallhaltiger Arzneimittel gegen Stoffwechselerkrankungen, Krebs und Infektionen hin.
Zitation: EL-Gammal, O.A., El-Boraey, H.A. & Tolan, D.A. Synthesis, spectroscopic investigation, theoretical insights via DFT and biological assessment of some isatin-based metal complexes. Sci Rep 16, 13151 (2026). https://doi.org/10.1038/s41598-026-41979-1
Schlüsselwörter: isatin Metallkomplexe, vanadiumbasierte Therapeutika, metallbasierte Antikrebsmittel, antidiabetische Enzyminhibitoren, antibakterielle Koordinationsverbindungen