Clear Sky Science · ru
Блокирование рецепторов AT1 телмисартаном защищает клетки SH‑SY5Y от паркинсонической нейротоксичности, вызванной 6‑OHDA
Почему это важно для здоровья мозга
Болезнь Паркинсона наиболее известна своими треморами и нарушениями движений, но глубоко в мозге заболевание обусловлено стрессом и гибелью нервных клеток. В этом исследовании изучали, может ли распространённый препарат от высокого давления — телмисартан — защитить клетки, похожие на мозговые, от связанных с Паркинсоном повреждений в лабораторных условиях. Если аналогичная защита проявится у людей, препараты, уже доступные в аптеках, могли бы однажды помочь замедлить, а не только маскировать, это разрушительное заболевание.
Ближе к проблемам при Паркинсоне
Болезнь Паркинсона поражает миллионы людей во всём мире и характеризуется потерей дофаминергических нейронов и накоплением липкой белковой массы — альфа‑синуклеина. Существующие лечения, такие как L‑DOPA, улучшают симптомы, но не останавливают гибель этих клеток, а длительное применение может вызывать побочные эффекты, например непроизвольные движения. Учёные знают, что хроническое воспаление, избыток реактивных молекул — часто называемый «окислительным стрессом» — и агрегация белков способствуют медленной дегенерации мозговых клеток, но превратить эту сложную сеть причин в эффективную защиту оказалось непросто.
Нелёгкий союзник из препаратов против давления
Помимо роли в регуляции артериального давления, ренин‑ангиотензиновая система действует и в мозге, где влияет на кровоток, воспаление и выживаемость клеток. Один из её ключевых «переключателей», рецептор AT1, при чрезмерной активности может усиливать воспаление и окислительные повреждения, способствуя гибели дофаминергических нейронов и накоплению альфа‑синуклеина. Телмисартан, блокатор этого рецептора, уже показал защитный эффект в животных моделях, похожих на паркинсоническое повреждение. Авторы поставили цель проверить, сможет ли телмисартан аналогично защитить полученные от человека нервоподобные клетки в строго контролируемом культуре.
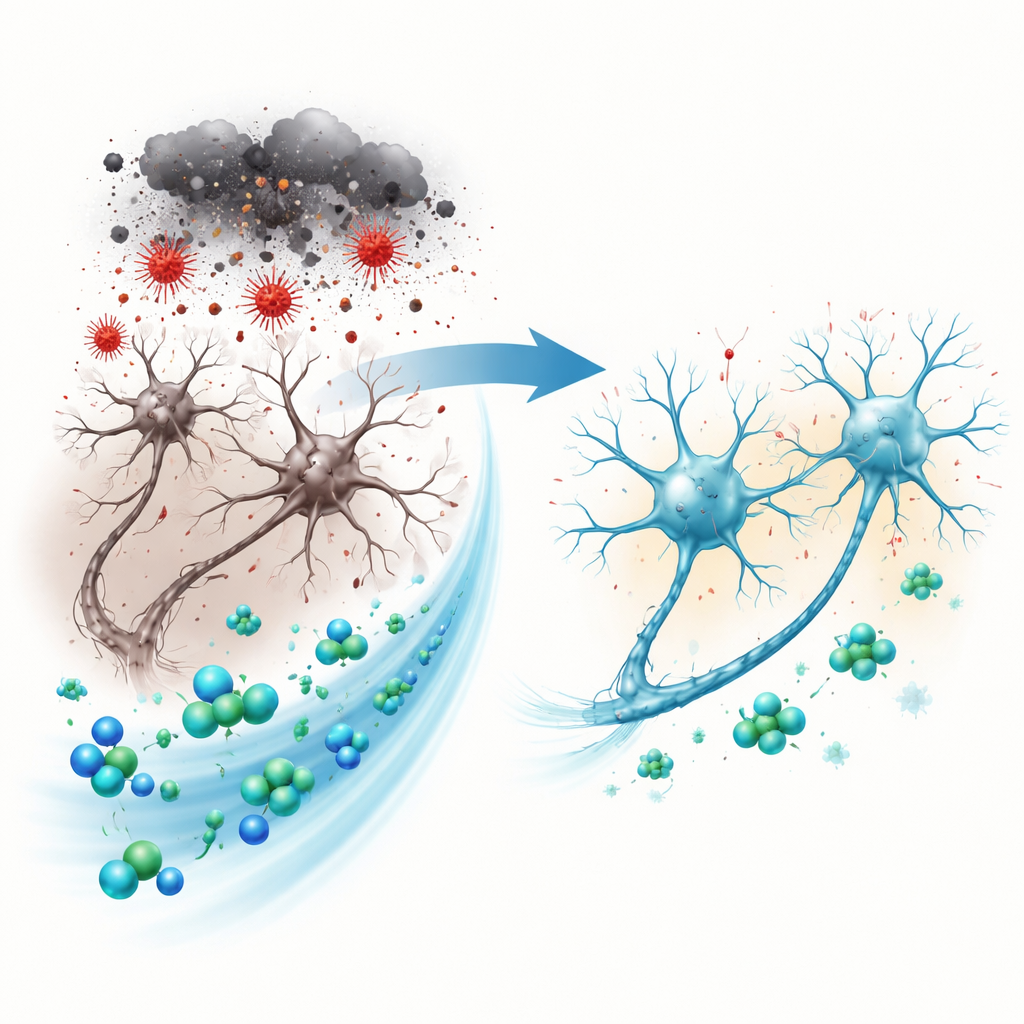
Создание стресса для клеток мозга в лаборатории
Команда использовала клетки SH‑SY5Y, широко применяемую человеческую линию, которая во многих отношениях ведёт себя как незрелые нейроны. Чтобы смоделировать повреждение, связанное с Паркинсоном, они подвергали эти клетки 6‑гидроксидопамину (6‑OHDA) — токсину, который напоминает дофамин и селективно поражает дофаминоподобные клетки, вызывая окислительный стресс, нарушение митохондрий и программируемую гибель. Перед введением токсина клетки обрабатывали разными дозами телмисартана. Затем измеряли выживаемость клеток, степень утечек и повреждений, а также уровень различных маркёров стресса и воспаления.
Как телмисартан успокоил клеточный шторм
При одном только воздействии 6‑OHDA клетки демонстрировали резкое падение выживаемости и всплеск активности фермента, связанного с повреждением — признаки массовой гибели или тяжёлого повреждения. Уровни малонового диальдегида, побочного продукта повреждения липидов, резко возросли, в то время как собственные антиоксидантные защиты клеток — молекулы и ферменты, нейтрализующие вредные реактивные виды — значительно снизились. Одновременно сильную активацию проявили гены, связанные с воспалением и программируемой гибелью, включая несколько ключевых провоспалительных посредников и каспазу‑3, белок‑исполнителя. В отличие от этого, клетки, предварительно обработанные телмисартаном, чувствовали себя значительно лучше: выжило больше клеток, утечки уменьшились, маркёры окислительного повреждения снизились, а антиоксидантные системы восстановились.
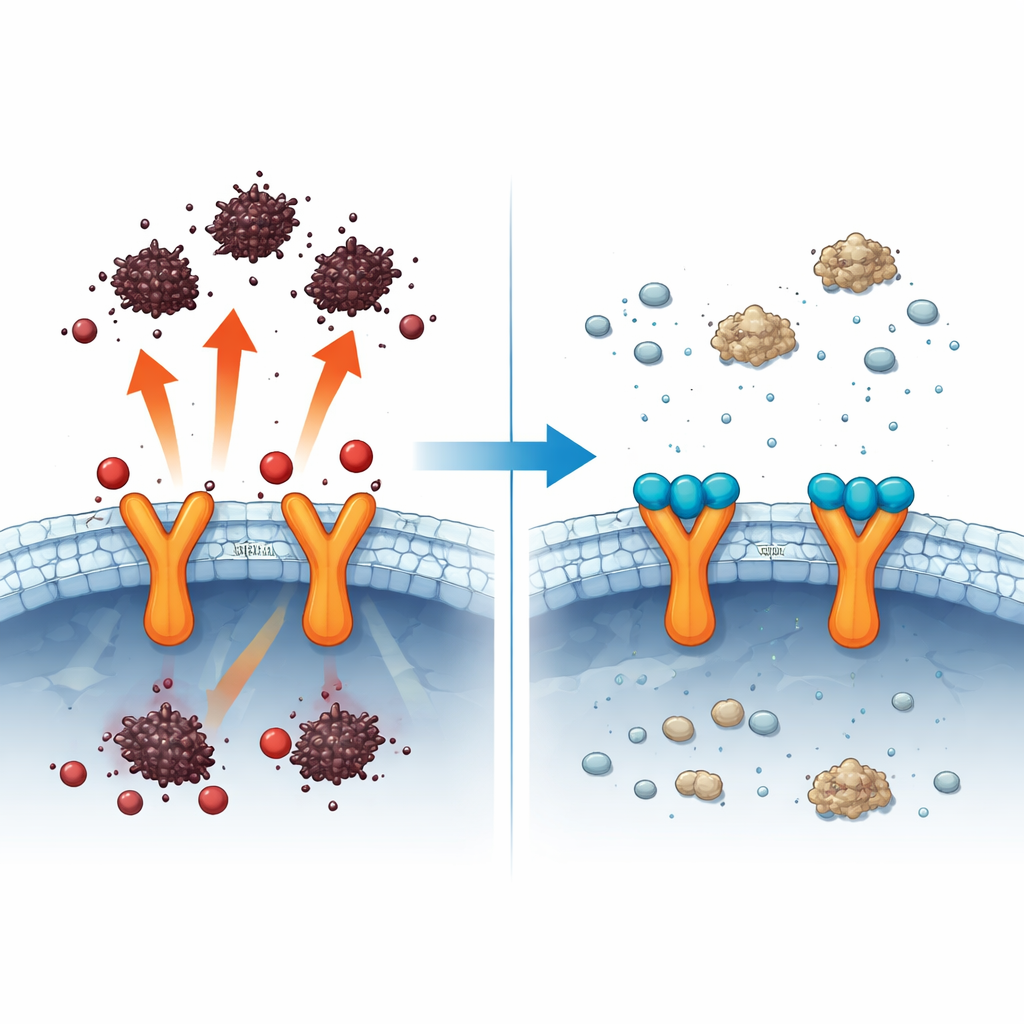
Уменьшение воспаления и накопления белка
Телмисартан также изменил воспалительный профиль клеток. Токсин повышал уровни провоспалительных молекул, таких как TNF‑альфа, IL‑6, NF‑kappaB и IL‑1 бета, которые часто повышены у пациентов с Паркинсоном и, как считается, ускоряют потерю нейронов. Телмисартан снизил эти вредные сигналы и повысил IL‑10 — молекулу, известную своей успокаивающей и защитной ролью в иммунитете. Под микроскопом клетки, подвергшиеся 6‑OHDA, накапливали яркие кластеры альфа‑синуклеина и IL‑1 бета, повторяя агрегацию белка и воспалительную активность, наблюдаемые в мозге при Паркинсоне. При обработке телмисартаном эти флуоресцентные сигналы значительно уменьшились, что указывает на снижение агрегации белков и более спокойную воспалительную среду.
Что это может означать для будущих методов лечения
Проще говоря, в лабораторной модели паркинсонического повреждения телмисартан действовал как щит для уязвимых мозго‑подобных клеток: помогал им выдерживать токсический стресс, ослаблял неконтролируемое воспаление и ограничивал накопление проблемных белков. Хотя эти результаты получены на клеточных культурах — не на людях — и не способны отразить всю сложность живого мозга, они добавляют доказательств в пользу идеи, что блокирование рецепторов AT1 может предложить многоцелевой подход к защите дофаминовых нейронов. При дальнейшем тестировании на животных и, в конечном счёте, у пациентов, препараты вроде телмисартана могут стать частью будущих стратегий, направленных не только на облегчение симптомов Паркинсона, но и на замедление самого заболевания.
Цитирование: Gundogdu, O.L., Burul, F., Akyol, E.T. et al. Targeting AT1 receptors with telmisartan protects SH-SY5Y cells from 6-OHDA induced Parkinsonian neurotoxicity. Sci Rep 16, 12298 (2026). https://doi.org/10.1038/s41598-026-40095-4
Ключевые слова: Болезнь Паркинсона, телмисартан, нейропротекция, окислительный стресс, рецептор ангиотензина AT1