Clear Sky Science · fr
Le ciblage des récepteurs AT1 avec le télmisartan protège les cellules SH‑SY5Y de la neurotoxicité parkinsonienne induite par le 6‑OHDA
Pourquoi cela compte pour la santé cérébrale
La maladie de Parkinson est surtout connue pour ses tremblements et ses troubles du mouvement, mais au cœur du cerveau, ce trouble est entraîné par des cellules nerveuses stressées et en train de mourir. Cette étude examine si un médicament courant contre l’hypertension, le télmisartan, peut protéger en laboratoire des cellules de type cérébral contre les dommages associés à la maladie de Parkinson. Si une protection similaire se produisait chez l’humain, des médicaments déjà disponibles en pharmacie pourraient un jour aider à ralentir — et non seulement masquer — cette maladie dévastatrice.
Un regard plus précis sur les problèmes liés à la maladie de Parkinson
La maladie de Parkinson touche des millions de personnes dans le monde et se caractérise par la perte de neurones producteurs de dopamine et l’accumulation d’une protéine collante appelée alpha‑synucléine. Les traitements actuels, comme la L‑DOPA, améliorent les symptômes mais n’empêchent pas ces cellules de mourir, et un usage prolongé peut entraîner des effets secondaires tels que des mouvements involontaires. Les chercheurs savent que l’inflammation chronique, l’excès de molécules réactives souvent qualifié de « stress oxydatif » et l’agrégation protéique contribuent à la dégénérescence progressive des cellules cérébrales, mais convertir ce réseau complexe en une protection efficace reste difficile.
Un allié inattendu venu des médicaments antihypertenseurs
Au‑delà de son rôle dans le contrôle de la pression artérielle, le système rénine‑angiotensine agit aussi dans le cerveau, où il peut influencer le flux sanguin, l’inflammation et la survie cellulaire. L’un de ses interrupteurs clés, le récepteur AT1, peut provoquer des dommages inflammatoires et oxydatifs lorsqu’il est suractivé, favorisant la mort des neurones producteurs de dopamine et l’accumulation d’alpha‑synucléine. Le télmisartan, un bloqueur de ce récepteur, a déjà montré des effets protecteurs dans des modèles animaux de lésions de type parkinsonien. Les auteurs ont cherché à tester si le télmisartan pouvait protéger de la même manière des cellules d’origine humaine en culture, dans une expérience strictement contrôlée.
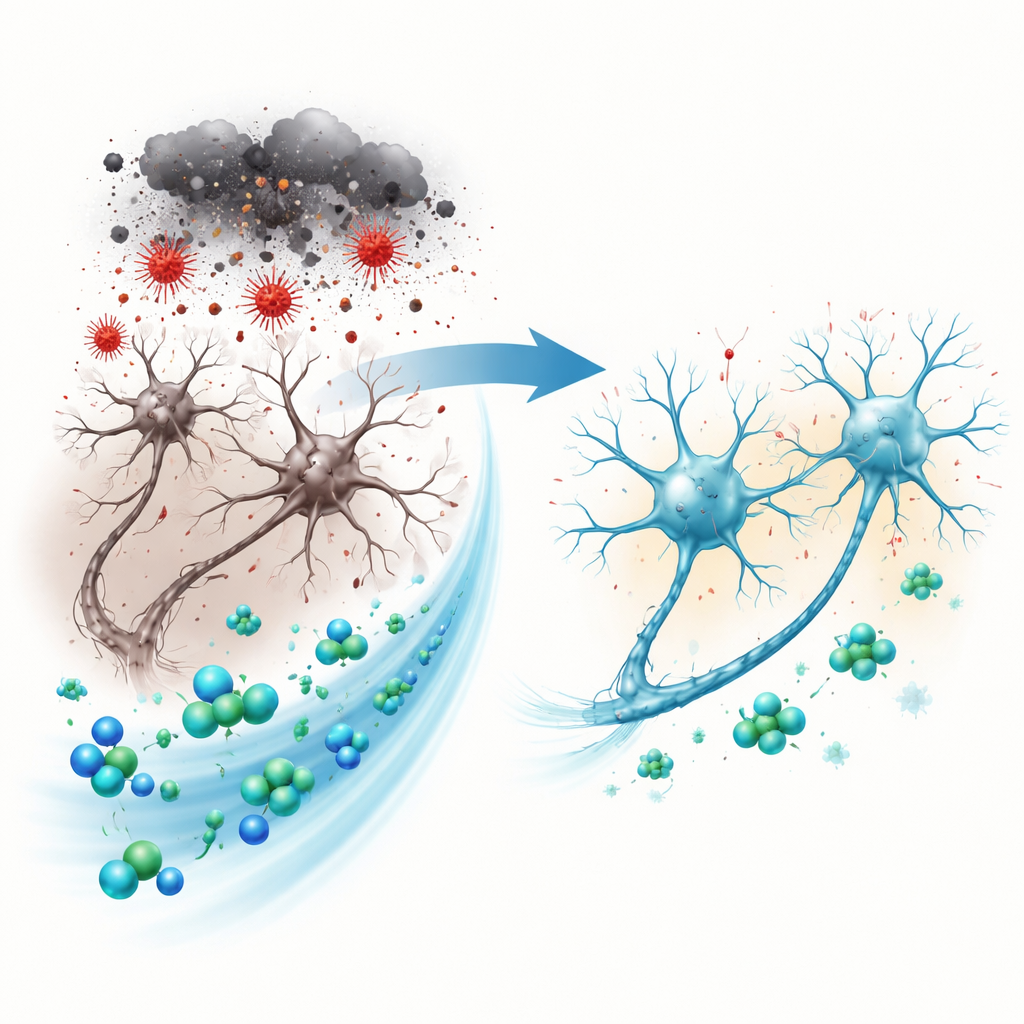
Soumettre des cellules cérébrales au stress en laboratoire
L’équipe a utilisé des cellules SH‑SY5Y, une lignée humaine largement employée qui se comporte de nombreuses façons comme des neurones immatures. Pour imiter la lésion liée à la maladie de Parkinson, elles ont exposé ces cellules à la 6‑hydroxydopamine (6‑OHDA), une toxine ressemblant à la dopamine qui endommage sélectivement les cellules dopaminergiques en déclenchant un stress oxydatif, un dysfonctionnement mitochondrial et une mort cellulaire programmée. Avant l’ajout de la toxine, les cellules ont été traitées par différentes doses de télmisartan. Les chercheurs ont ensuite mesuré le nombre de cellules survivantes, leur perméabilité et leurs dégâts, ainsi que l’activation de divers marqueurs de stress et d’inflammation.
Comment le télmisartan a calmé la tempête cellulaire
Exposées à la 6‑OHDA seules, les cellules ont montré une forte chute de viabilité et une montée d’une enzyme associée aux dommages, signes que beaucoup étaient en train de mourir ou gravement blessées. Les niveaux de malondialdéhyde, un sous‑produit de l’oxydation des lipides, ont augmenté de manière marquée, tandis que les défenses antioxydantes propres aux cellules — molécules et enzymes neutralisant les espèces réactives — étaient fortement réduites. Parallèlement, des gènes liés à l’inflammation et à la mort cellulaire, y compris plusieurs médiateurs pro‑inflammatoires majeurs et la protéine exécutrice caspase‑3, ont été fortement activés. En revanche, les cellules prétraitées au télmisartan s’en sont beaucoup mieux tirées : davantage ont survécu, la fuite cellulaire a diminué, les marqueurs de dommages oxydatifs ont chuté et les systèmes antioxydants se sont rétablis.
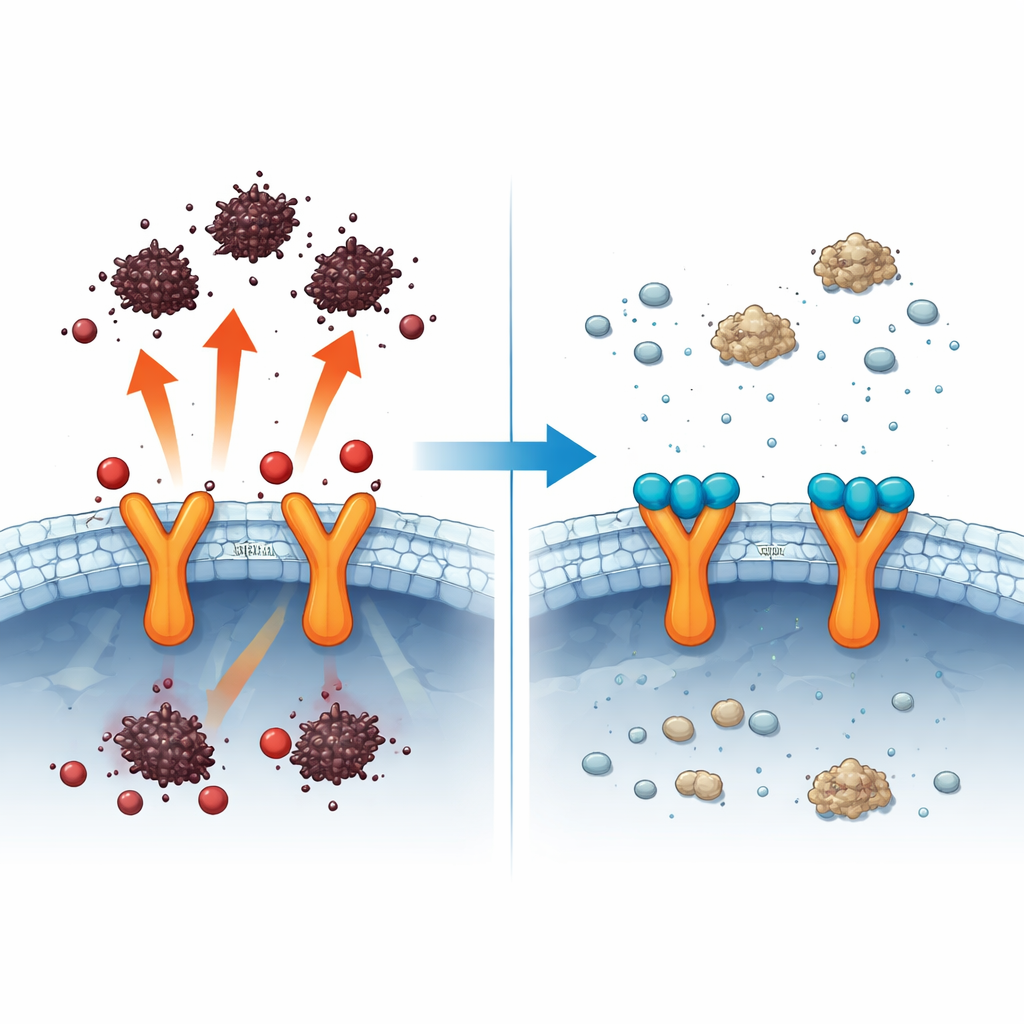
Réduire l’inflammation et l’accumulation protéique
Le télmisartan a aussi modifié l’équilibre inflammatoire des cellules. La toxine a augmenté des molécules pro‑inflammatoires telles que le TNF‑alpha, l’IL‑6, le NF‑kappaB et l’IL‑1 beta, souvent élevées chez les patients parkinsoniens et considérées comme accélératrices de la perte neuronale. Le télmisartan a réduit ces signaux nocifs tout en augmentant l’IL‑10, une molécule connue pour son rôle calmant et protecteur dans le système immunitaire. Au microscope, les cellules exposées à la 6‑OHDA ont accumulé des amas brillants d’alpha‑synucléine et d’IL‑1 beta, reflétant les agrégats protéiques et l’activité inflammatoire observés dans le cerveau des personnes atteintes de Parkinson. Avec le traitement au télmisartan, ces signaux fluorescents étaient nettement réduits, suggérant moins d’agrégation protéique et un environnement inflammatoire plus apaisé.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, le télmisartan a agi comme un bouclier pour des cellules cérébrales vulnérables dans un modèle en culture de lésions parkinsoniennes, les aidant à résister au stress toxique, à atténuer l’inflammation débridée et à limiter l’accumulation de protéines problématiques. Bien que ces résultats proviennent de cultures cellulaires — et non d’êtres humains — et ne puissent pas reproduire la complexité d’un cerveau vivant, ils renforcent l’idée que le blocage des récepteurs AT1 pourrait offrir une approche multitarget pour protéger les neurones producteurs de dopamine. Après des tests complémentaires chez l’animal et, éventuellement, chez le patient, des médicaments comme le télmisartan pourraient faire partie de stratégies futures visant non seulement à soulager les symptômes de la maladie de Parkinson, mais aussi à ralentir son évolution.
Citation: Gundogdu, O.L., Burul, F., Akyol, E.T. et al. Targeting AT1 receptors with telmisartan protects SH-SY5Y cells from 6-OHDA induced Parkinsonian neurotoxicity. Sci Rep 16, 12298 (2026). https://doi.org/10.1038/s41598-026-40095-4
Mots-clés: maladie de Parkinson, télmisartan, neuroprotection, stress oxydatif, récepteur de l’angiotensine AT1