Clear Sky Science · ru
Модификация лигандов формирует гидрофобные микроокружения для эффективного электрокаталитического окисления жирных спиртов
Превращая жир в зелёную химию
Повседневные продукты — от мыла и шампуней до смазок — используют жирные спирты: маслянистые молекулы, которые трудно перерабатывать чисто в водной среде. Традиционные методы превращения этих спиртов в более полезные жирные кислоты часто требуют агрессивных реагентов и драгоценных металлов. В этом исследовании показано, как хитрое молекулярное проектирование может обойти эти недостатки, используя электричество и специально подобранный катализатор для более эффективного и устойчивого преобразования маслянистых молекул в воде.
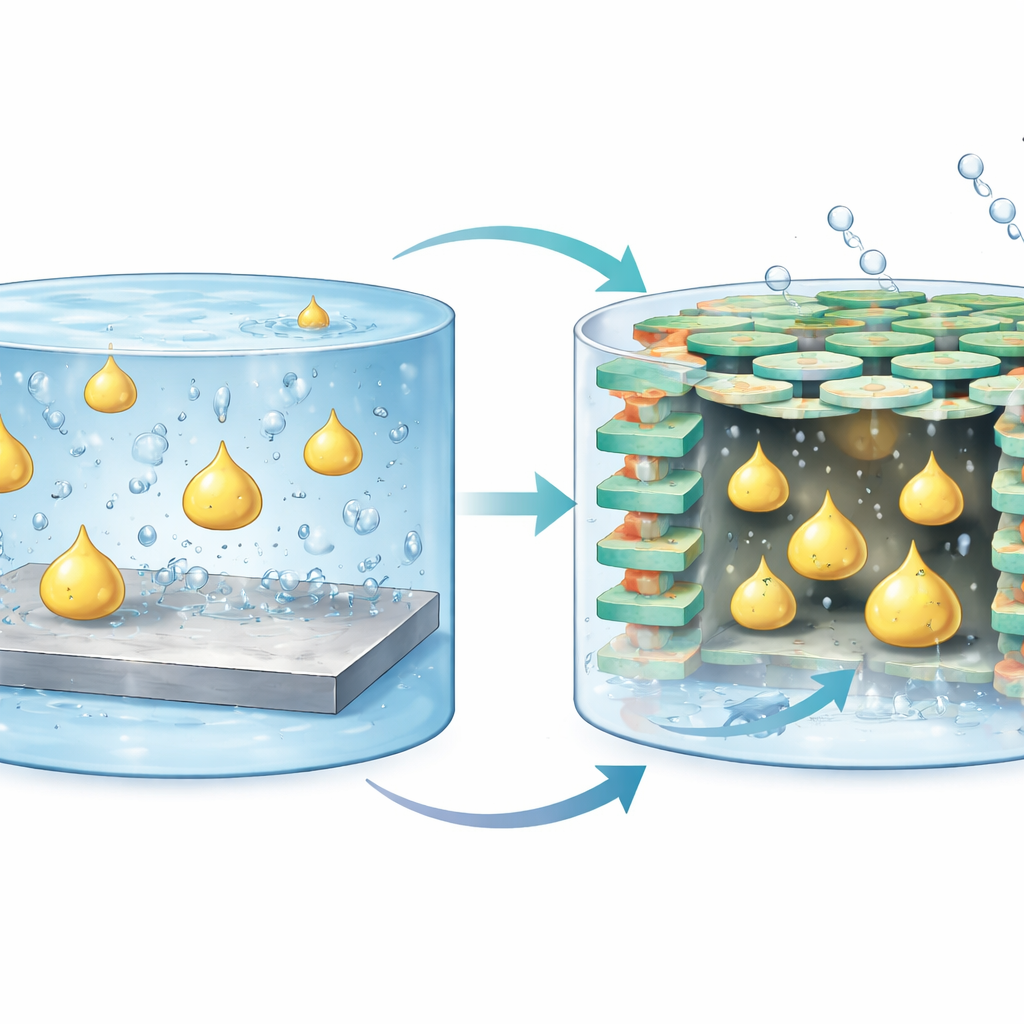
Почему маслянистые молекулы так трудно усмирить
Жирные спирты не любят воду, в то время как большинство промышленных электрохимических систем работают в водных растворах. Это несоответствие приводит к тому, что маслянистые реагенты остаются далеко от поверхности твердого катализатора, замедляя реакцию и давая кислородному образованию преимущество. Стандартные катализаторы на основе гидроксида никеля хорошо работают для мелких, водорастворимых спиртов, например метанола, но испытывают трудности с длинноцепочечными жирными спиртами. В результате наблюдаются вялое превращение, потери электрической энергии и образование большого количества нежелательного кислорода вместо целевых жирных кислот.
Заимствование трюка у природных ферментов
Природа уже решила похожую задачу. Ферменты, такие как химотрипсин, используют кластеры ароматических аминокислот для создания «гидрофобных карманов», которые притягивают маслянистые молекулы и удерживают их в нужном положении для реакции. Вдохновлённые этой идеей, исследователи построили никельсодержащие металло‑органические каркасы (Ni‑MOF), где атомы никеля связаны органическими лигандами, несущими одну, две или три бензольные кольца. Увеличивая число колец, они могли настраивать степень отталкивания воды и структуру внутренней среды катализатора, стремясь создать карманы, похожие на ферментативные, на неорганическом остове.
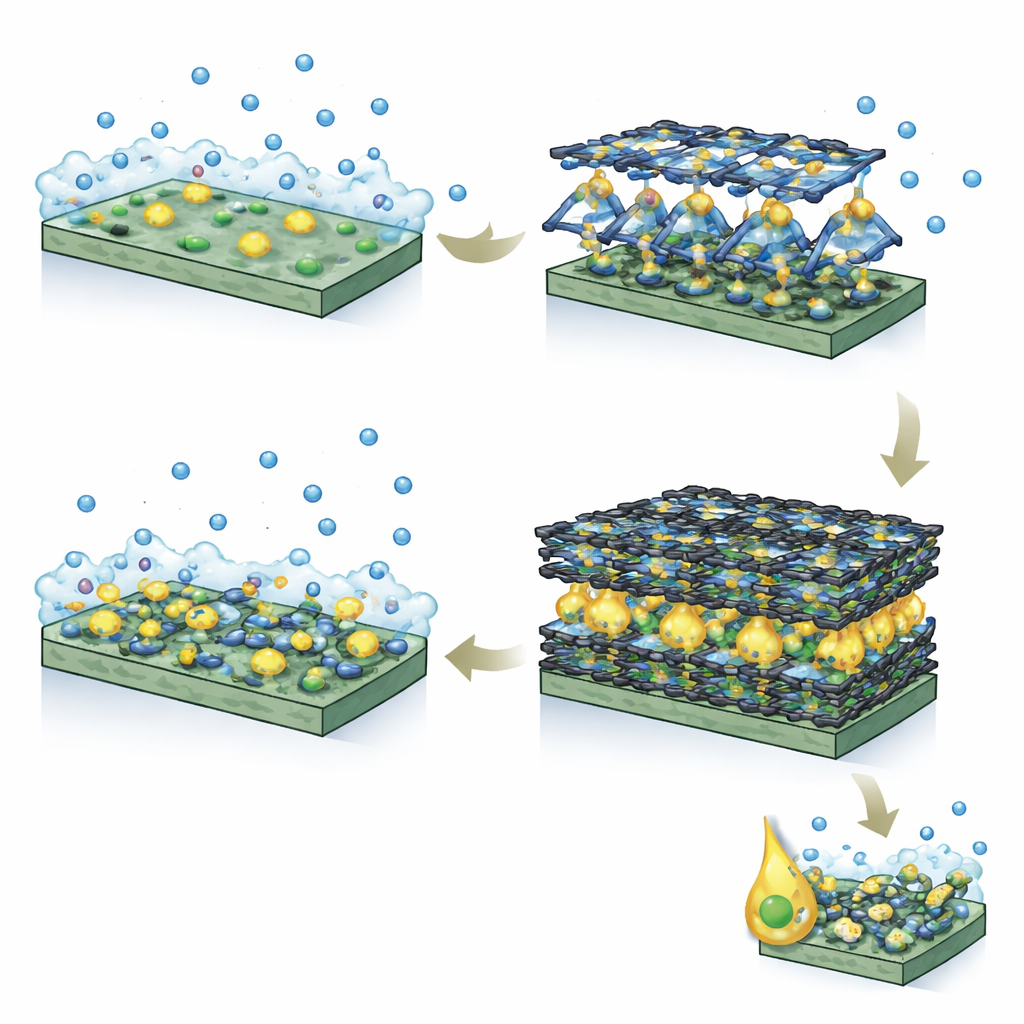
Создание лучшего микроскопического «дома» для жирных спиртов
Команда синтезировала три слоистых Ni‑MOF и сравнила их с обычным гидроксидом никеля. Они обнаружили, что версия с самым длинным лигандом, построенная из терфенилового (трёхкольцевого) звена и обозначенная Ni‑TPDC, создавала наиболее гидрофобную внутреннюю среду. Эксперименты по измерению растекания капель октанола и поглощению масляного красителя показали, что Ni‑TPDC привлекает примерно вдвое больше жирного спирта, чем гидроксид никеля. Компьютерные моделирования подтвердили это, показав, что молекулы октанола сильно накапливаются у поверхности Ni‑TPDC благодаря усиленным ван‑дер‑ваальсовым взаимодействиям в его ароматически выстланных каналах.
Сохранение каркаса катализатора целым
Обычная слабость электродов на основе MOF — их разрушение в жёстких условиях, необходимых для окислительных реакций, с потерей тщательно спроектированной внутренней архитектуры. В этом исследовании детальные рентгеновские и колебательные спектроскопические данные показали важную разницу между тремя Ni‑MOF. В материалах с более короткими лигандами органические мостики отщеплялись в ходе работы, и структура превращалась в аморфную фазу, похожую на гидроксид никеля. Напротив, Ni‑TPDC сохранял свой слоистый кристаллический каркас даже после многих циклов активации и часов электролиза. Дополнительное бензольное кольцо обеспечивало сильную укладку соседних лигандов, действуя как сцепляющаяся плитка, которая удерживает решётку, в то время как только внешняя поверхность частично превращается в активный слой никель‑оксигидроксида.
Более быстрые реакции, меньше побочных продуктов
При использовании октанола в качестве модельного жирного спирта Ni‑TPDC существенно превзошёл стандартный гидроксид никеля. При рабочих напряжениях он обеспечивал примерно в три раза большую скорость образования октановой кислоты при Фарадеевой эффективности выше 80%, по сравнению с примерно 30% для гидроксида никеля, где доминировало образование кислорода. Тщательный анализ показал, что превосходство Ni‑TPDC не объясняется просто большим числом активных никелевых сайтов или значительно большей площадью поверхности; его гидрофобное микроокружение эффективнее подводило жирные спирты в реакционную зону, облегчая транспорт массы. Оптимизированный катализатор завершал полное превращение октанола в октановую кислоту всего за 3,5 часа с практически 100% селективностью, достигая скоростей производства, сопоставимых с современными термическими методами окисления, которые обычно опираются на драгоценные металлы.
От лабораторной концепции к практическим энергетическим системам
Чтобы проверить потенциал в реальных условиях, авторы интегрировали Ni‑TPDC в проточную ячейку, где окисление жирных спиртов на аноде совмещено с генерацией водорода на катоде. Поскольку окисление октанола легче, чем выделение кислорода при разложении воды, общее напряжение ячейки снижалось почти на 0,2 вольта при практических плотностях тока, уменьшив энергетические затраты на производство водорода и одновременно обеспечив получении ценной жирной кислоты. Система работала стабильно в течение 48 часов с высокими выходами как водорода, так и октановой кислоты. Для неспециалистов ключевая мысль такова: спроектировав микросреду катализатора более «дружелюбной к маслу», но при этом структурно прочной, можно чисто преобразовывать маслянистые молекулы в воде с использованием возобновляемой электроэнергии, открывая путь к более экологичному производству повседневных химикатов и более эффективным схемам получения энергии на основе водорода.
Цитирование: Du, R., Chen, Z., Zhang, B. et al. Ligand engineering tailors hydrophobic microenvironments for efficient electrocatalytic oxidation of fatty alcohol. Nat Commun 17, 3628 (2026). https://doi.org/10.1038/s41467-026-70501-4
Ключевые слова: органическая электрокатализ, окисление жирных спиртов, гидрофобные катализаторы, металло‑органические каркасы, зелёный водород