Clear Sky Science · pt
Engenharia de ligantes ajusta microambientes hidrofóbicos para oxidação eletrocatalítica eficiente de álcool graxo
Transformando gordura em química verde
Produtos do dia a dia, de sabonetes e xampus a lubrificantes, dependem de álcoois graxos — moléculas oleosas que são notoriamente difíceis de processar de forma limpa em água. Métodos tradicionais para converter esses álcoois em ácidos graxos mais úteis costumam exigir produtos químicos agressivos e metais preciosos. Este estudo mostra como um desenho molecular inteligente pode contornar essas desvantagens, usando eletricidade e um catalisador cuidadosamente ajustado para transformar moléculas oleosas em água de maneira mais eficiente e sustentável.
Por que moléculas oleosas são tão difíceis de domar
Álcoois graxos não gostam de água, e a maioria dos sistemas eletroquímicos industriais opera em soluções aquosas. Esse descompasso faz com que os reagentes oleosos tendam a ficar afastados da superfície sólida do catalisador, retardando a reação e dando vantagem à formação de oxigênio. Catalisadores convencionais de hidróxido de níquel funcionam bem para álcoois pequenos e hidrofílicos, como o metanol, mas têm dificuldade com álcoois graxos de cadeia longa. O resultado é conversão lenta, desperdício de energia elétrica e muito oxigênio indesejado em vez dos ácidos graxos desejados.
Tomando emprestado um truque das enzimas da natureza
A natureza já resolveu um problema semelhante. Enzimas como a quimotripsina usam aglomerados de aminoácidos aromáticos para construir “bolsos hidrofóbicos” que atraem moléculas oleosas e as mantêm na posição exata para a reação. Inspirados por essa ideia, os pesquisadores construíram estruturas metal–orgânicas à base de níquel (Ni‑MOFs), nas quais átomos de níquel são ligados por moléculas orgânicas contendo um, dois ou três anéis benzênicos. Ao aumentar o número de anéis, eles puderam ajustar o quão repelente à água e estruturalmente robusto seria o ambiente interno do catalisador, visando criar bolsos semelhantes aos enzimáticos em um arcabouço inorgânico.
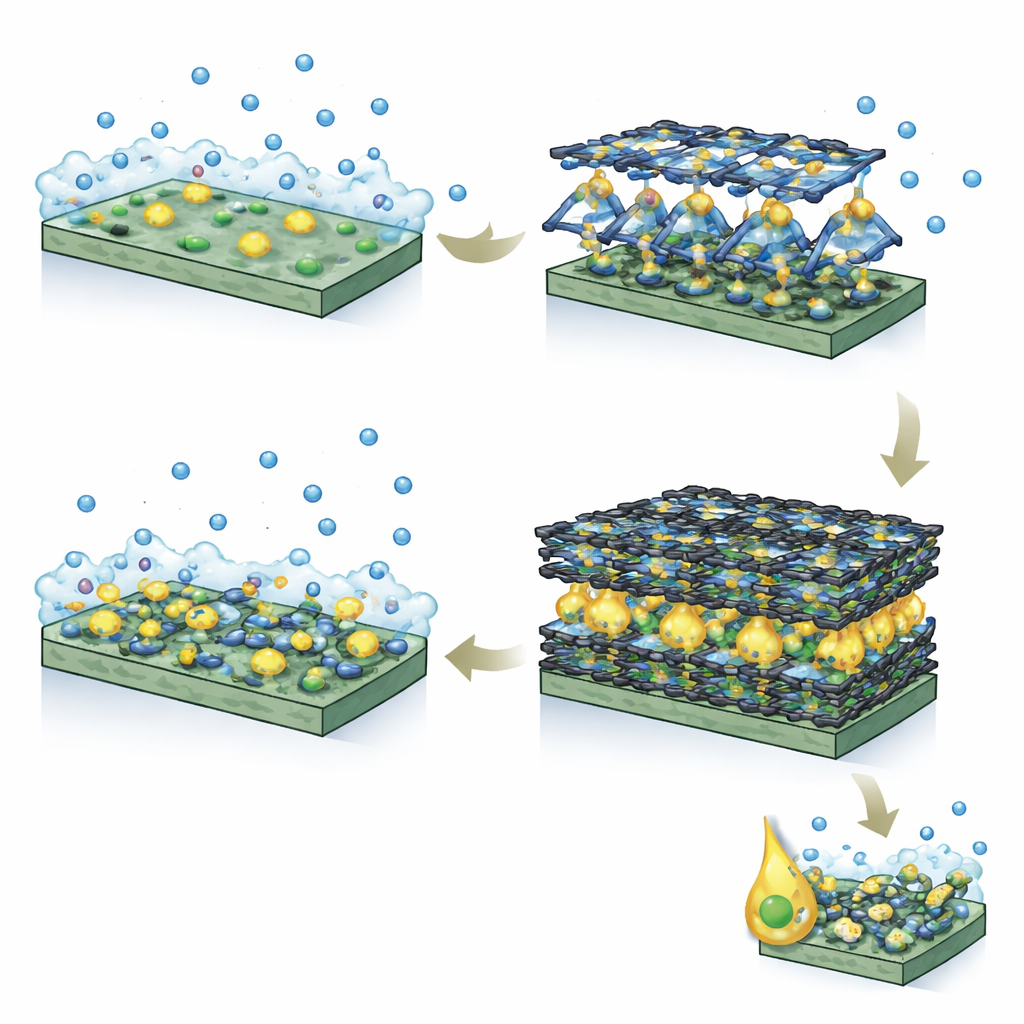
Projetando um lar microscópico melhor para álcoois graxos
A equipe sintetizou três Ni‑MOFs em camadas e os comparou com hidróxido de níquel convencional. Eles descobriram que a versão com o ligante mais longo, construída a partir de uma unidade terfenil (três anéis) chamada Ni‑TPDC, criou os arredores mais hidrofóbicos. Experimentos que mediram como gotas de octanol se espalham e quanto corante oleoso os materiais absorvem mostraram que o Ni‑TPDC atraiu aproximadamente o dobro de álcool graxo em comparação com o hidróxido de níquel. Simulações computacionais corroboraram esses achados, revelando que moléculas de octanol se aglomeram fortemente na superfície do Ni‑TPDC devido a atrações de van der Waals aumentadas em seus canais revestidos por aromáticos.
Mantendo a estrutura do arcabouço do catalisador
Uma fraqueza comum de eletrodos à base de MOFs é que eles se desfazem sob as condições severas necessárias para reações de oxidação, perdendo sua arquitetura interna cuidadosamente projetada. Aqui, difração de raios X detalhada e espectroscopia vibracional revelaram uma diferença crucial entre os três Ni‑MOFs. Nos materiais com ligantes mais curtos, os conectores orgânicos eram removidos durante a operação e a estrutura colapsava em uma fase amorfa semelhante a hidróxido de níquel. Em contraste, o Ni‑TPDC manteve seu arcabouço cristalino em camadas mesmo após muitos ciclos de ativação e horas de eletrólise. O anel benzênico extra permitiu um empilhamento forte entre ligantes vizinhos, funcionando como um conjunto de ladrilhos encaixados que seguram a rede enquanto somente a superfície externa se converte parcialmente na camada ativa de oxihidróxido de níquel.
Reações mais rápidas, menos subprodutos
Quando os pesquisadores usaram octanol como álcool graxo teste, o Ni‑TPDC superou dramaticamente o hidróxido de níquel padrão. Em voltagens relevantes, ele entregou cerca de três vezes a taxa de produção de ácido octanoico, mantendo eficiência faradaica acima de 80%, em comparação com aproximadamente 30% para o hidróxido de níquel, onde a formação de oxigênio domina. Análises cuidadosas mostraram que o Ni‑TPDC não possuía simplesmente mais sítios ativos de níquel ou uma área superficial muito maior; em vez disso, seu microambiente hidrofóbico alimentava os álcoois graxos para a zona reacional de forma mais eficaz, aliviando gargalos de transporte de massa. O catalisador otimizado completou a conversão total de octanol em ácido octanoico em apenas 3,5 horas com essencialmente 100% de seletividade, alcançando taxas de produção competitivas com métodos térmicos de oxidação de ponta que tipicamente dependem de metais preciosos.
Do conceito de laboratório a sistemas energéticos práticos
Para testar o potencial em condições reais, os autores integraram o Ni‑TPDC em uma célula de fluxo onde a oxidação de álcool graxo no ânodo é pareada com geração de hidrogênio no cátodo. Como oxidar octanol é mais fácil do que fracionar a água para formar oxigênio, a tensão total da célula caiu quase 0,2 volts em densidades de corrente práticas, reduzindo o custo energético da produção de hidrogênio enquanto simultaneamente gera ácido graxo valioso. O sistema operou de forma estável por 48 horas, com altos rendimentos tanto de hidrogênio quanto de ácido octanoico. Para não especialistas, a conclusão é que, ao projetar os arredores microscópicos de um catalisador para serem mais “amigáveis ao óleo” e ao mesmo tempo estruturalmente resistentes, é possível converter moléculas oleosas de forma limpa em água usando eletricidade renovável, abrindo caminho para uma fabricação mais verde de produtos químicos cotidianos e esquemas de energia mais eficientes movidos a hidrogênio.
Citação: Du, R., Chen, Z., Zhang, B. et al. Ligand engineering tailors hydrophobic microenvironments for efficient electrocatalytic oxidation of fatty alcohol. Nat Commun 17, 3628 (2026). https://doi.org/10.1038/s41467-026-70501-4
Palavras-chave: eletrocatalise orgânica, oxidação de álcool graxo, catalisadores hidrofóbicos, estruturas metal-orgânicas, hidrogênio verde