Clear Sky Science · ru
Генетические варианты взаимодействуют с воздействием полибромированных дифенил-эфиров и изменяют липидный гомеостаз
Почему повседневные химикаты и кровяные липиды имеют значение
Многие привычные предметы — от диванов до электроники — содержат антипирены, известные как полибромированные дифенил-эфиры (ПБДЭ). Эти соединения накапливаются в организме и связывались с неблагоприятными уровнями кровяных липидов, такими как холестерин и триглицериды. В то же время не все, кто подвергается одинаковому воздействию ПБДЭ, развивают нарушения. В этом исследовании поставлен важный для общественного здравоохранения и индивидуального риска вопрос: определяют ли наши гены, кто наиболее уязвим перед этими невидимыми загрязнителями?
Незримые загрязнители в масштабной национальной выборке
Исследователи использовали данные Китайского национального когортного проекта по биомониторингу человека — крупного репрезентативного исследования, отслеживающего воздействия окружающей среды и здоровье. Из более чем 21 000 участников они сосредоточились на 871 взрослом с детальными измерениями: уровни ПБДЭ в крови, генетические данные, сотни малых молекул (метаболитов) и стандартные показатели липидов крови — общий холестерин, «плохой» ЛПНП, «хороший» ЛПВП и триглицериды. Участников разделили на группы с высоким и низким уровнем экспозиции по суммарным ПБДЭ. Люди с более высоким воздействием ПБДЭ как правило имели более высокий общий холестерин и триглицериды и более низкий ЛПВП, хотя возраст, вес, курение и употребление алкоголя были сопоставимы между группами. Эта картина указывала на то, что ПБДЭ действительно влияют на липидный баланс — но также намекала, что дело не только в самой экспозиции.
Гены, меняющие реакцию организма на ПБДЭ
Чтобы найти «что-то ещё», команда просканировала весь геном в поисках вариантов, изменяющих влияние ПБДЭ на липиды крови. Они выявили 3571 генетический маркер в 622 регионах генома, чьи эффекты зависели от экспозиции ПБДЭ. Большинство этих вариантов расположены в некодирующей ДНК, где они влияют на силу включения соседних генов, а не на изменение самих белков. Многие находились в участках ДНК, действующих как регуляторные узлы, отмеченных открытой хроматином и особыми гистоновыми метками, и перекрывались с сайтами связывания ключевых транскрипционных факторов, контролирующих метаболизм. Когда исследователи объединили эти чувствительные к ПБДЭ варианты в поли-генетические риск‑оценки, они обнаружили, что люди с более высокими баллами имели значительно худшие липидные профили — но только при высокой экспозиции ПБДЭ. При низкой экспозиции тот же генетический риск практически не сказывался, что подчеркивает мощное взаимодействие ген–окружающая среда.
Подсказки от малых молекул в крови
Далее учёные попытались выяснить, как именно эти взаимодействия генов и загрязнителей нарушают метаболизм. С помощью метаболомики они проанализировали сотни малых молекул в крови и искали те, которые коррелировали одновременно с поли-генетическими баллами риска и с уровнями липидов. Несколько молекул выделялись, особенно аминокислота глицин, а также цитрат, желчные кислоты и глицерол-3-фосфат. Анализ путей показал, что сети, вовлечённые в антиоксидантную защиту, образование желчных кислот и выработку энергии, были сильно затронуты. Медиаторный анализ указал, что глицин действует как ключевой промежуточный компонент: генетические варианты, меняющие уровни липидов при воздействии ПБДЭ, часто делали это во многом через сдвиг уровней глицина. Поскольку глицин необходим для синтеза желчных кислот, помогающих выводить холестерин, это указывало на конкретный путь, по которому загрязнители и гены могут совместно повышать уровни липидов в крови.
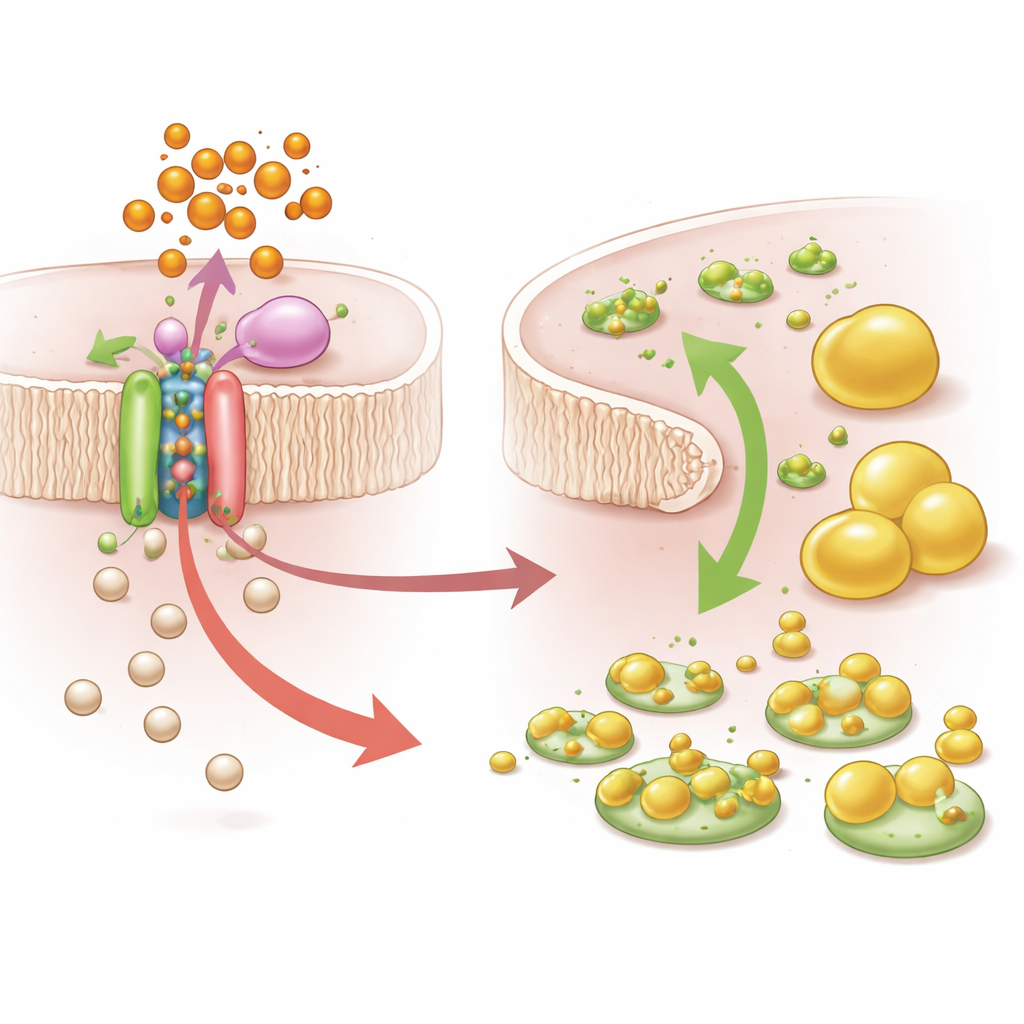
Одна буквa в ДНК, сдвигающая равновесие
Углубившись в детали, команда сосредоточилась на одном варианте, rs9869609, который был тесно связан с увеличением общего холестерина и ЛПНП при воздействии ПБДЭ. Этот вариант расположен рядом с геном SLC6A20, кодирующим транспортер, помогающий перемещать глицин в клетки. На основании данных из человеческих тканей и искусственно модифицированных печёночных клеток исследователи показали, что «рискованная» аллель rs9869609 усиливает связывание репрессора транскрипции BHLHE40, что в свою очередь подавляет активность SLC6A20. Когда клетки с рискованной аллелью подвергались воздействию распространённого ПБДЭ (BDE-47), уровни SLC6A20 снижались ещё сильнее, внутриклеточный глицин падал, и холестерин накапливался. Дополнительные эксперименты подтвердили, что блокирование SLC6A20 или уменьшение глицина ограничивало образование глицин-связанных желчных кислот и способствовало накоплению холестерина, что соответствует наблюдаемым паттернам у людей с высокой экспозицией и высоким генетическим риском.
Что это значит для здоровья и профилактики
В совокупности исследование выявляет подробный путь от повседневной химической экспозиции до нарушения липидного обмена, но только у генетически восприимчивых людей. ПБДЭ, по-видимому, ухудшают контроль холестерина, усиливая эффект определённых вариантов ДНК, которые ослабляют транспорт глицина и синтез желчных кислот, снижая способность организма выводить холестерин. Для широкой аудитории главный вывод таков: ни гены, ни среда не действуют в одиночку — тонкие различия в нашей ДНК могут решить, насколько вредным окажется данный уровень загрязнения. В будущем инструменты вроде разработанной здесь поли-генетической оценки риска могут помочь выявлять людей, которым особенно нужна защита от конкретных загрязнителей, а механистические данные о глицине и SLC6A20 могут направить разработку целевых терапий или нутриционных стратегий для смягчения метаболического воздействия неизбежных экспозиций.
Цитирование: Hu, N., Li, B., Lu, Y. et al. Genetic variations interact with polybrominated diphenyl ether exposure to alter lipid homeostasis. Nat Commun 17, 3529 (2026). https://doi.org/10.1038/s41467-026-70222-8
Ключевые слова: загрязнители окружающей среды, холестерин, взаимодействие ген–окружающая среда, метаболомика, огнестойкие ПБДЭ