Clear Sky Science · it
Variazioni genetiche interagiscono con l’esposizione a eteri difenilici polibromurati per alterare l’omeostasi lipidica
Perché le sostanze chimiche quotidiane e i grassi nel sangue contano
Molti prodotti di uso comune — dai divani ai dispositivi elettronici — contengono ritardanti di fiamma chiamati eteri difenilici polibromurati (PBDE). Questi composti possono accumularsi nei nostri corpi e sono stati collegati a livelli alterati di grassi nel sangue, come colesterolo e trigliceridi. Tuttavia non tutti esposti alla stessa quantità di PBDE sviluppano problemi. Questo studio pone una domanda rilevante per la salute pubblica e il rischio individuale: i nostri geni decidono chi è più vulnerabile a questi inquinanti invisibili?
Inquinanti nascosti in un’indagine nazionale
I ricercatori si sono basati sulla coorte nazionale cinese di biomonitoraggio umano, un grande progetto rappresentativo a livello nazionale che monitora esposizioni ambientali e salute. Da oltre 21.000 partecipanti, si sono concentrati su 871 adulti con misurazioni dettagliate: livelli di PBDE nel sangue, dati genetici, centinaia di piccole molecole (metaboliti) e lipidogrammi standard come colesterolo totale, LDL “cattivo”, HDL “buono” e trigliceridi. Le persone sono state divise in gruppi a alta e bassa esposizione in base ai loro livelli totali di PBDE. Chi aveva esposizione più alta tendeva ad avere colesterolo totale e trigliceridi maggiori e HDL più basso, nonostante età, peso, fumo e consumo di alcol fossero simili tra i gruppi. Questo schema suggeriva che i PBDE influenzano davvero l’equilibrio lipidico — ma lasciava intendere anche che qualcosa di più dell’esposizione da sola fosse in gioco.
Geni che modificano la risposta ai PBDE
Per trovare quel “qualcosa di più”, il team ha scandagliato l’intero genoma alla ricerca di varianti che modificano l’effetto dei PBDE sui lipidi ematici. Hanno individuato 3.571 marcatori genetici in 622 regioni del genoma i cui effetti dipendevano dall’esposizione ai PBDE. La maggior parte di queste varianti si trova nel DNA non codificante, dove influenzano quanto intensamente i geni vicini vengono attivati o repressi piuttosto che alterare direttamente le proteine. Molte erano in tratti di DNA che agiscono come hub regolatori, segnati da cromatina aperta e specifiche modifiche degli istoni, e sovrapponevano siti di legame per fattori di trascrizione chiave che aiutano a controllare il metabolismo. Quando i ricercatori combinarono queste varianti sensibili ai PBDE in punteggi di rischio poligenico, trovarono che le persone con punteggi più alti mostravano profili lipidici molto peggiori — ma solo se l’esposizione ai PBDE era elevata. Con bassa esposizione, lo stesso rischio genetico contava poco, evidenziando una potente interazione gene–ambiente.
Indizi dalle piccole molecole nel sangue
Successivamente, gli scienziati hanno chiesto come queste interazioni gene–inquinante disturbino effettivamente il metabolismo. Usando la metabolomica, hanno esaminato centinaia di piccole molecole circolanti nel sangue e ricercato quelle che seguissero sia i punteggi di rischio genetico sia i livelli lipidici. Diverse spiccarono, in particolare l’amminoacido glicina, insieme a citrato, acidi biliari e glicerolo-3-fosfato. L’analisi dei percorsi mostrò che reti coinvolte nella difesa antiossidante, nella formazione degli acidi biliari e nella produzione di energia erano fortemente interessate. L’analisi di mediazione indicò che la glicina in particolare agisce come un intermediario cruciale: le varianti genetiche che modificavano i livelli lipidici sotto esposizione ai PBDE spesso lo facevano in gran parte alterando i livelli di glicina. Poiché la glicina è necessaria per produrre acidi biliari che aiutano il corpo ad eliminare il colesterolo, questo suggerisce una via specifica attraverso cui inquinanti e geni possono collaborare per aumentare i grassi ematici.
Una singola lettera del DNA che fa pendere l’ago
Approfondendo, il team si è concentrato su una variante genetica, rs9869609, fortemente legata agli aumenti di colesterolo totale e LDL associati ai PBDE. Questa variante si trova vicino a un gene chiamato SLC6A20, che codifica per un trasportatore che facilita l’ingresso della glicina nelle cellule. Utilizzando dati da tessuti umani e cellule epatiche ingegnerizzate, i ricercatori hanno mostrato che la versione “a rischio” di rs9869609 aumenta il legame di una proteina repressore trascrizionale, BHLHE40, che a sua volta attenua l’attività di SLC6A20. Quando cellule portatrici della variante a rischio venivano esposte a un comune PBDE (BDE-47), i livelli di SLC6A20 diminuiscono ulteriormente, la glicina intracellulare calava e il colesterolo si accumulava. Esperimenti aggiuntivi confermarono che bloccare SLC6A20 o ridurre la glicina limitava la formazione di acidi biliari legati alla glicina e promuoveva l’accumulo di colesterolo, corrispondendo ai modelli osservati in persone con alta esposizione e alto rischio genetico.
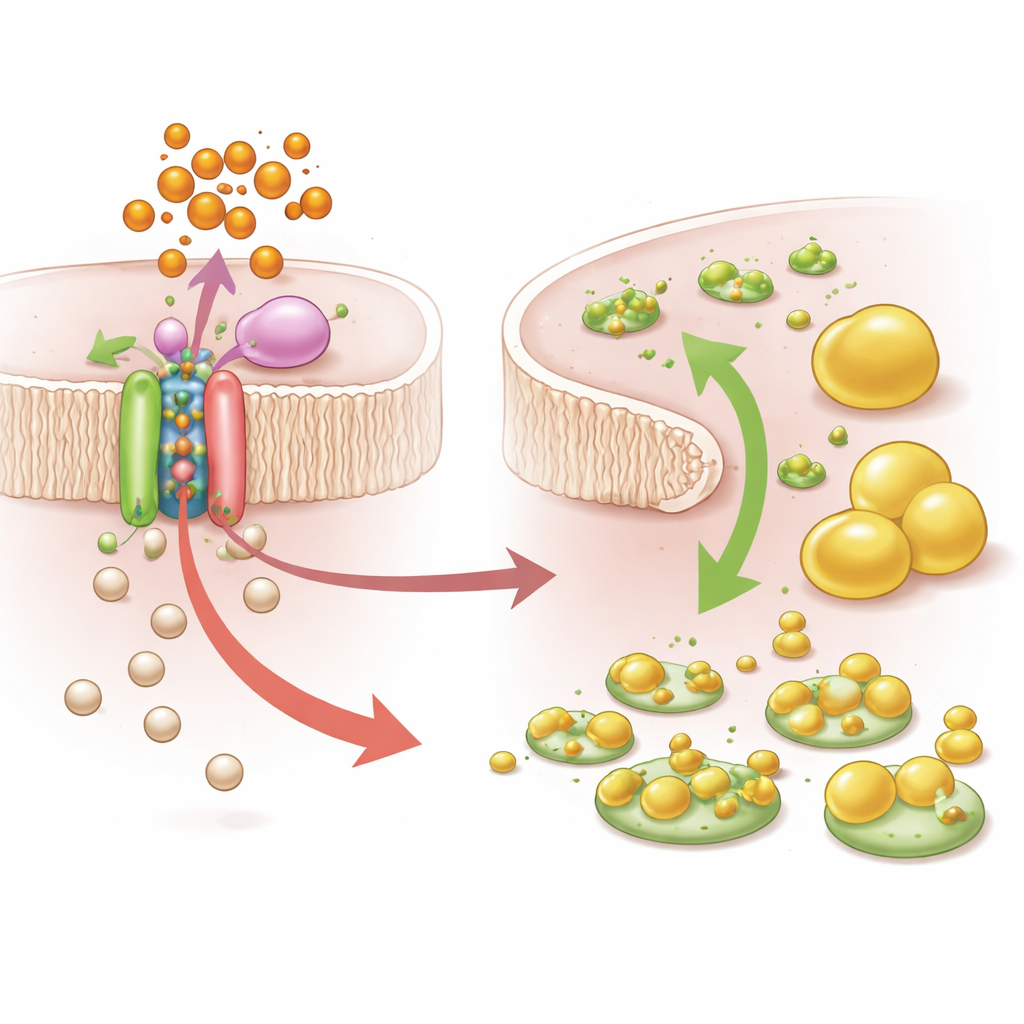
Che cosa significa per la salute e la prevenzione
Nel complesso, lo studio rivela una via dettagliata che va dall’esposizione a sostanze chimiche quotidiane all’alterazione dei grassi nel sangue, ma solo in individui geneticamente suscettibili. I PBDE sembrano peggiorare il controllo del colesterolo amplificando gli effetti di particolari varianti del DNA che indeboliscono il trasporto della glicina e la produzione di acidi biliari, riducendo la capacità del corpo di eliminare il colesterolo. Per il lettore generico, il messaggio è che né i geni né l’ambiente agiscono da soli: differenze sottili nel nostro DNA possono determinare quanto dannoso sarà un certo livello di inquinamento. In futuro, strumenti come il punteggio di rischio poligenico sviluppato qui potrebbero aiutare a identificare le persone che più hanno bisogno di protezione da specifici inquinanti, mentre le intuizioni meccanicistiche su glicina e SLC6A20 potrebbero guidare terapie mirate o strategie nutrizionali per attenuare l’impatto metabolico di esposizioni inevitabili.
Citazione: Hu, N., Li, B., Lu, Y. et al. Genetic variations interact with polybrominated diphenyl ether exposure to alter lipid homeostasis. Nat Commun 17, 3529 (2026). https://doi.org/10.1038/s41467-026-70222-8
Parole chiave: inquinanti ambientali, colesterolo, interazione gene–ambiente, metabolomica, ritardanti di fiamma PBDE