Clear Sky Science · ru
Двойная деконволюция в мультифотонной структурированной освещённой микроскопии для сверхразрешающей визуализации в глубине тканей
Взгляд глубже в живые ткани
Современная биология во многом зависит от возможности видеть мельчайшие детали внутри толстых образцов ткани, таких как срезы мозга или развивающиеся эмбрионы. К сожалению, по мере прохождения света через эти плотные среды он преломляется и искажается, из‑за чего изображения становятся размытыми именно тогда, когда учёным необходима высокая чёткость. В этой статье представлен способ цифрового «размазывания» — восстановить такие изображения, позволяя стандартному продвинутому микроскопу выявлять чрезвычайно тонкие структуры в глубине ткани без добавления дорогого и сложного оборудования.
Почему глубинная визуализация так трудна
Флуоресцентные микроскопы позволяют помечать определённые молекулы и наблюдать, как строятся и функционируют клетки и ткани. За последние десятилетия несколько методов «сверхразрешения» превзошли традиционные пределы резкости, обнаруживая детали далеко ниже 200 нанометров. Однако большинство этих подходов хорошо работают только вблизи поверхности образца. В толстых тканях, например в мозге мыши, как возбуждающий свет, так и излучение флуорофора на пути к детектору искажаются мелкими неоднородностями структуры ткани. Эти искажения, называемые аберрациями, размывают фокус микроскопа и стирают высокочастотную информацию, особенно на глубинах больше десятков микрометров.
От аппаратных исправлений к программному решению
Популярный способ борьбы с аберрациями — аппаратная адаптивная оптика, где подвижные зеркала или другие элементы формируют фронт волны света и восстанавливают чёткий фокус. Хотя такие системы мощные, они дороги, технически сложны и часто корректируют искажения только для одного цвета или одного направления распространения света за раз. Авторы предлагают вычислительный подход, совместимый с типом микроскопа, уже распространённого во многих лабораториях: лазерным сканирующим мультифотонным микроскопом. Заменив обычный одиночный детектор камерой, они регистрируют богатый набор просканированных изображений, в которых зашифрована информация о том, как ткань исказила как входящий возбуждающий свет, так и выходящее флуоресцентное излучение.
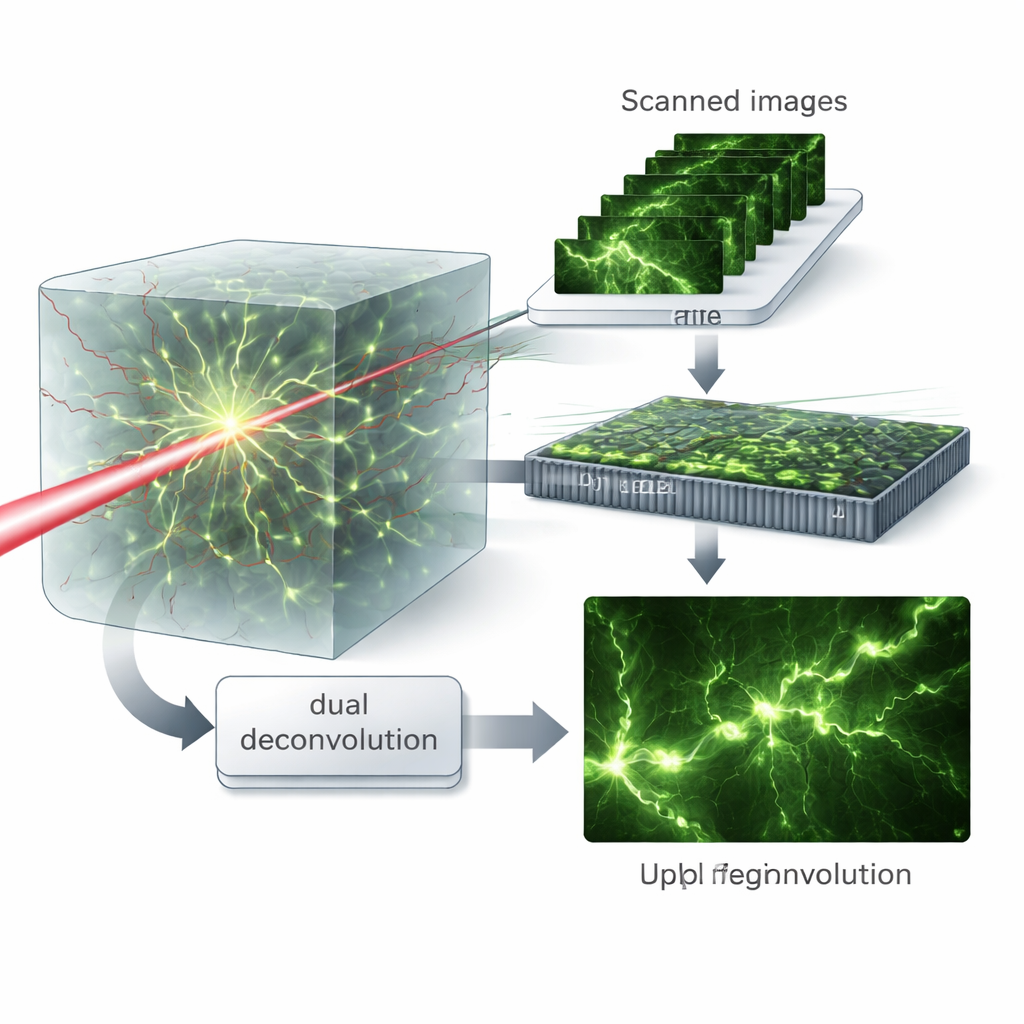
Виртуальные узоры и двойная очистка
Ключевая идея — рассматривать набор просканированных изображений так, как будто образец освещался множеством разных тонких световых узоров, концепция, которую авторы называют виртуальной структурированной подсветкой. Математическое рекомбинирование этих данных в частотной области позволяет разделить вклад процессов возбуждения и эмиссии. Затем они вводят алгоритм «двойной деконволюции», который поочередно оценивает и корректирует размытие с каждой стороны — входящего и исходящего света — вместо того чтобы сводить всё к одному эффективному размытому фильтру. Такое матричное представление сохраняет больше высокочастотных деталей и позволяет алгоритму восстанавливать тонкие структуры даже при сильных аберрациях.
Более чёткие изображения в симуляциях и реальных образцах
Чтобы проверить метод, команда сначала использовала компьютерные симуляции двухфотонной микроскопии — техники глубокого сканирования, где пара фотонов с меньшей энергией одновременно возбуждает флуоресценцию лишь в точке фокуса. При сильных моделируемых искажениях традиционные двухфотонные и стандартные реконструкции со структурированной подсветкой давали заметно размытые изображения. Напротив, двойная деконволюция восстанавливала чёткие узоры с разрешением, приближающимся к четверти длины волны флуоресценции — порядка 130 нанометров — что соответствует теоретическим ожиданиям. Затем авторы собрали пользовательскую двухфотонную установку с научной камерой и применили алгоритм к реальным образцам: флуоресцентным частицам, контрольным шаблонам за рассеивающими слоями, культивируемым клеткам, тканям мозга мыши и целым подготовкам данио-рерио. Снова и снова структуры, казавшиеся размытыми или раздвоенными на обычных изображениях, после обработки обнаруживались как разъединённые элементы, а тонкие нейронные структуры, такие как дендритные шипики, оставались разрешимыми на глубинах до 180 микрометров в ткани мозга мыши.
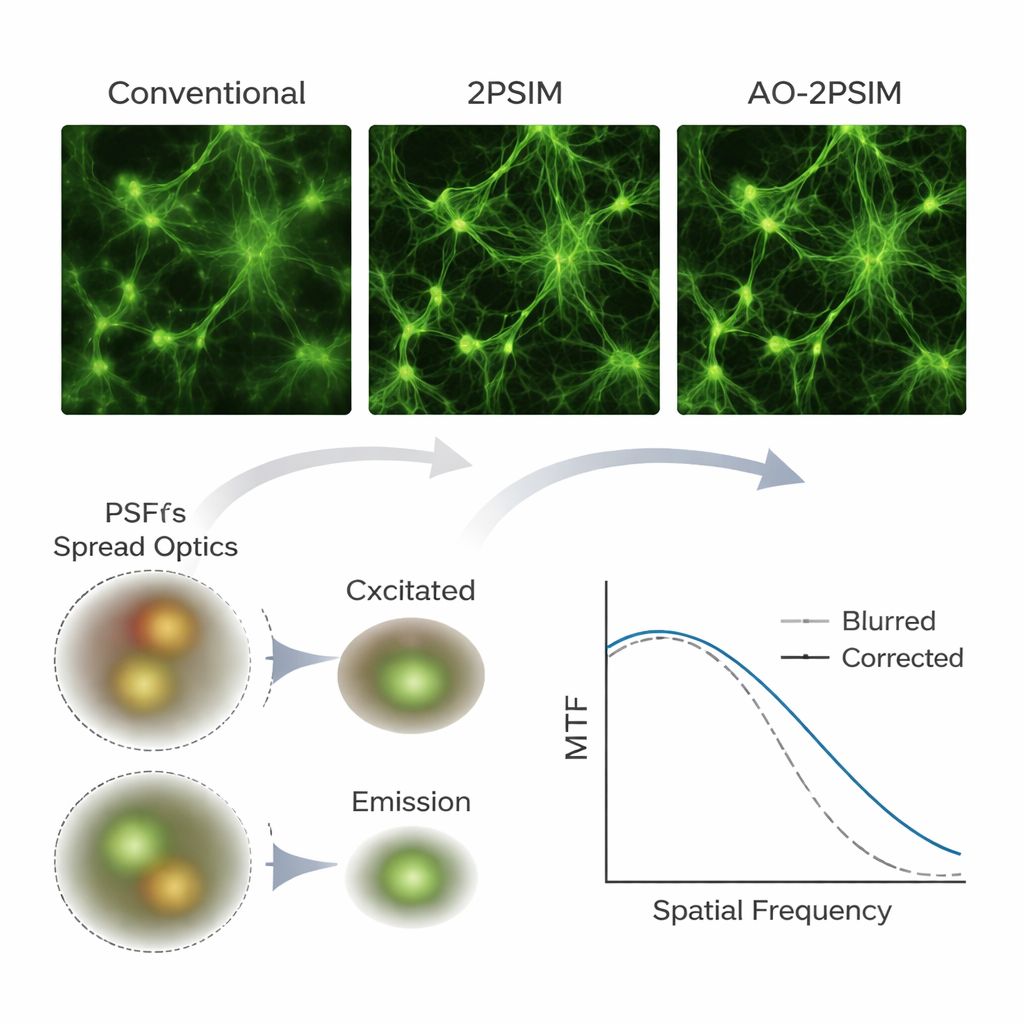
Что это значит для биологической визуализации
Для неспециалистов главное сообщение в том, что авторы показали, как с помощью преимущественно программных средств и апгрейда до камеры можно превратить существующие мультифотонные микроскопы в значительно более мощные инструменты для глубокотканной визуализации. Тщательно моделируя и корректируя, как ткани изгибают свет на входе и выходе, их подход двойной деконволюции удваивает обычный предел разрешения в сложных толстых образцах без опоры на сложные адаптивные зеркала. Хотя метод всё ещё требует достаточного сигнала и в настоящее время предполагает относительно медленное сканирование, он предлагает практичный и экономически выгодный путь к рутинному получению ультра‑чётких трёхмерных изображений мозга и других органов, открывая возможности для более детальных исследований организации и динамики биологических структур со временем.
Цитирование: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Ключевые слова: микроскопия сверхразрешения, двухфотонная визуализация, адаптивная оптика, визуализация глубоких тканей, компьютерная визуализация