Clear Sky Science · ru
DCTPP1 координирует динамику пула dCTP и стабильность мтДНК в покоящихся клетках
Сохранение здоровья «энергетических станций» клетки
Каждая клетка в нашем организме полагается на крошечные внутренние «электростанции» — митохондрии — для выработки энергии. Эти структуры несут собственный небольшой геном, митохондриальную ДНК (мтДНК), которую необходимо копировать и ремонтировать на протяжении всей жизни, даже в клетках, переставших делиться. В этом исследовании показано, как малоизвестный фермент DCTPP1 помогает контролировать химические строительные блоки, необходимые для мтДНК, и что регулирование активности этого фермента может помочь лечить редкие болезни, при которых мтДНК опасно истощается.
Строительные блоки жизни в равновесии
ДНК строится из четырёх химических «кирпичиков», известных как дезоксинуклеотиды, и клетки должны поддерживать их в нужных пропорциях. Слишком много или слишком мало любого из них может повредить ДНК и угрожать выживанию клетки. В неделящихся, или покоящихся, клетках ядро в значительной степени «не занято» копированием ДНК, но митохондриям всё ещё требуется стабильный запас этих кирпичиков для поддержания собственной ДНК. Исследователи сосредоточились на DCTPP1 — ферменте, разрушающем один конкретный кирпич, dCTP, — и изучили, как он ведёт себя в покоящихся человеческих лёгочных фибробластах, стандартной модели для исследования митохондриального гомеостаза.
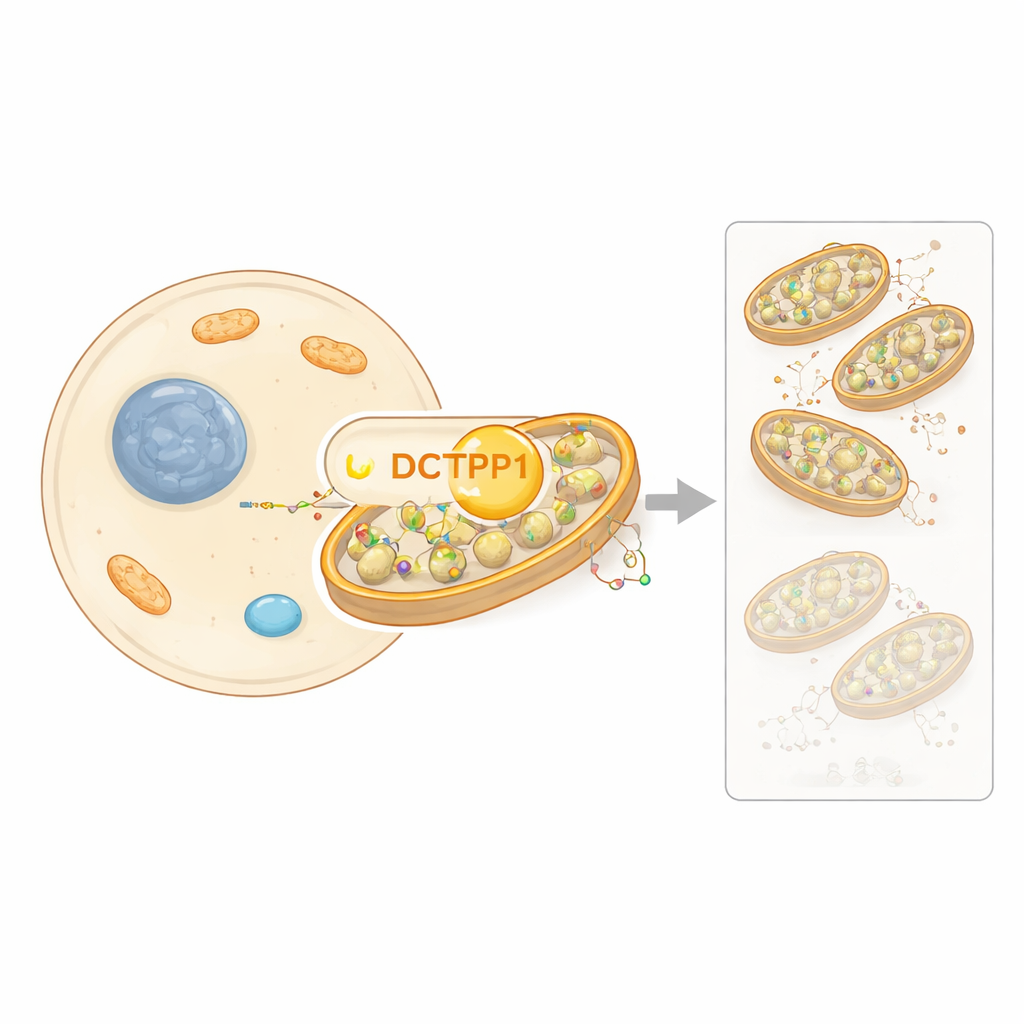
Когда клетки отдыхают, DCTPP1 перемещается в «электростанции»
Лишив клетки сыворотки роста, команда перевела их в длительное состояние покоя без гибели. Затем они измерили совокупность ферментов, которые синтезируют, перерабатывают или разрушают строительные блоки ДНК. Как и ожидалось, многие ферменты, связанные с массовым синтезом ДНК, оказались подавлены. Поразительно было то, что оставшийся DCTPP1 изменил своё местоположение: вместо того чтобы быть распределённым между ядром и цитозолем, большая его часть теперь локализовалась внутри митохондрий. Это говорит о том, что в покоящихся клетках DCTPP1 может специализироваться на управлении локальным пулом dCTP прямо там, где происходит репликация мтДНК.
Снятие «тормоза» меняет химические пулы
Чтобы проверить роль DCTPP1, учёные использовали малые интерферирующие РНК для резкого снижения его уровня как в делящихся, так и в покоящихся клетках. В делящихся клетках это привело к замедлению роста и увеличению как dCTP, так и другого строительного блока — dTTP. В покоящихся клетках утрата DCTPP1 вызвала ещё более драматическую реконфигурацию химических пулов: dCTP и dGTP стали особенно многочисленными, причём dGTP доминировал в общем составе. Эти сдвиги подтвердили, что DCTPP1 обычно действует как «тормоз» для определённых нуклеотидов и навели на мысль, что ослабление этого тормоза может влиять на способность митохондрий поддерживать свою ДНК.
Защита митохондриальной ДНК в условиях стресса
Далее команда изучила напрямую функцию митохондрий и стабильность генома. С помощью флуоресцентных красителей и методов мечения ДНК они показали, что в покоящихся клетках снижение DCTPP1 фактически сохраняло работоспособность митохондрий и увеличивало копийность мтДНК. Затем они обратились к лабораторной модели тяжёлого человеческого заболевания — митохондриального нейрогастроинтестинального энцефаломиепатии (MNGIE), при котором дефект в разложении тимидина смещает баланс строительных блоков ДНК и приводит к истощению мтДНК. Перегрузив клетки тимидином, исследователи воссоздали этот дисбаланс: уровни мтДНК падали, но их можно было восстановить либо добавлением дезоксицитидина, либо подавлением DCTPP1, что расширяло пул dCTP и спасало мтДНК.
Терапевтическая цель с перспективой лекарственной разработки
Наконец, учёные протестировали маломолекулярный ингибитор DCTPP1, TH1217, в покоящихся клетках. При низких дозах это соединение было лишь слабо токсично, но увеличивало копийность мтДНК, особенно при перегрузке тимидином, имитирующей MNGIE. Биохимические измерения показали, что TH1217 повышал уровни dCTP в соответствии с его защитным эффектом на митохондриальную ДНК. В совокупности эти результаты указывают на то, что аккуратное ослабление активности DCTPP1 может восстанавливать баланс митохондриальных нуклеотидов и помогать защищать мтДНК от истощения.
Что это значит для пациентов
Проще говоря, эта работа выделяет DCTPP1 как молекулярный «регулятор», с помощью которого клетки тонко настраивают поставки строительных блоков ДНК внутри митохондрий, особенно в долговечных неделящихся тканях, таких как мозг и мышцы. Когда dCTP в дефиците, как при синдромах истощения митохондриальной ДНК, включая MNGIE, ослабление этого регулятора позволяет клетке восстановить запасы и лучше поддерживать мтДНК. Хотя необходимы дополнительные исследования, включая эксперименты на животных и оценку безопасности, таргетирование DCTPP1 может стать новой терапевтической стратегией для стабилизации «электростанций» клетки при заболеваниях, вызванных потерей мтДНК.
Цитирование: Fernández, B., Pérez-Moreno, G., Martínez-Arribas, B. et al. DCTPP1 orchestrates dCTP pool dynamics and mtDNA stability in quiescent cells. Cell Death Dis 17, 404 (2026). https://doi.org/10.1038/s41419-026-08632-1
Ключевые слова: митохондриальная ДНК, обмен нуклеотидов, DCTPP1, MNGIE, митохондриальная болезнь